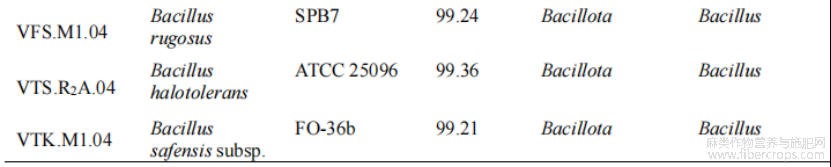摘 要:【目的】探明新疆北部罗布麻内生和根际细菌的多样性及群落组成,并筛选具有高效、专一性脱胶潜力的菌株资源。【方法】采集克拉玛依、阜康、乌鲁木齐及吐鲁番4个地区的罗布麻样品,利用16S rRNA基因高通量测序分析细菌群落结构;采用纯培养技术分离菌株,并通过刚果红染色与酶活力测定筛选具有木聚糖酶和果胶酶活性,而无纤维素酶活性的功能菌株。【结果】高通量测序共鉴定出38门345科872属的细菌。其中假单胞菌门(Pseudomonadota)和放线菌门(Actinomycetota)为优势菌门。细菌丰度与多样性表现为根际土壤>根部>叶>茎;吐鲁番样地微生物丰度和多样性低于其他三地。从样品中分离获得361株纯培养细菌,分属于4门47科86属。从中筛选出9株专性脱胶功能菌,其中7株(77.78%)为来源于茎和叶的内生菌。功能最优菌株Bacillus rugosus(VFS.M1.04)的木聚糖酶与果胶酶活力分别为2237U/mL和1002U/mL。【结论】罗布麻内生与根际细菌群落结构受所处生境与植物部位影响。Bacillus是其中的优势功能菌属,采用“同源筛选”策略从其茎、叶内生菌中能有效获得脱胶能力强、且不损伤纤维素的优良菌株,为开发罗布麻绿色生物脱胶工艺提供了宝贵的菌种资源与理论基础。
关键词:罗布麻;细菌多样性;生物脱胶;酶活力
罗布麻(Apocynum venetum L.)为夹竹桃科多年生草本灌木,广泛分布于亚洲、欧洲和北美的温带地区,尤其是在盐碱地、河岸及沙质土壤等生境中,常用作药物和纤维来源[1]。在中国北方大多省区都有生长[2],其中属新疆沙漠地区的罗布麻品质最佳[3-4]。罗布麻纤维织物因具有独特的抗菌性能和舒适性而广受关注,以其优良的纤维特性被称为“野生纤维之王”[5]。罗布麻应用历史悠久,在新疆尉犁、若羌地区,罗布麻制衣有300年历史[6],罗布麻麻秆韧皮部纤维制备的织物具有高透气性、防紫外线、抗菌等性能,对大肠杆菌、金黄色葡萄球菌和白色念珠菌抑制率可达到90%[7-8]。除此之外,罗布麻含有黄酮类、木脂素类等化合物[6],且具有耐盐碱、耐旱等特性,因此罗布麻在医学和生态学中有重要应用潜力。在新疆尉犁县围绕罗布麻已形成纺织、食品、旅游等多产业融合的发展模式,因地制宜地带动了地区经济发展[9]。
植物内生和根际细菌作为植物根际的重要组成部分,在生态结构和农业、工业生产中具有独特地位。内生和根际细菌能通过合成生长调节因子、增强植物抗氧化酶系统、分泌胞外多糖等[10-13]方法,提高植物抗逆能力和生物量。其次,内生和根际细菌会直接产生或者诱导植物提高特定分泌物的合成,这些分泌物包括有机酸、黄酮类物质和挥发性有机化合物等,它们不仅能促进植物生长,而且在医药、农业生产中也起到重要作用[14-15]。另一方面,根际和内生细菌作为特殊生境中的微生物资源,在酶制剂生产中具有重要价值,产生包括纤维素酶、淀粉酶、木糖酶、果胶酶在内的多种生物酶[16]。因此,对植物内生和根际菌株资源的挖掘在生产实践中有重要意义。
作为重要的麻类资源,罗布麻纤维的开发利用面临一个关键瓶颈——罗布麻韧皮部中含有的大量胶质,使得纤维类和非纤维类物质粘连,严重影响其可纺性[6,17]。因此,脱胶工艺一直是麻类预处理工艺中的重要环节,目前罗布麻等纤维脱胶方法主要有化学脱胶、物理脱胶、生物脱胶以及联合脱胶4种方式[18]。其中化学脱胶技术成熟但污染严重[19];物理脱胶利用微波、超声波、超临界流体等方法去除胶质,虽高效便捷,但存在脱胶效果差、纤维可纺性能不稳定的问题[17];相比之下,生物脱胶是利用微生物或其分泌的酶专一性分解胶质。早在上世纪,研究已发现霉菌、芽孢杆菌等可以分泌聚半乳糖醛酸酶和木聚糖酶等分解胶质的酶,这些微生物在一定的工艺条件下可以达到90%以上的除胶率,并且在保持麻类原有力学性能的同时对环境影响更小[20-23]。生物脱胶具有条件温和、环境友好、能耗低等突出优势,是当前最具发展潜力的绿色脱胶技术[24-25]。同时,生物脱胶技术在高效菌种的选育、工艺参数的优化以及酶系代谢调控机制等方面仍存在广阔的探索空间,具有重要的研究价值。例如:Ntabo等[26]从肯尼亚红树林分离出大量具有果胶酶、蛋白酶、几丁质酶活性的菌株。王慧慧等[21]利用异源菌株探索了对苎麻的最优脱胶条件,其中最优条件下甘露聚糖酶活力为48.25U/mL,木聚糖酶活力为44.83U/mL。然而,生物脱胶中酶制剂研发和生产成本高,另外处于异源生存环境中的脱胶菌株活性会受到影响[27]。针对这些痛点,如何获得高效且适应性强的脱胶功能菌株成为了主要焦点。对上述问题以往的研究,一方面聚焦于脱胶工程菌株的构建[28]。另一方面,随着对微生物资源的不断挖掘,特殊环境中的微生物体现出独特的适应能力,分离与麻类植物同源的野生脱胶功能菌,以及复合菌系的驯化,具有重要的研究价值[29-30]。其中利用基因工程手段构建高效工程菌株过程复杂且成本高昂,所以在特殊环境中筛选野生型功能菌株具有实际的研究意义。
新疆天山以北地区处于北温带,气候干旱、土壤盐碱化程度高。罗布麻植株在高盐高碱的胁迫下,其内生和根际微生物群落可能具备特殊的代谢特性。其独特的微生物群落具有广泛的生态学、经济学价值[31]。同时,鉴于罗布麻内生细菌和根际细菌所处环境的营养结构多为胶质[32],其中必然存在能够以胶质为碳源的菌株。为了保持纤维强度,脱胶功能菌株需要分泌高活力的木聚糖酶和果胶酶,且不分解纤维素。因此,从罗布麻自身微生态系统中同源筛选功能菌株,有望获得脱胶能力强、适应性好的优良菌种,为罗布麻的生物脱胶工艺提供核心材料支撑。
1材料与方法
1.1样品采集及处理
1.1.1样品采集
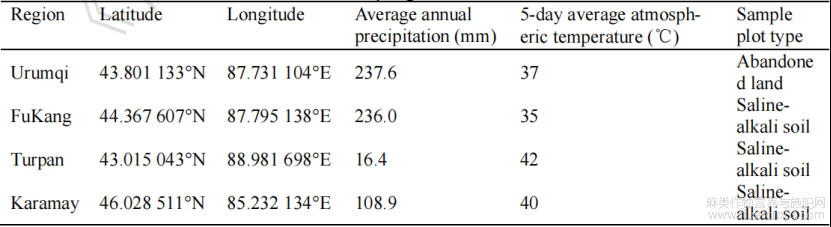
于2024年6月在新疆维吾尔自治区北部的4个区域——吐鲁番市高昌区(VT)、克拉玛依市乌尔禾区(VK)、乌鲁木齐市水磨沟区(VU)和昌吉回族自治州阜康市(VF),采集健康的罗布麻植株。每个样地采集3个重复样本,每个样本之间至少间隔3m。使用无菌器具分别收集其根部(R)、茎部(S)、叶片(L)以及根际土壤(M)。采集后立即用石蜡封存切口,并于低温保温箱中运输保存。根际土壤的采集采用“抖根法”,即抖落根部松散的大块土壤后,收集紧密附着在根系表面1−4mm范围内的土壤,存入无菌袋中低温保存。详细记录各采样点的地理坐标、年均降水量及采样时温度等信息(表1)。
免培养样品处理,取新鲜罗布麻根、茎、叶样品和根际土壤样品,其中组织样品经无菌水冲洗。用锡箔纸分别包裹各部分样品,并迅速投入液氮中速冻,随后转移至−80℃超低温冰箱中保存,用于后续高通量测序。
1.1.2样品预处理
将植物样品用无菌清水冲洗去除表面泥土,随后置于超声波清洗器中反复清洗直至水清澈。在超净工作台中,依次使用体积分数为75%的乙醇浸泡5min、体积分数为5%的次氯酸钠溶液浸泡5min进行表面消毒,每次消毒后均用无菌水冲洗3次。为验证表面消毒效果,取100μL最后一次的无菌水清洗液涂布于ISP2培养基上,于28℃培养4d,若无菌落长出,则说明表面消毒彻底。将消毒后的植物样品于无菌环境下晾干,分装于无菌试管中,4℃保存备用。根际土壤样品去除砂石等杂质后,密封于无菌试管,4℃保存。
表1采样点环境信息
1.2罗布麻内生和根际细菌高通量测序
免培养样品的细菌16S rRNA基因高通量测序委托美格基因科技有限公司完成。简要流程如下:使用FINDROP磁珠法土壤DNA提取试剂盒进行基因组DNA抽提后,利用NanoDrop One(Thermo Fisher Scientific,MA,USA)检测DNA的浓度和纯度。以基因组DNA为模板,使用带barcode的特异引物799F(5′-AACMGGATTAGATACCCKG-3′)和1193R(5′-ACGTCATCCCCACCTTCC-3′)及PremixTaq由美格基因科技有限公司对V5−V7区进行扩增,PCR反应体系(50μL):2×Premix Taq 25µL,上、下游引物(10µmol/L)各1µL,DNA模板50ng,添加ddH2O补充至50µL。PCR反应条件:94℃预变性5min;94℃变性30s,52℃退火30s,72℃延伸30s,共30个循环;72℃终延伸10min。后续建库按照NEBNext®Ultra™DNALibraryPrepKitforIllumina®标准流程进行建库操作,完成后以高通量测序平台Hiseq或Miseq进行上机测序。随后采用DADA2进行序列过滤与去噪,设置核心参数如下,截取reads片段长度,默认不做截取;reads错误碱基数,超过2则去掉该条read;设置reads最低质量值(Q值)阈值,若Reads质量值低于2,则舍弃该条read。随后使用QIIME 2降噪进行物种注释,仅保留置信度≥0.8的注释结果。
1.3罗布麻纯培养细菌分离与鉴定
1.3.1菌株分离、纯化与保藏
取20g植物样品于无菌的破碎机中粉碎,后通过无菌研钵进行充分研磨,将植物内细菌充分释放后,取1g样品于无菌试管中,进行10倍梯度稀释,稀释浓度为10-1、10-2、10-3;取1g根际土壤,稀释浓度为10-3、10-4、10-5。分别吸取100μL不同浓度的稀释液,涂布于预实验确定的4种最适培养基[33]M1(TWYE)、M2(cellulose-proline)、M6(histidine-raffinose)、R2A平板中,将平板置于28℃培养箱培养3−5d,统计各培养基中不同细菌的数量。挑取不同形态的单菌落,之后通过平板划线进行反复纯化,直至获得纯化菌株,并用30%甘油保存至−80℃超低温冰箱。菌株编号命名格式为[地区编号]+[组织部位编号]+[培养基编号]+[菌落序列号]。
本研究所有菌株信息已上传至NCBI,登录号为PX678207−PX678568。
1.3.2菌株16S rRNA基因序列扩增与测序
挑取纯化单菌落溶于5%Chelex-100的无菌溶液,于99℃下裂解10min,以释放菌体中的DNA。使用细菌的16S rRNA通用引物27F(5′-AGAGTTTGATCCTGGCTCAG-3′)和1492R(5′-TACGGYTACCTTGTTAYGACTT-3′)进行PCR扩增。PCR反应体系(25μL):
DNA模板1μL,的上、下游引物(10μmol/L)各1μL,2×EasyTaq PCR SuperMix 12.5μL,ddH2O 9.5μL。PCR扩增程序:94℃预变性5min;94℃变性1min;55℃退火1min;72℃延伸1min,共35个循环,72℃终延伸10min;4℃保存。PCR产物经1.5%琼脂糖凝胶电泳检测后,条带清晰的PCR产物送至生工生物工程(上海)股份有限公司测序。将获得序列结果通过NCBI在线标准菌株数据库(https://blast.ncbi.nlm.nih.gov/Blast.cgi)使用BLAST程序进行同源性比对,并选取相似度最高的已发表模式菌株序列作为参考。
1.4脱胶功能菌筛选与酶活力测定
1.4.1功能菌株筛选(刚果红染色法初筛)
将分离得到的细菌菌株于28℃、180r/min培养72h。取发酵液100μL接种在果胶固体筛选培养基和木聚糖固体筛选培养基中[5],置于28℃恒温培养箱72h后,向平板上倾倒0.15%刚果红染液染色处理20min,覆盖质量浓度为1mg/mL。随后弃去刚果红溶液,加入1mol/L NaCl溶液脱色处理20min。之后去除NaCl溶液,仔细观察并挑选菌落周围出现透明圈的菌株[33],初步定性选择具有木聚糖酶和果胶酶活力的菌株。
1.4.2酶活力定量测定(复筛)
采用3,5-二硝基水杨酸(3,5-dinitrosalicylic acid,DNS)比色法测定初筛阳性菌株的木聚糖酶、果胶酶及纤维素酶活力,筛选木聚糖酶和果胶酶活力高且无纤维素酶活力的菌株,具体方法如下。
首先绘制标准曲线,分别以木糖(检测木聚糖酶)、半乳糖醛酸(检测果胶酶)、葡萄糖(检测纤维素酶)使用pH5.5的磷酸缓冲液(磷酸氢二钠0.6246g和磷酸二氢钾9.078g溶于1L水中)配制1mg/mL的标准溶液。之后用磷酸缓冲液梯度稀释标准液为0.05、0.10、0.20、0.30、0.40、0.50mg/mL的系列工作液。使用DNS法测定工作液在540nm波长下的吸光度值,重复3次,以此绘制标准曲线。之后制备粗酶液,将菌株按2%的体积浓度接种于发酵培养基中,在28℃、200r/min培养24h。培养结束后,经过4℃、4000r/min离心15min,收集上清液即为粗酶液,并添加1倍体积的磷酸缓冲液稀释酶液[34]。最后进行酶促反应及酶活力测定,底物分别以果胶、木聚糖和羟甲基纤维素钠溶液作为3种酶的底物,在10mL试管中加入1.0mL相应底物溶液和0.2mL粗酶液,混匀后于50℃水浴中精确反应30min,随后立即加入2.0mL DNS试剂终止反应并显色,沸水浴5min后冷却,随后于540nm波长下测定吸光度值,酶促反应重复3次。根据标准曲线计算反应产生的还原糖量。酶活计算方法,酶活力单位(U)定义为:在上述反应条件下,每分钟催化底物产生1μmol还原糖(以相应标准品计)所需的酶量。酶活力(U/mL)按公式(1)计算。
酶活力=(还原糖含量×1000×稀释倍数)/(酶液体积×反应时间)(1)
式中:反应时间为30min,酶液体积为0.2mL。
2结果与分析
2.1罗布麻不同样地和组织部位细菌群落差异
2.1.1群落α多样性分析
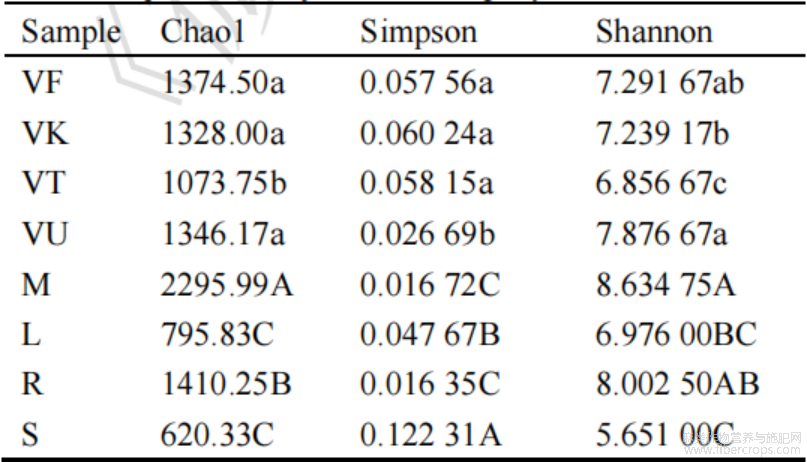
本研究对4个样地罗布麻样品的16S rRNA基因进行高通量测序,并通过α多样性指数评估其细菌群落的丰富度和多样性。不同样地及罗布麻不同部位的细菌群落结构存在差异(表2)。
对比4个采样地的α多样性发现,阜康(VF)、克拉玛依(VK)和乌鲁木齐(VU)样地的Chao1指数显著高于吐鲁番(VT),表明吐鲁番罗布麻丰富度低于其他3个样地。4个样地的Simpson指数均低于0.05,Shannon指数均高于5,表明所有样地均保持了较高的细菌物种多样性,其中乌鲁木齐(VU)的Simpson指数最低为0.02669,Shannon指数最高为7.87667,表明乌鲁木齐的罗布麻细菌群落多样性高且物种分布均匀。另外,吐鲁番罗布麻(VT)的细菌群落均匀度显著低于其他样地。
对罗布麻不同组织部位的α多样性进行比较发现,根际土壤(M)和根部(R)的Chao1指数与Shannon指数显著高于茎(S)和叶(L),表明罗布麻根和根际具有更高的细菌丰富度。茎部(S)的Simpson指数最高为0.12231,Shannon指数最低为5.65100,表明罗布麻茎中细菌群落多样性相对较低且物种均匀度较低于其他部位。相比之下,罗布麻根际土壤(M)和根部(R)的Shannon指数分别为8.63475和8.00250,Simpson指数分别为0.01672和0.01635,表现出土壤和根部中高多样性且均匀的群落特征。从组织部位整体细菌丰富度和多样性来看,其中根际土壤>根>叶>茎。
![]() 表2罗布麻细菌群落的α多样性指数
表2罗布麻细菌群落的α多样性指数
2.1.2群落β多样性分析
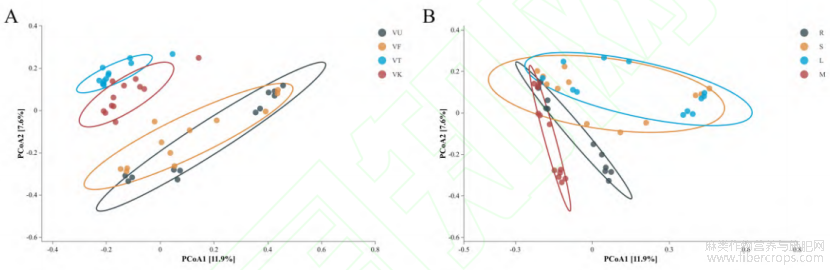
为了深入分析样品间的微生物群落结构整体差异,本研究采用了基于Bray-Curtis距离的β多样性分析方法。通过主坐标分析(principal coordinates analysis,PCoA)对样品进行了可视化展示,阜康(VF)和乌鲁木齐(VU)样品在PCoA图中的位置较为接近(图1A),表明阜康和乌鲁木齐样地的微生物群落组成具有较高的相似性。相反,克拉玛依(VK)和吐鲁番(VT)样品在图中与其他样地的样品距离较远,表示了这些样品的微生物群落组成与其他样品相比存在差异,相似性较低。从组织部位分析(图1B),发现罗布麻的茎(S)和叶(L)样品在PCoA图中的位置较为接近,这表明罗布麻茎和叶的微生物群落组成具有一定的相似性。土壤(M)和根(R)样品则与其他部位样品的距离较远,这可能反映了这些部位的微生物群落组成与其他部位相比具有较大的差异性。
图1样品β多样性PCoA主坐标分析
2.1.3罗布麻根际和内生细菌优势菌群
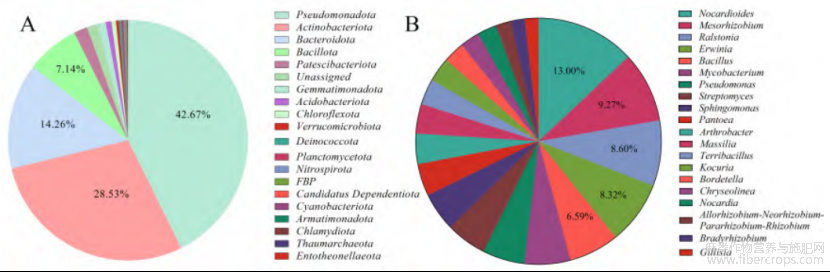
为进一步解析罗布麻细菌群落结构,通过分析16S rRNA高通量测序得到其中可观测的细菌,罗布麻内生及根际细菌群落包含38门345科872属,主要由假单胞菌门(Pseudomonadota)占42.67%、放线菌门(Actinomycetota)占28.53%、拟杆菌门(Bacteroidota)占14.26%、芽孢杆菌门(Bacillota)占7.14%,4个门构成(图2A),这4个门在整体微生物丰度中占比超过92%。然而,属水平丰度前20的细菌全部分属于这4个门(图2B),其中Actinomycetota包含类诺卡氏菌属(Nocardioides)、分枝杆菌属(Mycobacterium)、链霉菌属(Streptomyces)、节杆菌属(Arthrobacter)、考克氏菌属(Kocuria)和诺卡氏菌属(Nocardia)6个属,Bacillota拥有芽孢杆菌属(Bacillus)、土地芽孢杆菌属(Terribacillus)2个属,Bacteroidota包含金黄线菌属(Chryseolinea)和吉莱氏菌属(Gillisia)2个属,其余10个属均属于Pseudomonadota。
图2基于高通量测序的罗布内生及根际细菌整体群落组成
深入对比罗布麻不同样地和组织部位的细菌丰度,发现不同样地间特定菌属丰度有所不同(图3)。结果显示,不同样本类型中微生物属的分布存在明显差异。就不同样地而言(图3A),阜康地区的罗尔斯通氏菌属(Ralstonia)、中生根瘤菌属(Mesorhizobium)等,乌鲁木齐地区的Nocarida、鞘氨醇单胞菌属(Sphingomonas)等,克拉玛依地区的金黄杆菌属(Chryseobacterium)等属以及吐鲁番地区的鲍特氏菌属(Bordetella)、Bacillus等菌属相对丰度最高,表现了各个样地的群落特点。在不同组织中特定的细菌丰度也出现明显差异(图3B),其中,根际土壤优势菌属为Bordetella、Sphingomonas等,叶片中优势菌属为Ralstonia、Mesorhizobium等,根部的优势菌属为Mycobacterium、Nocardioides等,以及茎中的优势菌属欧文氏菌属(Erwinia)、泛菌属(Pantoea)。如图3A、3B所示,组织部位热图的颜色分布较样地热图更为集中,可能是因为植物内部不同部位对微生物群落的选择性更强,微生境对菌群结构的影响可能比不同生境差异更为显著。

图3不同组织和样地间罗布麻细菌群落在属水平的相对丰度
2.2基于纯培养的罗布麻内生和根际细菌群落特征
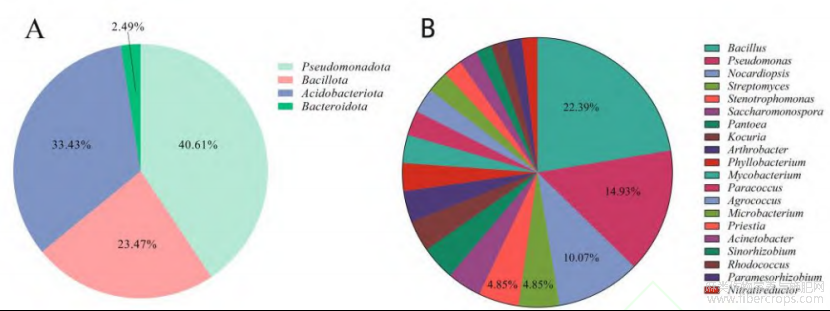
从4个地区的罗布麻样品中共分离、纯化并保藏了361株细菌,基于16S rRNA扩增子鉴定,这些菌株分属于4门8纲26目47科86属。可培养菌株在门水平,分布在Pseudomonadota(40.61%)、Actinomycetota(33.43%)、Bacillota(23.47%)和占比较少的Bacteroidota(2.49%)(图4A)。在属水平,丰度前20的主要优势属有Bacillus、Pseudomonas、Nocardiopsis,分别占比22.39%、14.93%、10.07%(图4B)。其中,各有9个菌属分别属于Actinomycetota和Pseudomonadota,另2个属为Bacillota。
图4纯培养分离菌株的群落组成
2.3高效脱胶菌株VFS.M1.04的获取
通过刚果红染色法从361株细菌中进行初筛,结果表明其中产木聚糖酶的菌株29株,产果胶酶的菌株19株,其中,同时能分解木聚糖和果胶的菌株共有15株。这些菌株分别分布在克拉玛依5株、乌鲁木齐4株、阜康3株、吐鲁番3株,其中7株(46.67%)来源于罗布麻叶片。15株脱胶功能菌分别属于Actinomycetota、Bacillota、Pseudomonadota 3个门,其中Acinetobacter和Bacillus各占4株,为优势菌属。
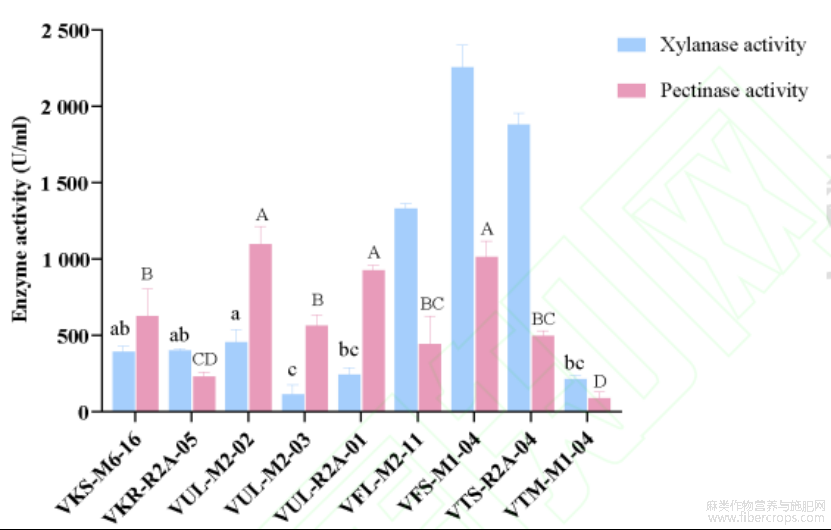
对上述15株菌进行液体发酵并测定其粗酶液的木聚糖酶、果胶酶及纤维素酶活力。得到木糖标准曲线为Y=4.4939X+0.0201,R²=0.9973;葡萄糖为Y=3.3146X−0.0524,R²=0.9926;半乳糖醛酸为Y=4.6194X+0.0256,R²=0.9969。经过酶促反应得到各菌株酶活,最终,成功筛选出9株同时具有木聚糖酶和果胶酶活性,且不具备纤维素酶活的目标脱胶功能菌株(表3)。其中,7株(77.78%)为内生菌,并多来源于罗布麻的茎和叶,2株来源于根际土壤。根据种属信息发现其中有4株Bacillus,2株为Pseudomonas。这9株菌的酶活力差异显著(图5),酶活力最高的三株菌VFL.M2.11、VFS.M1.04和VTS.R2A.04均为Bacillus。其中,菌株VFS.M1.04的酶活力最强,其木聚糖酶活力达到2237U/mL,果胶酶活力达到1002U/mL。
表3脱胶功能菌株在NCBI数据库中比对结果
图5 脱胶功能菌株酶活评价
3讨论
3.1罗布麻细菌群落结构受生境与植物部位双重影响
本研究结果显示,罗布麻内生及根际细菌群落以Pseudomonadota和Actinomycetota为优![]() 势菌门,这一发现与小麦、石斛等植物中的研究结果一致[10,35-37],表明Pseudomonadota和Actinomycetota在植物—微生物互作中可能扮演着核心角色。此外,本研究从纯培养物中分离到的菌株与高通量测序中丰度前四的门一致。在属水平上高通量中可观测丰度前二十的属中,有Bacillus、Pseudomonas、Streptomyces、Kocuria、Arthrobacter、Mycobacterium共6个属被成功分离。通过纯培养和高通量测序在不同分类水平进行对比,发现纯培养分离的细菌约占高通量测序检测到细菌群落的1/10。
势菌门,这一发现与小麦、石斛等植物中的研究结果一致[10,35-37],表明Pseudomonadota和Actinomycetota在植物—微生物互作中可能扮演着核心角色。此外,本研究从纯培养物中分离到的菌株与高通量测序中丰度前四的门一致。在属水平上高通量中可观测丰度前二十的属中,有Bacillus、Pseudomonas、Streptomyces、Kocuria、Arthrobacter、Mycobacterium共6个属被成功分离。通过纯培养和高通量测序在不同分类水平进行对比,发现纯培养分离的细菌约占高通量测序检测到细菌群落的1/10。
在不同的组织部位,发现细菌的丰富度与多样性在根际土壤中最高,并沿着根、叶、茎的生态梯度递减,这清晰地反映了从土壤到植物内部,营养环境愈发专一、生态位选择增强,细菌多样性降低。在不同生境下,本研究发现吐鲁番和克拉玛依干旱样地的细菌丰度低于阜康和乌鲁木齐。罗布麻生境一般为干旱、高盐碱的土壤,在这种胁迫生境下,罗布麻可能倾向于招募具有特定促生、抗逆功能的微生物以协助其适应逆境,并且相较于不同采样地,微生物所处的组织环境对微生物选择能力更强(图3)。
3.2 Bacillus是罗布麻微生态系统中的核心功能类群
在属水平上,Bacillus无论在总体分离菌株(22.39%)还是在脱胶功能菌株(44.4%)中均优势明显。这与骆驼刺、甘草等其他干旱区植物的细菌群落分布一致[38-39]。本研究推测这样的表现主要归因于芽孢杆菌能够产生抗逆性极强的芽孢,使其在罗布麻所处的干旱、盐碱胁迫环境中具备更强的生存优势。此外,芽孢杆菌通常能够通过产生ACC脱氨酶、铁载体和生物膜等多种方式促进植物生长与抗逆能力,这或许正是其成为罗布麻在严峻环境中不可或缺的共生伙伴的原因之一。程芬等[5]与邬金云等[40]在罗布麻及亚麻脱胶研究中也均以芽孢杆菌作为关键菌种,这与本研究结果相互印证,共同凸显了芽孢杆菌在麻类生物脱胶应用中的巨大潜力。
3.3同源筛选获得的内生菌株展现出卓越的脱胶应用潜力
经过二级筛选,本研究最终获得了9株能够同时分泌高活力木聚糖酶和果胶酶、且不分解纤维素的特异性脱胶功能菌株。本研究发现其中7株(77.78%)为内生菌,且酶活力最高的3株菌均为来源于罗布麻的茎和叶的Bacillus。造成这一结果的原因可能是罗布麻茎叶内部的特殊微环境,它们可能以果胶、半纤维素等胶质作为主要碳源,对其中定殖的内生菌构成了自然选择压力,驱使它们进化出高效分解这些特定物质的酶系。因此,采用“同源筛选”策略—即从植株自身筛选功能菌株,能够更高效地获得兼具高酶活性和高度环境适应性的优质菌种资源。
在酶活力方面,本次实验获得最优菌株Bacillus rugosus(VFS.M1.04)其木聚糖酶活力为2237U/mL,果胶酶活力为1002U/mL,对比其他异源(土壤、昆虫肠道)的脱胶菌株,酶活力优势明显。朱豪杰等[41]将从克氏原螯虾肠道筛选到的类芽孢杆菌进行发酵优化后,得到在最优条件下菌株果胶酶活力为206.37U/mL。吴丽艳等[42]从亚麻沤麻水、亚麻种植土、沤麻残渣堆积土中筛选得到的最优菌株YN1.1为芽孢杆菌,其果胶酶活为103.8U/mL木聚糖酶活为92.1U/mL。因此,来自罗布麻茎内的细菌受到长期的环境选择,对罗布麻中果胶和木聚糖的利用能力远高于其他环境的微生物。另外,对比王楚元等[43]将商用酶液直接应用于脱胶工艺,测得夏盛木聚糖酶活力为2400U/mL,丹尼悦果胶酶为3046U/mL。本研究得到菌株其果胶酶活力仍低于商业酶制剂,但源于植物内生环境的安全性和适应性,使其在开发高效、低损伤、绿色的罗布麻生物脱胶工艺中具有独特的应用价值。
4结论
本研究系统解析了新疆北部罗布麻内生及根际细菌多样性,筛选获得具有应用潜力的同源脱胶功能菌株。该植物内生及根际细菌群落以Pseudomonadota和Actinomycetota为优势类群,群落丰富度与多样性呈现土壤>根>叶>茎的特征。通过纯培养,本研究获得的361株细菌,分属4个优势门、86个属,其群落结构与高通量测序结果基本吻合,可较好表征罗布麻可培养微生物资源特征。
采用“同源筛选”策略,从罗布麻茎、叶组织中筛选获得多株高效脱胶内生菌。最优菌株Bacillus rugosus(VFS.M1.04)的木聚糖酶为2237U/mL,果胶酶为1002U/mL。实验结果表明Bacillus既是罗布麻微生态系统的优势菌属,也是脱胶功能菌株的核心类群,在生态保护与工业应用中均具潜在价值。
本研究丰富了干旱区植物——微生物互作的理论体系,为罗布麻绿色纺织加工产业提供了优良菌种资源及理论支撑,为从宿主植物特异生境中发掘高效功能菌株提供了新思路。后续将聚焦功能菌株的发酵工艺优化及脱胶应用效能评估。
参考文献
[1]Xiang T,Wu LJ,Isah MB,Chen C,Zhang XY.Apocynum venetum,a medicinal,economical and ecological plant:a review update[J].PeerJ,2023,11:e14966.
[2]肖正春,袁昌齐,束成杰,张广伦,张卫明.罗布麻类植物资源开发利用及展望[J].中国野生植物资源,2018,37(1):1-4.Xiao ZC,Yuan CQ,Shu CJ,Zhang GL,Zhang WM.Development,utilization and outlook of Apocynum resources[J].Chinese Wild Plant Resources,2018,37(1):1-4(in Chinese).
[3]苏前,邱连勇.新疆罗布麻资源概况[J].农业灾害研究,2015,5(6):61-63.Su Q,Qiu LY.Survey of Apocynum re-sources in Xinjiang[J].JOURNAL of AGRICULTURAL CATASTROPHOLOGY,2015,5(6):61-63(in Chinese).
[4]赵瑞丹,李怡鸽,董李,余小平,刘天明,王富邦.罗布麻黄酮类化合物对纺织品染色研究进展[J].西部皮革,2024,46(8):24-26.Zhao RD,Li YG,Dong L,Yu XP,Liu TM,Wang FB.Research Progress on flavonoids from Apocynum venetum for textile dyeing[J].West Leather,2024,46(8):24-26(in Chinese).
[5]程芬,张兴群,王云龙,王颖.罗布麻微生物脱胶的菌种筛选与工艺优化[J].纺织学报,2022,43(12):82-87.Cheng F,Zhang XQ,Wang YL,Wang Y.Optimizing microorganism degumming process of Apocynum and bacterial screening[J].Journal of Textile Research,2022,43(12):82-87(in Chinese).
[6]王金玉.大叶白麻可纺性纤维的联合脱胶制备工艺构建及参数优化[D].上海:东华大学,2022.Wang JY.Construction and parameter optimization of combined degumming preparation of spinnable fiber of Poacynum hendersonii[D].Shanghai:Donghua University,2022(in Chinese).
[7]Li MH,Han GT,Chen H,Yu JY,Zhang YM.Chemical compounds and antimicrobial activity of volatile oils from bast and fibers of Apocynum venetum[J].Fibers and Polymers,2012,13(3):322-328.
[8]Guo RX,Wang T,Zhou GH,Xu MY,Yu XK,Zhang X,Sui F,Li C,Tang LY,Wang ZJ.Botany,phytochemistry,pharmacology and toxicity of Strychnos nux-vomica L.:a review[J].The American Journal of Chinese Medicine,2018,46(1):1-23.
[9]李伶,刘佳.“生态+康养”加速尉犁罗布麻全产业链发展[N].巴音郭楞日报(汉)2023-09-05(05).Li L,Liu J."Ecology+Wellness"Accelerates the development of the entire Apocynum Venetum Industry Chain in Yuli[N].Bayingolin Daily(Chinese)2023-09-05(05).
[10]赵芹,邓渊钰,李伟,孙海燕,夏云磊,陈怀谷.小麦幼苗内生菌多样性的宏基因组分析[J].植物病理学报,2017,47(3):313-324.Zhao Q,Deng YY,Li W,Sun HY,Xia YL,Chen HG.Analysis of endophytes diversity in wheat seedlings by metagenomic technology[J].Acta Phytopathologica Sinica,2017,47(3):313-324(in Chinese).
[11]Armada E,Roldán A,Azcon R.Differential activity of autochthonous bacteria in controlling drought stress in native Lavandula and Salvia Plants species under drought conditions in natural arid soil[J].Microbial Ecology,2014,67(2):410-420.
[12]Xiong YW,Ju XY,Li XW,Gong Y,Xu MJ,Zhang CM,Yuan B,Lv ZP,Qin S.Fermentation conditions optimization,purification,and antioxidant activity of exopolysaccharides obtained from the plant growth-promoting endophytic actinobacterium Glutamicibacter halophytocola KLBMP 5180[J].International Journal of Biological Macromolecules,2020,153:1176-1185.
[13]Meneses C,Gonçalves T,Alquéres S,Rouws L,Serrato R,Vidal M,Baldani JI.Gluconacetobacter diazotrophicus exopolysaccharide protects bacterial cells against oxidative stress in vitro and during rice plant colonization[J].Plant and Soil,2017,416(1/2):133-147.
[14]Sudakov K,Rana A,Faigenboim-Doron A,Gordin A,Carmeli S,Shimshoni JA,Cytryn E,Minz D.Diverse effects of Bacillus sp.NYG5-emitted volatile organic compounds on plant growth,rhizosphere microbiome,and soil chemistry[J].Microbiological Research,2025,295:128089.
[15]Mondal A,Parvez SS,Majumder A,Sharma K,Das B,Bakshi U,Alam M,Banik A.Co-inoculation of Trichoderma and tea root-associated bacteria enhance flavonoid production and abundance of mycorrhizal colonization in tea(Camellia sinensis)[J].Microbiological Research,2025,293:128084.
[16]Marques NP,de Cassia Pereira J,Gomes E,da Silva R,Araújo AR,Ferreira H,Rodrigues A,Dussán KJ,Bocchini DA.Cellulases and xylanases production by endophytic fungi by solid state fermentation using lignocellulosic substrates and enzymatic saccharification of pretreated sugarcane bagasse[J].Industrial Crops and Products,2018,122:66-75.
[17]李迎澳,桂海升,浣光辉,杨帆,李仲薇,贾丽霞,何江.罗布麻纤维的化学-生物酶联合脱胶工艺[J].上海纺织科技,2024,52(3):27-31,58.Li YA,Gui HS,Huan GH,Yang F,Li ZW,Jia LX,He J.Chemical-biological enzyme combined degumming process for Apocynum venetum fibers[J].Shanghai Textile Science&Technology,2024,52(3):27-31,58(in Chinese).
[18]于春雨,郑永杰,孙颖,李端鑫,王佳怡,王大伟.麻纤维脱胶研究进展[J].黑龙江纺织,2023(4):16-19.Yu CY,Zheng YJ,Sun Y,Li DX,Wang JY,Wang DW.Research progress of hemp fiber degumming[J].Heilongjiang Textiles,2023(4):16-19(in Chinese).
[19]王亚非,吴韶华,陈韶娟,丁洪亮,冯震,王亭忠.汉麻纤维脱胶技术研究进展[J].丝绸,2024,61(8):70-79.Wang YF,Wu SH,Chen SJ,Ding HL,Feng Z,Wang TZ.Research progress on degumming technology of hemp fibers[J].Silk,2024,61(8):70-79(in Chinese).
[20]郝利民.国内外苎麻微生物脱胶研究概述[J].中国麻作,1983,5(3):28-32.HAO LM.Overview of microbial degumming research on ramie at home and abroad[J].China’s Fiber Crops,1983,(03):28-32(in Chinese).
[21]王慧慧,张非,舒潼,李攀登,吴亚,余天意,付春华,余龙江.两株芽孢杆菌在苎麻纤维复合脱胶中的应用[J].微生物学通报,2021,48(8):2512-2523.Wang HH,Zhang F,Shu T,Li PD,Wu Y,Yu TY,Fu CH,Yu LJ.Application of two Bacillus sp.strains in composite degumming of ramie fibers[J].Microbiology China,2021,48(8):2512-2523(in Chinese).
[22]Liu ZC,Duan SW,Sun QX,Peng YD,Feng XY,Zheng K,Hu ZX,Zhang YX.A rapid process of ramie bio-degumming by Pectobacterium sp.CXJZU-120[J].Textile Research Journal,2012,82(15):15531559.
[23]Xiang MX,Bai Y,Li YR,Wei ST,Shu T,Wang HH,Li PD,Yu TY,Yu LJ.An eco-friendly degumming process of flax roving without acid pickling and NaClO2-bleaching[J].Process Biochemistry,2020,93:77-84.
[24]Yang Q,Duan SW,Cheng LF,Feng XY,Zheng K,Liu ZY,Gao MQ,Peng YD.An effective degumming technology for ramie fibers based on microbial coculture strategy[J].Journal of Natural Fibers,2022,19(4):1555-1565.
[25]杨琦,段盛文,彭源德.苎麻微生物脱胶技术的研究进展[J].中国麻业科学,2018,40(1):36-42.Yang Q,Duan SW,Peng YD.Research development on microbial degumming of ramie[J].Plant Fiber Sciences in China,2018,40(1):36-42(in Chinese).
[26]Ntabo RM,Nyamache AK,Lwande W,Kabii J,Nonoh J.Enzymatic activity of endophytic bacterial isolates from selected mangrove plants in Kenya[J].The Open Microbiology Journal,2018,12(1):354-363.
[27]Wang JC,Liu ZX,Li XZ,Liu GD,Zhao J.Elucidating structure of pectin in ramie fiber to customize enzyme cocktail for high-efficiency enzymatic degumming[J].Carbohydrate Polymers,2023,314:120954.
[28]Lyu P,Zhang Y,Wang XG,Hurren C.Degumming methods for bast fibers:a mini review[J].Industrial Crops and Products,2021,174:114158.
[29]杨琦,成莉凤,冯湘沅,郑科,彭正红,段盛文.近三年麻纤维生物脱胶技术研究进展[J].中国麻业科学,2022,44(4):245-252.Yang Q,Cheng LF,Feng XY,Zheng K,Peng ZH,Duan SW.Research progress of bio-degumming technology of bast fibers in recent three years[J].Plant Fiber Sciences in China,2022,44(4):245-252(in Chinese).
[30]张越,傅佳佳,孟超然,王鸿博.亚麻生物脱胶的研究进展[J].针织工业,2024(8):84-89.Zhang Y,Fu JJ,Meng CR,Wang HB.Research progress in biological degumming method of flax fiber[J].Knitting Industries,2024(8):84-89(in Chinese).
[31]田蕾蕾,李道忠.新疆尉犁县:罗布麻产业成为“绿色”新动能[N].农民日报,2023-12-12(2).Tian LL,Li DZ.Yuli County,Xinjiang:Apocynum Venetum Industry Becomes a New"Green"Driver[N].Farmers'Daily,December 12,2023(2).
[32]王金城.基于苎麻胶质结构的脱胶酶系设计和酶的高效表达及改造[D].济南:山东大学,2023.Wang JC.Design of degumming enzymes system based on the structure of ramie gum and efficient expression and modification of enzymes[D].Jinan:Shandong University,2023(in Chinese).
[33]Musa Z,Ma JB,Egamberdieva D,Abdelshafy Mohamad OA,Abaydulla G,Liu YH,Li WJ,Li L.Diversity and antimicrobial potential of cultivable endophytic Actinobacteria associated with the medicinal plant thymus roseus[J].Frontiers in Microbiology,2020,11:191.
[34]董鹤娟,丁轲,恒子钤,贾艳艳,彭春平,罗伟光,李旺.一株土壤源高产纤维素酶芽孢杆菌的分离与鉴定[J].家畜生态学报,2013,34(6):48-52.Dong HJ,Ding K,Heng ZQ,Jia YY,Peng CP,Luo WG,Li W.Isolation and identification of a high yield cellulase Bacillus strain from soil[J].Acta Ecologiae Animalis Domastici,2013,34(6):48-52(in Chinese).
[35]李朝英,郑路.基于DNS比色法的土壤蔗糖酶检测条件选择[J].中国农学通报,2016,32(27):171-176.Li ZY,Zheng L.Soil sucrase:detection conditions based on DNS colorimetric[J].Chinese Agricultural Science Bulletin,2016,32(27):171-176(in Chinese).
[36]柳芳洲,游胜方,申知煦,龙丽,李小兰,王倩,何芋岐,秦琳,胡欢.2种基质种植下石斛根系内生菌多样性分析[J].南方农业学报,2023,54(4):1186-1197.Liu FZ,You SF,Shen ZX,Long L,Li XL,Wang Q,He YQ,Qin L,Hu H.Diversity analysis of endophytic microbes in roots of Dendrobium nobile(Lindl.)(Orchidaceae)on two substrates[J].Journal of Southern Agriculture,2023,54(4):1186-1197(in Chinese).
[37]张爱梅,郭保民,韩雪英,李曦冉.两种不同生境中国沙棘种子内生细菌的多样性[J].生态学报,2020,40(15):5247-5257.Zhang AM,Guo BM,Han XY,Li XR.Diversity of endophytic bacteria in seeds of Hippophae rhamnoides subsp.sinensis in two different habitats[J].Acta Ecologica Sinica,2020,40(15):52475257(in Chinese).
[38]Dong ZY,Rao MPN,Liao TJ,Li L,Liu YH,Xiao M,Mohamad OAA,Tian YY,Li WJ.Diversity and function of rhizosphere microorganisms between wild and cultivated medicinal plant Glycyrrhiza uralensis Fisch under different soil conditions[J].Archives of Microbiology,2021,203(6):3657-3665.
[39]木尼热·木塔力甫,叶艺洁,张芯语,艾尼江·尔斯满,张志东,王伟,楚敏.骆驼刺可培养内生细菌的分离及功能特性[J].微生物学通报,2024,51(8):2857-2869.Munire Mutalifu,Ye YJ,Zhang XY,Ainijiang Ersiman,Zhang ZD,Wang W,Chu M.Isolation and functional characterization of culturable endophytic bacteria from Alhagi sparsifolia Shap[J].Microbiology China,2024,51(8):2857-2869(in Chinese).
[40]邬金云,任燕,黄昊.罗布麻纤维的微生物脱胶[J].纺织科技进展,2021,43(9):22-25,43.Wu JY,Ren Y,Huang H.Microbial degumming of Apocynum fiber[J].Progress in Textile Science&Technology,2021,43(9):22-25,43(in Chinese).
[41]朱豪杰,何昌远,张钰昌,钱星月,石玉,冯光志.类芽孢杆菌C21产果胶酶液体发酵条件优化及其在苎麻纤维生物脱胶中的应用[J].中国酿造,2024,43(9):152-156.Zhu HJ,He CY,Zhang YC,Qian XY,Shi Y,Feng GZ.Optimization of liquid fermentation conditions of pectinase-producing Paenibacillus sp.C21 and its application in biological degumming of ramie fiber[J].China Brewing,2024,43(9):152-156(in Chinese).
[42]吴丽艳,段继强,范志祥,杜威,梁雪妮,刘飞虎.亚麻脱胶菌的分离、筛选和鉴定[J].云南大学学报(自然科学版),2007,29(4):419-423.Wu LY,Duan JQ,Fan ZX,Du W,Liang XN,Liu FH.Isolation,screening and identification of bacterium strains for accelerating flax degumming[J].Journal of Yunnan University(Natural Sciences Edition),2007,29(4):419-423(in Chinese).
[43]王楚元.苎麻复合生物酶脱胶工艺的研究[D].无锡:江南大学,2024.Wang CY.Study on degumming process of ramie by composite enzymes[D].Wuxi:Jiangnan University,2024(in Chinese).
文章摘自:周德龙,Murad Muhammad,远怡博,等.罗布麻内生与根际细菌多样性及脱胶功能菌株的挖掘[J].微生物学报,2026,66(04):1616-1630.DOI:10.13343/j.cnki.wsxb.20250924.