摘 要:【目的】探究不同浓度盐胁迫对罗布麻幼苗生长和抗氧化酶能力的影响。【方法】本研究以4个浓度梯度0、50、100和200mmol/L NaCl溶液处理罗布麻幼苗,观察不同时间罗布麻表观特征和生理生化指标变化,并分析罗布麻对不同盐胁迫的生理响应差异。【结果】短期低盐胁迫(50和100mmol/L NaCl)和长期低盐(50mmol/L NaCl)处理可促进罗布麻生长,而高浓度抑制生长;短时间盐处理罗布麻中类黄酮、叶绿素和花青素指数无明显差异,且顶部叶片花青素指数皆高于中部叶片花青素指数,与类黄酮和叶绿素指数在不同高度叶片中花青素积累量相反;随NaCl浓度增加罗布麻叶片过氧化物酶(POD)活性、还原型谷胱甘肽(GSH)含量和总黄酮含量呈上升趋势,过氧化氢酶(CAT)和抗坏血酸过氧化物酶(APX)活性呈先升高后降低趋势,在100mmol/L处理下达到最大值。【结论】50mmol/L NaCl处理可增加罗布麻生物量,罗布麻可通过提高抗氧化酶活性、GSH含量及黄酮含量来抵御盐胁迫对植物造成的损伤。该研究结果为罗布麻在盐渍化地区种植,改善盐渍化土地生态环境提供一定的理论依据。
关键词:罗布麻;盐胁迫;生物量;叶绿素;抗氧化能力;黄酮类化合物
全球气候的变化及劣质水源的灌溉加速了土壤盐碱化[1],全球约有超过8亿hm2的耕地受到盐胁迫的影响,我国盐渍土总面积约9913万hm2,占耕地面积的25%[2]。大面积的盐渍化土壤难以利用,对粮食安全、农业发展及资源保护构成威胁。因此,合理开发利用盐渍化土地,改善盐渍化土地生态环境成为我国乃至世界农业生产亟待解决的问题。
盐生植物是一类能够适应高浓度盐环境,并从中受益的植物[3],可用于盐碱地绿色开发并形成产业链,对粮食安全和生态治理具有潜在使用价值[4]。次生代谢物是植物适应逆境的产物,在植物抗逆过程中发挥重要作用[5]。其中黄酮类化合物是一类重要的次生代谢物,具有抗氧化、降血压、降血脂、抗肿瘤、抗病毒、增强免疫力等功效,并与植物的耐盐性、抗旱性等密切相关[6-13]。研究表明黄酮类化合物和抗氧化酶系统在盐胁迫中发挥着重要的作用[14],如Xu等[15]研究发现花椒叶片中黄酮类化合物可激活抗氧化酶以清除自由基,提高植物对逆境胁迫的耐受性;Chen等[16]发现盐胁迫下罗布麻中黄酮类化合物含量和抗氧化酶活性提高,保护细胞结构免受氧化损伤和渗透胁迫。由此可知,植物抗氧化酶系统和黄酮类化合物在盐胁迫中发挥着重要的作用,系统开展盐胁迫下抗氧化系统和黄酮类化合物变化规律研究,有助于进一步揭示盐生植物耐盐机制。
罗布麻(Apocynum Venetum)具有耐盐、耐旱、耐贫瘠、喜光、抗风蚀等特性,广泛分布在我国北方各省,是一种适宜栽培于盐碱地的优良经济植物[17-18]。罗布麻类植物被划分为3个种,即白麻(Apocynum Pictum)、大叶白麻(Apocynum Hendersonii)和罗布红麻(A.Venetum)。罗布红麻又称罗布麻,其叶片中含有丰富的黄酮类化合物,具有抗氧化、降血脂等药理活性[17,19,20]。目前,对罗布麻的研究主要集中在黄酮类化合物提取分离纯化、药理学研究以及逆境胁迫相关的生理与分子方面研究,对罗布麻的耐盐评价重要集中于种子和幼苗在单盐胁迫下的发芽率和生长势,以及盐胁迫条件下生理和表型的变化,而对抗氧化系统与次生代谢产物相关性方面研究较少[21-27]。
本文拟对罗布麻施加不同程度盐胁迫,系统开展罗布麻黄酮类化合物与抗氧化系统在盐胁迫下的变化规律研究,为后续进一步开展罗布麻适应盐渍化环境的分子机制奠定一定的基础。
1 材料与方法
1.1 试验材料
本试验选用罗布麻品种为罗布红麻,试验材料采集自新疆罗布泊地区(35°38'N,82°38'E)。挑选大小一致、颗粒饱满的种子,用0.5%KMnO4溶液浸泡10min,无菌水冲洗至无色后浸泡于无菌水中催芽24h,移栽至覆有滤纸的培养皿中培养,光暗周期为16h/8h,昼夜温度为26℃/22℃[28]。
1.2 方法
1.2.1 幼苗的处理方法
选择长势一致的罗布麻幼苗移栽至穴盘中,每个处理设5个重复,每个重复20株。放置于温度26℃,光照周期16L:8D,光照强度575μmol/(m2/s),相对湿度60%~70%的条件下培养,每2天更换1次1/2 Hoagland营养液。幼苗生长至6周龄时进行盐处理,浓度如下:
(1)1/2Hoagland营养液+0mmol/L NaCl
(2)1/2Hoagland营养液+50mmol/L NaCl
(3)1/2Hoagland营养液+100mmol/L NaCl
(4)1/2Hoagland营养液+200mmol/L NaCl
1.2.2 幼苗生物量的测定
盐处理24、48、72h和192h后,分别取不同浓度NaCl处理的罗布麻幼苗,测量株高根长,称量地上部分鲜重和地下部分鲜重,样品置于烘箱中80℃处理48h,冷却后称重,每个处理3个重复。
1.2.3 叶绿素、花青素和类黄酮指数的测定
植物叶绿素-多酚测量仪(Dualex,Force-A,法国)测定盐处理3、6、12、24、48、72h罗布麻顶部叶片和中部叶片(株高1/2处叶片)的叶绿素指数(Chl指数)、花青素指数(Anth指数)和类黄酮指数(Flav指数)等指标。
1.2.4 抗氧化能力和黄酮含量测定
选取盐处理192h培养的幼苗,采集同一高度位置的叶片,0mmol/L NaCl处理组为空白对照组,使用苏州科铭生物技术有限公司试剂盒测定POD、CAT、APX及GSH等指标,每个处理组5异显著性分析,GraphPad Prism 8绘制柱形图。
2 结果
2.1 不同浓度NaCl处理对罗布麻生长状况和生物量的影响
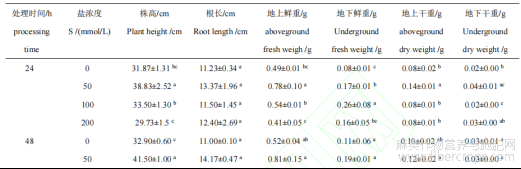
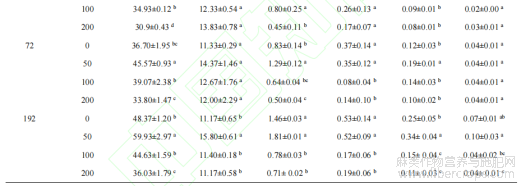
表1 不同浓度NaCl处理对罗布麻生物量的影响
注:表中数据为平均值±标准差(n=3),同列不同小写字母表示差异显著(P<0.05)。
不同浓度NaCl处理对罗布麻生长状况及罗布麻株高、根长以及地上部分和地下部分干鲜重的影响如图1及表1所示。50mmol/L NaCl处理在短期盐处理(24、48、72h)及长期盐处理(192h)期间显著促进罗布麻生长(P<0.05),与对照组相比,50mmol/L NaCl处理72h时罗布麻的罗布麻株高、地上部分鲜重、地上部分干重分别增加了24.17%、55.42%和35.00%;50mmol/L NaCl处理192h时罗布麻的株高、根长、地上部分鲜重和地上部分干重分别显著增加了23.90%、36.71%、23.97%和36.00%。100mmol/L NaCl处理的罗布麻株高、地上部分鲜重和地下部分干重在短期内高于对照组;但在长期盐处理时,100mmol/L NaCl处理罗布麻株高、地上部分和地下部分鲜重以及地上部分和地下部分干重分别下降了7.73%、46.58%、67.92%、40%和42.86%。200mmol/L NaCl处理的罗布麻株高、地上部分鲜重和地下部分干重均低于对照组。
图1 不同盐浓度NaCl胁迫192h时罗布麻幼苗生长情况
2.2 不同浓度NaCl处理对罗布麻叶片类黄酮指数的影响
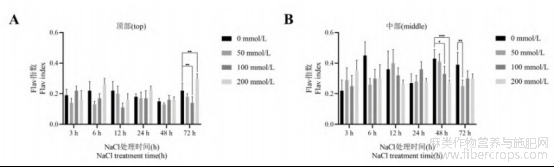
在不同浓度NaCl处理下,罗布麻中部叶片类黄酮指数总体高于顶部叶片类黄酮指数(图2)。各浓度NaCl处理3、6、12、24、48h时,罗布麻顶部叶片类黄酮指数与对照组相比无显著差异;100mmol/L NaCl处理72h时,罗布麻顶部叶片显著低于对照组;而200mmol/L NaCl处理72h时,罗布麻顶部叶片显著高于对照组(图2-A)。各浓度NaCl处理3、6、12、24h时,罗布麻中部叶片类黄酮指数与对照组相比无明显差异;NaCl处理48h时,中部叶片类黄酮指数随NaCl浓度增加呈下降趋势,且100、200mmol/L NaCl处理下罗布麻类黄酮指数显著低于对照组;50mmol/L NaCl盐处理72h时,50、100mmol/L NaCl处理下罗布麻类黄酮指数显著低于对照组(图2-B)。
图2 盐处理对罗布麻类黄酮指数的影响
注:图中数据为平均值±标准差(n=5),“*”表示在P<0.05水平上差异显著;“**”表示在P<0.01水平上差异显著;“***”表示在P<0.001水平上差异显著。
2.3 不同浓度NaCl处理对罗布麻叶绿素指数的影响
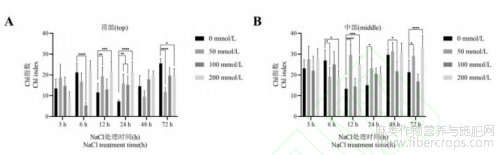
图3 盐处理对罗布麻叶绿素指数的影响
注:图中数据为平均值±标准差(n=5),“*”表示在P<0.05水平上差异显著;“**”表示在P<0.01水平上差异显著;“***”表示在P<0.001水平上差异显著;“****”表示在P<0.0001水平上差异显著。
在不同浓度NaCl处理下,罗布麻中部叶片叶绿素指数总体高于顶部叶片叶绿素指数(图3),表明中部成熟叶片中叶绿素的积累较顶部幼嫩的叶片多。50、200mmol/L NaCl处理12、24h时,罗布麻顶部叶片叶绿素指数显著高于对照组;100mmol/L NaCl处理24h时,罗布麻顶部叶片叶绿素指数显著高于对照组(图3-A)。50mmol/L NaCl处理12、24、72h时,罗布麻中部叶片叶绿素指数显著高于对照组;200mmol/L NaCl处理12、72h时,罗布麻中部叶片叶绿素指数显著高于对照组(图3-B)。
2.4 不同浓度NaCl对罗布麻叶片花青素指数的影响
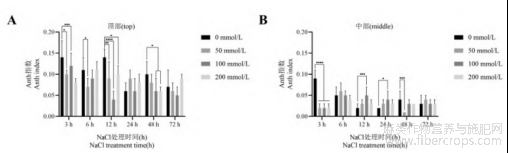
不同浓度NaCl处理下,罗布麻顶部叶片花青素指数总体高于中部叶片花青素指数(图4),与类黄酮和叶绿素指数在不同高度叶片中的积累量相反。各浓度NaCl处理下,顶部叶片花青素指数均不显著高于对照组,但200mmol/L NaCl处理6、24、72h时,顶部叶片花青素指数高于对照组(图4-A)。盐处理6、12、24、72h时,罗布麻中部叶片中花青素指数随着盐浓度增加呈先升后降趋势,在50mmol/L或100mmol/L NaCl处理下达到最大值。盐处理3h时,中部叶片的花青素指数随着盐浓度增加呈下降趋势(图4-B)。
图4 盐处理对罗布麻花青素指数的影响
注:图中数据为平均值±标准差(n=5),“*”表示在P<0.05水平上差异显著;“**”表示在P<0.01水平上差异显著;“***”表示在P<0.001水平上差异显著;“****”表示在P<0.0001水平上差异显著。
2.5 不同浓度NaCl处理对罗布麻叶片抗氧化能力的影响
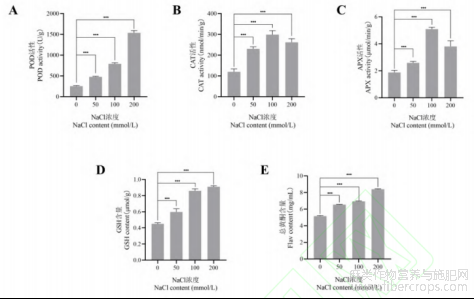
罗布麻叶片中过氧化物酶(POD)活性随NaCl浓度升高呈显著上升趋势,在200mmol/L NaCl处理下较对照组提高了506.03%(图5-A)。过氧化氢酶(CAT)和抗坏血酸过氧化物酶(APX)活性随NaCl浓度升高呈先升后降趋势,均在100mmol/L NaCl处理下酶活性最大,CAT活性在100mmol/LNaCl处理下较对照组升高了149.58%;APX活性在100 mmol/LNaCl处理下较对照组升高了172.00%(图5-B)(图5-C)。还原型谷胱甘肽(GSH)可以消除植物中活性氧伤害产生的自由基,也是最有效的过氧化物效清除剂之一[30]。罗布麻叶片中GSH含量随NaCl处理浓度的升高而增加,在200mmol/L NaCl处理下较对照组升高101.67%(图5-D)。
2.6 不同浓度NaCl处理对罗布麻叶片总黄酮含量的影响
黄酮类化合物是一类天然抗氧化剂,能够很好地清除活性氧和活性氮物质[31]。盐处理192h后,罗布麻叶片总黄酮含量增长显著(P<0.05),且随盐浓度增加呈上升趋势,在200mmol/L NaCl处理下黄酮含量达到最高值,与对照组相比提高62.68%(图5-E)。
图5 盐处理对罗布麻POD活性(A)、CAT活性(B)、APX活性(C)、GSH(D)含量及总黄酮(E)含量的影响
注:图中数据为平均值±标准差(n=5),“***”表示在P<0.001水平上差异显著。
3 讨论
3.1 NaCl胁迫对罗布麻生物量积累及光合色素的影响
盐胁迫促使植物减缓生长、改变形态特征、重新构建生物量分配格局来维持其在逆境下的存活,而株高和生物量则是植物受胁迫后的直观表现[32,33]。本研究表明,低盐胁迫(50mmol/L NaCl)及短时间盐胁迫(72h内)能促进罗布麻株高、根长以及地上部分和地下部分干鲜重的增加,表明罗布麻在此条件下具备一定的耐盐能力。然而高盐胁迫(200mmol/L NaCl)及长时间盐胁迫则显著抑制生长,这与前人研究一致[34,35]。
生物量的积累依赖于光合作用的效率,叶绿素作为植物光合作用的主要色素,其含量变化在一定程度上可以表征植株的耐盐性[36]。本研究发现,除6h外,短期低盐胁迫处理显著提高了罗布麻中部叶片叶绿素指数。这可能是由于植物在低盐胁迫下为保持自身较强的蒸腾作用和光合作用,促进光合色素的合成,从而增加植物生物量[37]。罗布麻作为拒盐植物,可将Na+积累在根茎结合处的木质部薄壁组织中,使溶解在土壤水分中的盐分难以进入根内,减轻其对细胞质的离子毒性[38,39]。在本研究中,高盐胁迫处理3、48、72h时,罗布麻中部叶片叶绿素指数升高,这反映了罗布麻在高盐胁迫下短期内维持光合作用的能力。此外,中部叶片的叶绿素积累普遍高于顶部叶片,这与叶片发育程度有关,成熟叶片更稳定的光合系统可能是其在胁迫下维持光合作用的关键[40]。
黄酮类化合物作为重要的次生代谢产物和抗氧化剂,其变化不仅参与光保护,也响应盐胁迫诱导的氧化损伤[41-43]。本研究发现,罗布麻中部叶片花青素指数随NaCl浓度增加多呈先升后降趋势,在50和100mmol/L NaCl处理时达到峰值,表明低盐胁迫、中度盐胁迫(100mmol/L NaCl)诱导了花青素的合成以应对盐胁迫诱导产生的活性氧(ROS),但严重的盐胁迫可能抑制其合成。陈斌等[44]研究表明花色素苷含量与光照强度呈正相关,在本研究中,罗布麻顶部叶片花青素含量显著高于中部叶片,这与其接受更高光照强度直接相关。总黄酮含量在长期盐胁迫下(192h)随NaCl浓度增加而上升,这与Agati等[45]在紫外辐射和根区盐度同样增强了牛至叶片中黄酮类化合物的生物合成的研究结果一致,说明罗布麻通过提高总黄酮的含量增强其耐盐能力。然而短期盐胁迫下,类黄酮变化无明显规律,且顶部叶片类黄酮指数低于中部叶片,这可能是由光照强度的差异引起的,中部叶片可能在适度光照下更有利于黄酮类物质的合成积累[43]。叶绿素、花青素和其他黄酮类化合物可能构成相互关联的生理响应网络以维持光合作用效率。低盐胁迫下叶绿素、花青素和其他黄酮类化合物的增加促进罗布麻光合作用并清除活性氧,共同促进了罗布麻生物量的积累;在高盐胁迫或长期盐胁迫下,叶绿素、花青素含量下降,而其他黄酮类化合物持续上升以抵抗氧化胁迫,维持罗布麻的生理功能和耐盐能力。
3.2 NaCl胁迫对罗布麻抗氧化酶活性的影响
盐胁迫诱导ROS大量产生,对植物细胞造成氧化损伤[46,47]。植物进化出复杂的抗氧化防御系统,包括酶促系统(POD,CAT,APX)和非酶促抗氧化剂(GSH)来清除ROS[47-53]。
POD活性在高盐胁迫下仍能保持上升趋势,与龙明秀等[54]对紫花苜蓿的研究结果相同,表明POD在罗布麻受到盐胁迫时持续清除ROS,在罗布麻盐胁迫响应中起重要作用。在低、中度盐胁迫下,CAT和APX活性的增强是清除ROS的有效补充途径,与POD协同维持细胞内的低ROS水平,保护细胞结构和功能,但在高盐胁迫下CAT和APX活性的显著下降,可能是由于高浓度盐离子造成的严重细胞损伤所致,与此浓度下罗布麻生物量、叶绿素含量下降相应,这与藜麦和盐肤木等植物中CAT、APX活性在高盐胁迫下的抑制现象相一致[50-52]。GSH是植物体内重要的抗氧化剂,GSH可以有效还原-S-S键,稳定-SH族,稳定膜蛋白结构,GSH的积累是对活性氧(ROS)升高的响应,是植物适应极端环境的一种表现[55,56]。GSH含量随盐浓度升高持续增加,与NaCl胁迫下盐穗木体内GSH变化的研究结果一致[57]。
综上所述,本研究发现罗布麻抗氧化系统对盐胁迫的响应过程如下,POD活性在不同盐浓度胁迫下持续上升,CAT和APX活性则呈先上升后下降的趋势,并在100mmol/L NaCl达到峰值,而GSH含量在不同盐浓度胁迫下保持上升趋势。在低、中度盐胁迫下,抗氧化酶、GHS和黄酮类化合物协同清除ROS。在高盐胁迫下,罗布麻对盐胁迫的响应发生改变,CAT、APX等抗氧化酶活性受到抑制,但GSH及总黄酮含量却显著上升,表明高盐胁迫下罗布麻更依赖于非酶促物质,如GSH和黄酮类化合物,以补偿抗氧化酶损伤和失活导致的抗氧化能力下降。黄酮类化合物、GSH及抗氧化酶可能形成协同的抗氧化网络,共同维持罗布麻的氧化还原稳态。
4 结论
探究罗布麻对盐胁迫的生理响应与适应机制对合理开发利用盐碱地、改善盐渍化土地生态环境具有重要意义,本研究通过罗布麻的生长和生理生化指标变化分析得出,低浓度盐胁迫可促进罗布麻生长,而在高浓度盐胁迫下,罗布麻可能通过多层次的抗氧化系统清除过量的ROS,抵抗盐胁迫诱导产生的氧化胁迫。低浓度盐胁迫下,抗氧化酶、GSH以及黄酮类化合物共同应对氧化胁迫,而在高浓度盐胁迫下,CAT、APX等部分抗氧化酶活性下降,GSH和黄酮类化合物含量升高,补偿罗布麻的抗氧化能力,抵御盐胁迫对罗布麻的氧化损伤。该研究结果为后续进一步开展罗布麻耐盐分子机制研究提供了一定的理论依据。
参考文献:
[1]Di Bella CE,Jacobo E,Golluscio RA,Rodriguez AM.Effect of cattle grazing on soil salinity and vegetation composition along an elevation gradient in a temperate coastal salt marsh of Samborombón Bay (Argentina) [J].Wetlands Ecology and Management,2014,22(1):1-13.
[2]Fu Y,Wan L.,Xiao D,Le BT.Remote sensing inversion of saline and alkaline land based on reflectance spectroscopy and D-TELM algorithm in Wuyuan areas.Infrared Physics & Technology,2020,109:103367-103378.
[3]Bosel J,Moreno AR,Shabala S.ROS homeostasis in halophytes in the context of salinity stress tolerance [J].Journal of Experimental Botany,2014,65(5):1241-1257.
[4]Flowers TJ,Colmer TD.Salinity tolerance in halophytes [J].New Phytologist.2008,179(4):945-963.
[5]Ahanger MA,Bhat JA,Siddiqui MH,Rinklebe J,Ahmad P.Silicon and secondary metabolites integration in plants:A Significant association in stress tolerance.[J].Journal of Experimental Botany,2020,71(21):291-339.
[6]Shen N,Wang TF,Gan Q,Liu S,Wang LI,Jin B.Plant flavonoids:Classification,distribution,biosynthesis,and antioxidant activity [J].Food Chemistry,2022,383:132531-132544.
[7]Abed O.Potential of flavonoid in Mahkota Dewa to reduce sistolic and diastolic blood pressure in patient with hypertension [J].Cardiovascular and Cardiometabolic Journal,2020,1:26-30.
[8]Tu LL,Wang R,Fang Z,Sun MG,Sun XH,Wu JH,Dang YL,Liu JH.Assessment of the hypoglycemic and hypolipidemic activity of flavonoid-rich extract from Angelica keiskei [J].Molecules,2022,27(19):6625-638.
[9]Kong FS,Ding ZD,Zhang K,Duan WJ,Qin YR,Su ZP,Bi YG.Optimization of extraction flavonoids from Exocarpium Citri Grandis and evaluation its hypoglycemic and hypolipidemic activities [J].Journal of Ethnopharmacology,2020,262:113178.
[10]Badshah SL,Faisal S,Muhammad A,Poulson BG,Emwas AH,Jaremko M.Antiviral activities of flavonoids [J].Biomedicine & Pharmacotherapy,2021,140:111596.
[11]陶爱恩,张晓灿,杜泽飞,赵飞亚,夏从龙,段宝忠.黄精属植物中黄酮类化合物及其药理活性研究进展[J].中草药,2018,49(09):2163-2171.TAO Aien,ZHANG Xiancan,DU Zefei,ZHAO Feiya,XIA Conglong,DUAN Baozhong.Research progress on flavonoids in plants of Polygonatum Mill.and their pharmacological activities [J].Chinese Traditional and Herbal Drugs,2018,49(09):2163-2171.
[12]Li BZ,Fan RN,Sun GL,Sun T,Fan YT,Bai SL,Guo SY,Huang SQ,Liu J,Zhang H,Wang PT,Zhu XH,Song CP.Flavonoids improve drought tolerance of maize seedlings by regulating the homeostasis of reactive oxygen species [J].Plant and Soil,2021,461:389–405.
[13]柳福智,王宁.外源海藻糖对NaCl胁迫下甘草幼苗生长及总黄酮含量的影响[J].中草药,2020,51(24):6345-6353.LIU Fuzhi,WANG Ning.Effects of exogenous trehalose on growth of Glycyrrhiza uralensis seedlingsand total flavonoid content under salt stress [J].Chinese Traditional and Herbal Drugs,2020,51(24):6345-6353.
[14]Stefanov M,Yotsova E,Gesheva E,Dimitrova V,Markovska Y,Doncheva S,Apostolova EL.Role of flavonoids and proline in the protection of photosynthetic apparatus in Paulownia under salt stress [J].South African Journal of Botany,2021,139:246-253.
[15]Xu HD,Fan JH.Macroporous adsorption resin purification of total flavonoids from the crude extract of Zanthoxylum bungeanum leaves and their reducing power and free radical scavenging activity [J].Food Science,2010,31:111–115
[16]Chen C,Wang CC,Liu ZX,Liu XH,Zou LS,Shi JJ,Chen SY,Chen JL,Tan MX.Variations in physiology and multiple bioactive constituents under salt stress provide insight into the quality evaluation of Apocyni Veneti Folium [J].International Journal of Molecular Sciences,2018,19(10):3042-3058
[17]邵德义,王悦,朱爱国,朱爱国,陈继康,高钢,陈平,陈坤梅,哈尼帕·哈再斯,喻春明.伊犁河谷罗布红麻资源调查及其黄酮抗氧化研究[J].植物遗传资源学报,2022,23(5):1362-1370.SHAO Deyi,WANG Yue,ZHU Aiguo,CHEN Jikang,GAO Gang,CHEN Ping,CHEN Kunmei,Hanipa Hazaisi,YU Chunming.Investigation on Apocynum venetum L.Resources in lli river valley and anti-oxidative activity of their flavonoids[J],Journal of Plant Genetic Resources,2022,23(5):1362-1370.
[18]吕海祥,田长彦,王梓宇,张科.外源硒对罗布麻幼苗生长及光合作用的影响[J].干旱区地理,2015,38(01):83-89.LV Haixiang,TIAN Changyan,WANG Ziyu,ZHANG Ke.Effects of exogenous selenium on growth and photosynthesis of Apocynum venetum L.seedlings [J].Arid Land Geography,2015,38(1):83-89.
[19]陈思如,张任翔,张学治,赵文慧,戎郁萍,邓波,王莉,刘起棠,刘雷震.基于MaxEnt优化模型的罗布麻类植物潜在分布研究[J].北京师范大学学报(自然科学版),2023,59(3):377-387.CHEN Siru,ZHANG Renxiang,ZHANG Xuezhi,ZHAO Wenhui,RONG Yuping,DENG Bo,WANG Li,LIU Qitang,LIU Leizhen.Potential distribution of Apocynum based on MaxEnt optimization model[J].Journal of Beijing Normal University(Natural Science),2023,59(3):377-387.
[20]Lu L,Zhang D,Sun B,Hu YW,Yan M,Liu K,Li XJ,Ren LQ.Apocynum leaf extract inhibits the progress of atherosclerosis in rats via the AMPK/Mtor pathway [J].Pharmazie,2017,72(1):41-48.
[21]Shao DV,Gao G,Abubakar AS,Hazaisi H,Chen P,Chen JK,Chen KM,Wang XF,Wang Y,Chen Y,Yu CM,Zhu AG.Total flavonoids extracts of Apocynum L.from the Ili River Valley Region at different harvesting periods and bioactivity analysis [J].Molecules,2022,27(21):7343-7358.
[22]Fu HM,Yin CL,Shen ZY,Yang MH.Flavonoids from the leaves of Apocynum venetum and their anti-inflammatory activity [J].Journal of Chemical Research,2022,46(1):1-4.
[23]Wang M,Ren TT,Huang RH,Li YQ,Zhang CS,Xu ZC.Overexpression of an Apocynum venetum flavonols synthetase gene confers salinity stress tolerance to transgenic tobacco plants[J].Plant Physiology and Biochemistry,2021,162:667–676.
[24]李茹玉,柴薇薇,郭晓农,王雪梅,韦良贞,韦兴英,徐瑛.盐处理对罗布麻(Apocynum venetum)幼苗渗透调节的影响[J].分子植物育种,2020,18(12):4105-4110.Li Ruyu,Chai Weiwei,Guo Xiaonong,Wang Xuemei,Wei Liangzhen,Wei Xingying,Xu Ying.Effect of salt treatment on osmotic adjustment of Apocynum venetum seedlings [J].Molecular Plant Breeding,2020,18(12):4105-4110.
[25]王珊,李静,吴玉洁,李晓刚,封晓辉.盐胁迫对罗布麻生长和生理的影响[J].草业科学,2022,39(9):1832-1841.WANG Shan,LI Jing,WU Yujie,LI Xiaogang,FENG Xiaohui.Effects of salt stress on the growth and physiology of Apocynum venetum [J].Pratacultural Science,2022,39(9):1832-1841.
[26]徐宗昌,周金辉,张成省,李义强.我国罗布麻种质资源研究利用现状[J].植物学报,2018,53(3):382-390.XU Zongchang,ZHOU Jinhui,ZHANG Chengsheng,LI Yiqiang.Review ofcurrent research and utilization status of Apocynum venetum germplasm in China[J].Chinese Bulletin of Botany,2018,53(3):382-390.
[27]甄熙,刘旭洋,张晓明,宛涛.盐胁迫下基于TMT技术的罗布麻蛋白质组学分析[J].西北植物学报,2024,44(2):205-218.ZHEN Xi,LIU Xuyang,ZHANG Xiaoming,WAN Tao.TMT-based proteomic analysis of Apocynum venetum under salt stress[J].Acta Botanica Boreali-Occidentalia Sinica,2024,44(2):205-218.
[28]任婷婷,任宏伟,杜海娜,张成省,李义强,高婷,徐宗昌.罗布麻EMS突变体库构建及黄酮变异突变体筛选[J].植物遗传资源学报,2020,21(3):655-662.REN Tingting,REN Hongwei,DU Haina,ZHANG Chengsheng,LI Yiqiang,GAO TING,XU Zongchang.Construction of EMS mutant library and screening of total flavonoid content mutants of Apocynum venetum L.[J].Journal of Plant Genetic Resources,2020,21(3):655-662.
[29]张晋,陈杨,曹飒丽,尹兴斌,祁娟娟,张慧,党晓芳,倪健.水煎煮法提取葛根总黄酮的动力学模型适用性研究[J].中国中药杂志,2013,38(17):2788-2792.ZHANG Jin,CHEN Yang,CAO Sa-li,YIN Xing-bin,QI Juanjuan,ZHANG Hui,DANG Xiaofang,NI Jian.Study on applicability of kinetic model for water extracts from Puerariae Radix [J].China Journal of Chinese Materia Medica,2013,38(17):2788-2792.
[30]陈晶,庞思琪,赵秀兰.外源生长素对镉胁迫下玉米幼苗生长及抗氧化系统的影响[J].植物生理学报,2016,52(8):1191-1198.CHEN Jing,PANG Siqi,ZHAO Xiulan.Effects of exogenous auxins on growth and antioxidation system in maize seedlings under cadmium stress [J].Plant Physiology Journal,2016,52(8):1191-1198.
[31]Kaur H,Sirhindi G,Bhardwaj R,Alyemeni MN,Siddique KHM,Ahmad P.28-homobrassinolide regulates antioxidant enzyme activities and gene expression in response to salt-and temperature-induced oxidative stress in Brassica juncea [J].Scientific Reports,2018,8(1):8735-8745
[32]邓甜甜,刘倩钰,何金金,廖飞勇.不同盐胁迫对紫金牛生长以及生理的影响[J].生态科学,2023,42(3):53-60 DENG Tiantian,LIU Qianyu,HE Jinjin,LIAO Feiyong.Effects of different salt tress on growth and physiology of Ardisia japonica [J].Ecological Science,2023,42(3):53-60.
[33]杨发荣,刘文瑜,黄杰,魏玉明,金茜.不同藜麦品种对盐胁迫的生理响应及耐盐性评价[J].草业学报,2017,26(12):77-88.YANG FaRong,LIU WenYu,HUANG Jie,WEI YuMing,JIN Qian.Physiological responses of different quinoa varieties to salt stress and evaluation of salt tolerance [J].Acta Prataculturae Sinica,2017,26(12):77-88
[34]熊韬,闫淼,王豪杰,毛建才,王江涛,胡国智.盐碱胁迫对甜瓜种子萌发及幼苗生长发育的影响[J].新疆农业科学,2022,59(8):1965-1974.XIONG Tao,YAN Miao,WANG Haojie,MAO Jiancai,WANG Jiangtao,HU Guozhi.Effects of saline-alkali stress on seed germination and seedling growth of Muskmelon [J].Xinjiang Agricultural Sciences,2022,59(8):1965-1974.
[35]谷艳芳,丁圣彦,李婷婷,王欣,李俊娇,张丽霞.盐胁迫对冬小麦幼苗干物质分配和生理生态特性的影响[J].生态学报,2009,29(2):840-845 GU Yanfang,DING Shengyan,LI Tingting,WANG Xin,LI Junjiao,ZHANG Lixia.Effects of saline stress on dry matter partitioning and ecophysiological characteristics of winter wheat seedlings [J].Acta Ecologica Sinica,2009,29(2):840-845.
[36]Lutts S,Kinet J M,Bouharmont J.NaCl-induced senescence in leaves of rice (Oryza sativa L.) cultivars differing in salinity resistance [J].Annals of Botany,1996,78:389-398.
[37]韩浩章,王晓立,张丽华,李素华,王芳,张颖,刘宇.盐碱胁迫对榉树幼苗生长期生理特性的影响[J].中国野生植物资源,2021,40(1):9-14 Han Haozhang,Wang Xiaoli,Zhang Lihua,Li Suhua,Wang Fang,Zhang Ying,Liu Yu.Effects of saline-alkali stress on physiological characteristics of beech seedling [J].Chinese Wild Plant Resources,2021,40(1):9-14
[38]薛琼琼,赵露露,王云霞,赵猛.盐生植物耐盐性研究进展[J].中国野生植物源,2021,40(5):60-65.Xue Qiongqiong,Zhao Lulu,Wang Yunxia,Zhao Meng.Research progress on salt tolerance of halophytes [J].Chinese Wild Plant Resources,2021,40(5):60-65.
[39]Yu J J,Chen S X,Zhao Q,Wang T,Yang CP,Diaz C,Sun GR,Dai SJ.Physiological and proteomic analysis of salinity tolerance in Puccinellia tenuiflora [J].Journal of Proteome Research,2011,10(9):3852-3870.
[40]周会萍,王晓冰,徐鑫,周晓君.红叶石楠不同叶龄叶片的光合特性研究[J].西部林业科学,2020,49(1):39-45.ZHOU Huiping,WANG Xiaobin,XU Xin,ZHOU Xiaojun.Photosynthetic characteristics of Photinia fraseri leaves at different ages [J].Journal of West China Forestry Science,2020,49(1):39-45.
[41]林义成,傅庆林,郭彬,刘琛,丁能飞.盐胁迫对红叶石楠花青素指数含量及抗氧化系统的影响[J].浙江农业学报,2018,30(6):970-977.LIN Yicheng,FU Qinglin,GUO Bin,LIU Chen,DING Nengfei.Effects of salt stress on anthocyanin content and activities of antioxidant enzymes in leaves of Photinia frasery[J].Acta Agriculturae Zhejiangensis,2018,30(6):970-977.
[42]欧阳可凡,王文君.芒萁黄酮类物质成分鉴定及体外抗氧化活性研究[J].草原与草坪,2021,41(05):113-118.OUYANG Kefan,WANG Wenjun.Identification of flavonoid components from Dicranopteris pedata and its antioxidant activity in vitro [J].Grassland and Turf,2021,41(05):113-118.
[43]牛欢,韦坤华,徐倩,李明杰,古力,王建明,张重义.不同光照度对金线莲生长、生理特性和药用成分的影响[J].植物资源与环境学报,2020,(1):26-36+43.NIU Huan,WEI Kunhua,XU Qian,LI Mingjie,GU Li,WANG Jianming,ZHANG Zhongyi.Effects of different illuminances on growth,physiological characteristics,and medicinal components of Anoectochilus roxburghii [J].Journal of Plant Resources and Environment,2020,(1):26-36+43.
[44]陈斌,李洪瑶,刘筱玮,夏斌,孙绍文,孙颖,何淼.不同光照强度对新娘草叶片形态建成及超微结构的影响[J].草业学报,2019,28(7):175-185.CHEN Bin,LI Hongyao,LIU Xiaowei,Xia Bin,SUN Shaowen,SUN Ying,HE Miao.Effects of different light intensities on morphogenesis and ultrastructure of Gibasis pellucida leaf [J].Acta Prataculturae Sinica,2019,28(7):175-185.
[45]Agati G,Biricolti S,Guidi L,Ferrini F,Fini A,Tattini M.The biosynthesis of flavonoids is enhanced similarly by UV radiation and root zone salinity in L.vulgare leaves [J].Journal of Plant Physiology,2011,168:204–212.
[46]赵嫚,陈仕勇,李亚萍,周青平,陈有军,常馨丹.外源GABA对盐胁迫下金花菜种子萌发及幼苗抗氧化能力的影响[J].江苏农业学报,2021,37(2):310-316.ZHAO Man,CHEN Shiyong,LI Yaping,ZHOU Qingping,CHEN Youjun,CHANG Xindan.Influence of exogenous γ-aminobutyric acid (GABA) on seed germination and antioxidant protection of Medicago polymorpha under salt stress [J].Jiangsu Journal of Agricultural Sciences,2021,37(2):310-316.
[47]Tuteja N.Mechanisms of high salinity tolerance in plants [J].Methods Enzymol,2007,428:419–438.
[48]Houmani H,Rodríguez-Ruiz M,Palma JM,Abdelly C.,Corpas FJ..Modulation of superoxide dismutase (SOD) isozymes by organ development and high long-term salinity in the halophyte Cakile maritima [J].Protoplasma,2015,253,885–894.
[49]韩志平,张海霞,刘冲,张巽,石福臣.NaCl胁迫对黄花菜生长和生理特性的影响[J].西北植物学报,2018,38(9):1700-1706.HAN Zhiping,ZHANG Haixia,LIU Chong,ZHANG Xun,SHI Fuchen.Growth and physiological characteristics of daylily plants under NaCl stress [J].Acta Botanica Boreali-Occidentalia Sinica,2018,38(9):1700-170
[50]刘文瑜,杨发荣,黄杰,魏玉明,金茜.NaCl胁迫对藜麦幼苗生长和抗氧化酶活性的影响[J].西北植物学报,2017,37(9):1797-1804.LIU Wenyu,YANG Farong,HUANG Jie,WEI Mingyu,JIN Xi.Response of Seedling growth and the activities of antioxidantenzymes of Chenopodium quinoato Salt Stress [J].Acta Botanica Boreali-Occidentalia Sinica,2017,37(9):1797-1804.
[51]李易珺,郭树江,杨自辉.盐、干旱胁迫对沙蒿种子萌发与幼苗生理特性的影响[J].草原与草坪,2023,43(05):113-119.LI Yijun,GUO Shujiang,YANG Zihui.Effect of salt and drought stresses on seed germination and seedling physiological characteristics of Artemisia desertorum[J].Grassland and Turf,2023,43(05):113-119.
[52]丁理成,王尧,李景刚,王庆华,王延玲.盐肤木与泰山盐肤木幼苗对盐胁迫的生理响应[J].植物生理学报,2022,58(7):1335-1345.DING Licheng,WANG Yao,LI Jinggang,WANG Qinghua.Physiological response of Rhus chinensis and R.taisanensis seedlings to salt stress [J].植物生理学报,2022,58(7):1335-1345.
[53]朱娟娟,马海军,张琇,李敏,徐小云,覃洪云.盐胁迫下解钾菌对枸杞幼苗的促生效应[J].应用生态学报,2021,32(4):1289-1297.ZHU Juanjuan,MA Haijun,ZHANG Xiu,LI Min,XU Xiaoyun,QIN Hongyun.Effects of potassium-solubilizing bacteria promoting the growth of Lycium barbarum seedlings under salt stress [J].Chinese Journal of Applied Ecology,2021,32(4):1289-1297.
[54]龙明秀,许岳飞,何学青,廖允成.NaCl胁迫下紫花苜蓿幼苗抗氧化酶活性的研究[J].草地学报,2012,20(1):83-87.LONG Mingxiu,XU Yuefei,HE Xueqing,LIU Yuncheng.Antioxidant enzymes activities of Medicago sativa L.seedling under salt stress [J].Acta Agrestia Sinica,2012,20(1):83-87.
[55]袁祖丽,吴中红.镉胁迫对烟草根抗氧化能力和激素含量的影响[J].生态学报,2010,30(15):4109-4118.YUAN Zuli,WU Zhonghong.Effect of cadmium on antioxidative capability and phytohormone level in tobacco roots [J].Acta Ecologica Sinica,2010,30(15):4109-411
[56]陈沁,刘友良.谷胱甘肽对盐胁迫大麦叶片活性氧清除系统的保护作用[J].作物学报,2000,26(3):365-371.CHEN Qin,LIU Youliang.Effect of Glutathion on active oxygen scavenging system in leaves of barley seedlings under salt stress [J].Acta Agronomica Sinica,2000,26(3):365-371.
[57]冯肖莉,樊寿德,周莲洁,富春,王艳.苗期盐穗木在不同盐浓度处理下的渗调和抗氧化系统[J].干旱区研究,2018,35(5):1118-1128.FENG Xiaoli,FAN Shoude,ZHOU Lianjie,FU Chun,WANG Yan.Osmotic and antioxidant system in halostachys caspica seedlings under salt stress [J].Arid Zone Research,2018,35(5):1118-1128.
文章摘自:吝瑞杰,王转霞,蔡德育,等.盐胁迫对罗布麻生长和抗氧化能力的影响[J/OL].草原与草坪,1-14[2026-04-10].https://link.cnki.net/urlid/62.1156.S.20260304.1629.006.