摘 要:由钟器疫腐霉(Phytopythium vexans)引起的根褐腐病是影响苎麻产量和品质的重要因素。为筛选具有拮抗钟器疫腐霉潜力的生防微生物资源,从苎麻根际土样中分离获得一株拮抗菌株SEC-488,并采用平板对峙培养法对其拮抗性能进行评价,结合显微镜与扫描电镜观察、生防相关功能特性测定、全基因组测序与生物信息学分析,对该菌株的生防潜力进行解析。结果表明,SEC-488在离体条件下能够显著抑制钟器疫腐霉菌落生长,其抑制率为(76.10±0.65)%。显微镜观察显示,SEC-488作用下钟器疫腐霉菌丝形态和超微结构发生明显改变。功能分析表明,SEC-488具有蛋白酶和淀粉酶活性,并具备溶磷、解钾、固氮和产铁载体等生防相关表型。基于形态学、生理生化特性、16SrRNA系统发育分析及全基因组ANI和isDDH比对结果,SEC-488被鉴定为类芽孢杆菌属(Paenibacillus)菌株。全基因组注释结果显示,该菌株基因组中含有310个碳水化合物活性酶相关基因和17个次生代谢生物合成基因簇。该研究结果为苎麻根褐腐病生物防治相关研究提供了试验依据和理论参考。
关键词:苎麻;钟器疫腐霉;类芽孢杆菌;拮抗活性;全基因组分析;生物防治
苎麻(Boehmeria nivea)是我国重要的特色纤维作物,但随着种植规模扩大和连作年限延长,土传病害日趋严重,其中由钟器疫腐霉(Phytopythium vexans)引起的根褐腐病已成为影响苎麻产量和品质的重要因素[1–4]。该病原隶属于卵菌纲、霜霉目、腐霉科、疫腐霉属,寄主范围广、环境适应能力强,在苎麻生产中具有发生隐蔽、防控难度大的特点[5–7]。目前该病害的防治仍以化学药剂为主,长期施用易引发抗药性、农药残留超标,并带来生态环境安全风险,难以满足苎麻产业绿色发展的需求[8]。
生物防治作为一种环境友好且可持续的病害防控策略,在多种植物疫病防治中显示出良好应用前景[9-10]。拮抗微生物可通过竞争营养和生态位、分泌拮抗代谢产物及产生胞外酶等多种机制抑制病原菌生长[11–13]。其中,芽孢杆菌及类芽孢杆菌因环境适应性强、代谢产物类型丰富而被认为是重要的生防微生物资源[14-15]。然而,针对苎麻根褐腐病病原钟器疫腐霉的生防菌筛选及其作用潜力研究仍相对有限。
基于此,本研究以钟器疫腐霉为代表性靶标菌,从苎麻根际土样中分离筛选拮抗微生物,获得一株拮抗活性稳定的类芽孢杆菌菌株SEC-488。通过体外拮抗试验、生防相关功能特性测定及全基因组测序与功能注释,对SEC-488的生防潜力进行系统解析,旨在为苎麻根褐腐病的生物防治提供新的微生物资源和理论依据,同时为其在卵菌类植物病害防控中的进一步研究与应用奠定基础。
1 材料与方法
1.1 菌株与病原菌来源
菌株SEC-488分离自苎麻根际土壤样品,供试病原菌为钟器疫腐霉(P.vexans),均由中国农业科学院南方经济作物研究中心提供。
1.2 供试培养基
LA、LB、PDA和V8培养基的制作参考王荣波等[16];蛋白酶与纤维酶活性检测培养基的制作参考赵文娟等[17];解钾培养基的制作参考褚睿等[18];固氮培养基的制作参考孙瑞波等[19];难溶性无机磷培养基的配制参考杨顺等[20];有机磷培养基和CAS检测培养基购于青岛海博生物技术有限公司。
1.3 主要仪器与试剂
PCR扩增采用2×EasyTaq PCR SuperMix。主要仪器包括生化培养箱(LRH-150型,上海一恒科学仪器有限公司)、恒温振荡培养箱(ZWY-2102C型,上海智城分析仪器制造有限公司)、PCR仪(TP600型,宝生物工程有限公司)、电泳系统(Wide Mini-Sub Cell GT型,伯乐生命医学产品有限公司)及凝胶成像系统(G:BOX F3型,英国Syngene公司)、显微镜(AE2000型,麦克奥迪实业集团有限公司)、扫描电子显微镜(Gemini300型,德国蔡司股份有限公司)等。
1.4 拮抗菌株的分离与初筛
钟器疫腐霉在PDA平板上活化后作为供试病原菌。拮抗菌株从苎麻根际土壤中经梯度稀释涂布于LA平板分离获得。初筛采用平板对峙法,在PDA平板中央接种病原菌,于距菌饼25mm处接种待测菌株,培养后记录抑制效果。
1.5 拮抗菌株的复筛与抑菌评价
制备SEC-488发酵液后采用打孔法进行抑菌评价。以钟器疫腐霉菌饼为中心,在PDA平板四点对称加样,每孔加入40μL发酵液,LB培养基为空白对照。培养至对照组长满平板后测定抑菌带宽度,并计算相对抑菌率。试验重复3次。
I(%)=(Dc-Dt)/(Dc-d0)×100。
试中:I表示相对抑菌率,%;Dc表示对照组病原菌菌落直径,mm;Dt表示处理组病原菌菌落直径,mm;d0表示初始菌饼直径,本研究中为5mm。
1.6 病原菌菌丝形态与超微结构观察
菌株SEC-488的菌落及细胞形态通过光学显微镜和扫描电镜观察(科学指南针公司)。其革兰氏染色及部分生理生化特性鉴定参考《常见细菌系统鉴定手册》和相关试剂说明书。
1.7 SEC-488的促生及生态相关功能特性测定
将菌株SEC-488接种至难溶性无机磷平板,5d后观察其有无透明圈;将菌株接种至解钾培养基上,5d后观察其有无透明圈;蛋白酶与纤维素酶活性检测参考巴翠玉等[21],菌株生物膜的测定参考Sun等[22],根据海博生物说明书进行产铁载体和溶解有机磷能力检测。
1.8 16S rRNA基因扩增、测序与系统发育分析
采用煮沸法提取菌株DNA作为模板,以引物对27F/1492R对菌株SEC-488的16SrRNA基因进行PCR扩增,16S rRNA基因扩增所用引物为27F(5′-AGAGTTTGATCCTGGCTCAG-3′)和1492R(5′-TACGGCTACCTTGTTACGACTT-3′),PCR反应体系及条件参考黄慧婧等[23]。PCR产物送至湖南擎科生物技术有限公司进行测序,测序结果在NCBI中比对,并采用MEGA7.0软件构建系统发育树(Neighbor-joining法,Bootstrap=1000)。
1.9 全基因组测序、组装与功能注释
提取菌株SEC-488的基因组DNA并完成质量检测后,采用长、短读长联合测序并经质量控制,利用Unicycler进行混合组装,获得完整闭环基因组。编码序列(CDS)通过GeneMarkS预测,tRNA和rRNA分别采用tRNAscan-SE和rRNAmmer鉴定,重复序列分析采用RepeatMasker和Tandem Repeats Finder(TRF)。基因功能注释基于BLAST比对完成,所用数据库包括NR(NRB_DB 202105、NRF_DB 202105)、Swiss-Prot(20210616)、GO(GO_CLASS 20210319)、KEGG(20181107)和COG(20200910)。
1.10 基于全基因组的系统发育与相似性分析
基于菌株SEC-488的完整基因组序列,选取近缘参考菌株进行比较分析,计算平均核苷酸相似性(ANI)和数字化DNA–DNA杂交值(isDDH,GGDC在线平台),并结合ANI≥96%和isDDH≥70%的物种划分阈值,对其分类地位进行判定。
1.11 CAZymes注释与次生代谢生物合成基因簇预测
基于CAZy(Carbohydrate-Active enZYmes)数据库(20210729),对菌株SEC-488基因组中的碳水化合物活性酶(CAZymes)进行注释与分类分析。分析糖苷水解酶(GHs)、糖基转移酶(GTs)、多糖裂解酶(PLs)、碳水化合物酯酶(CEs)及碳水化合物结合模块(CBMs)的组成特征。同时,利用antiSMASH v5.1预测次生代谢生物合成基因簇,并分析其类型和数量。
2 结果
2.1 SEC-488的分离、筛选及拮抗活性评价
2.1.1 拮抗菌株的分离与筛选
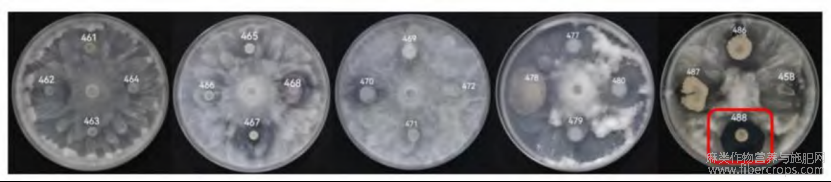
以钟器疫腐霉为指示病原,从土样中分离获得多株细菌菌株。经平板对峙培养法初筛与复筛,筛选到一株对钟器疫腐霉表现出稳定抑制作用的菌株,编号为SEC-488,其在重复试验中均形成清晰的抑制区域(图1),平板抑制率达到(76.10±0.65)%。
图1 拮抗细菌初筛结果
2.1.2 SEC-488对钟器疫腐霉的拮抗作用
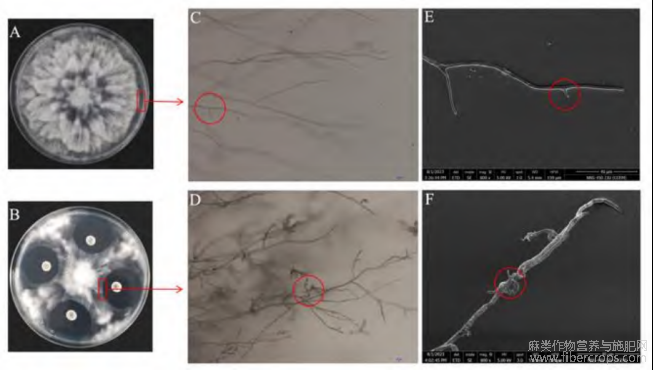
平板对峙培养结果显示,SEC-488可显著抑制钟器疫腐霉菌落的径向生长,并在两者交界处形成清晰抑制带(图2A、B)。光学显微观察表明,经SEC-488处理后,钟器疫腐霉菌丝出现弯曲、缠结及局部膨大等形态异常(图2C、D)。扫描电镜进一步显示,处理组菌丝表面产生褶皱并伴随局部塌陷,而对照组菌丝结构完整、表面光滑(图2E、F)。
图2 SEC-488对钟器疫腐霉的抑制作用
2.2 SEC-488的生防相关功能特性与分类鉴定
2.2.1 SEC-488的促生及生态相关功能特性
功能特性分析结果显示,SEC-488在蛋白酶和纤维素酶检测培养基上形成明显透明圈,表明其具有胞外酶分泌能力(图3A、B)。在养分转化方面,SEC-488表现出溶解有机磷、无机磷和无机钾的能力(图3C~E),并在固氮和铁载体检测培养基上呈阳性反应(图3F、G)。上述结果表明,SEC-488具备多种与植物生长促进及根际生态适应相关的功能表型特征。
注:A表示蛋白酶活性;B表示纤维素酶活性;C表示有机磷溶磷能力;D表示无机磷解磷能力;E表示解钾能力;F表示固氮能力;G表示铁载体产生能力。
图3 SEC-488的促生特性
2.2.2 SEC-488的形态学特征
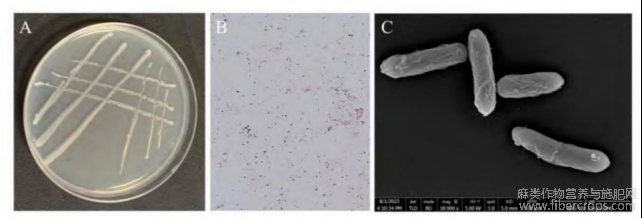
在LB培养基上培养24h后,SEC-488形成乳白色菌落,表面光滑,边缘整齐(图4A)。
革兰氏染色结果显示菌体呈紫色,为革兰氏阳性菌(图4B)。扫描电镜观察表明,SEC-488菌体呈短杆状,细胞大小相对均一,细胞表面结构完整、平整,未见明显变形或附着结构(图4C)。上述形态学特征为其分类鉴定提供了直观依据。
注:A为菌体在LB培养基上的菌落形态;B为菌体的革兰氏染色;C为菌体形态的扫描电镜图像。
图4 SEC-488菌株形态图
2.2.3 SEC-488的生理生化特性
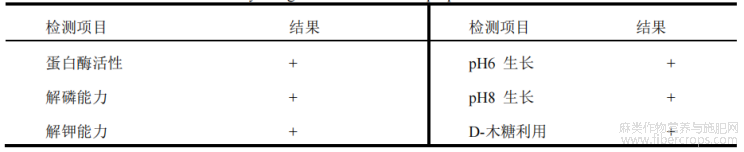
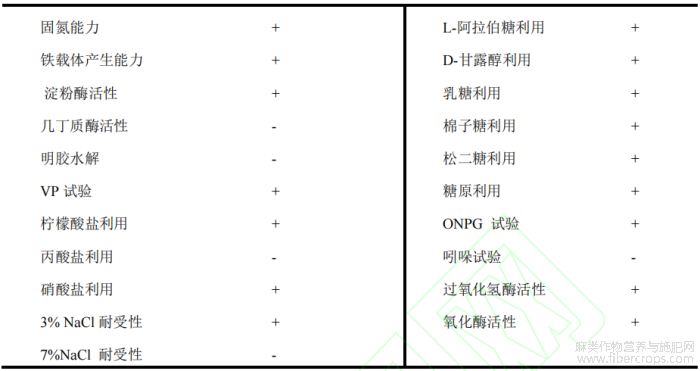
对SEC-488的生理生化特性进行分析,结果见表1。SEC-488具有蛋白酶和淀粉酶活性,并表现出溶磷、解钾、固氮和产铁载体等功能特征。同时,该菌株能够利用多种碳源,包括D-xylose、L-arabinose、D-mannitol、乳糖、棉子糖、海藻糖和糖原等。在环境适应性方面,SEC-488可在pH6~8条件下正常生长,在3%NaCl条件下仍能生长,但在7%NaCl条件下生长受限。部分水解反应如几丁质酶活性和明胶水解反应为阴性。整体来看,SEC-488的生理生化特性与Paenibacillus属已报道菌株的特征相一致。
表1 SEC-488的生理生化特性
注:“+”表示阳性,“-”表示阴性。
2.2.4 16S rRNA基因系统发育分析
基于16S rRNA基因序列构建系统发育树,对SEC-488的系统发育地位进行分析。结果显示,SEC-488与类芽孢杆菌属(Paenibacillus)多个已报道菌株聚为同一分支,并与巴西类芽孢杆菌(P.brasiliensis)、皮奥里亚类芽孢杆菌(P.peoriae)等菌株具有较近的系统发育关系。系统发育分析结果表明,SEC-488在分子系统发育层面隶属于类芽孢杆菌属,与其形态学特征及生理生化分析结果相互印证(图5)。
注:采用最大似然法(Maximum Likelihood)构建系统发育树,Bootstrap重复次数为1000,仅显示大于50%的Bootstrap支持值。比例尺表示序列进化距离。
图5 基于16S rRNA基因序列的菌株SEC-488系统发育树
2.3 SEC-488的全基因组特性分析
2.3.1 基因组测序与基本特征
对菌株SEC-488进行全基因组测序与组装分析,结果显示其基因组由一条环状染色体构成,基因组总长度为5919491bp(表2)。基因组GC含量为45.74%,编码区占基因组总长度的86.72%。
表2 基因组组装结果统计
基因组注释结果显示,SEC-488共预测到5475个蛋白编码基因,平均长度为938bp,并包含108个tRNA、39个rRNA和4个sRNA。基因组中还鉴定到6个基因岛、16个前噬菌体区域及3个CRISPR结构。
2.3.2 SEC-488的基因组结构特征
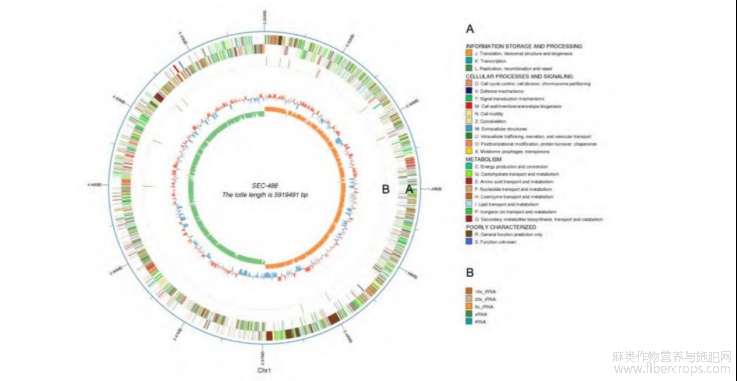
SEC-488的全基因组结构以环形图形式展示(图6)。由外至内依次显示染色体位置刻度、正负链编码基因分布、COG功能分类注释结果以及非编码RNA的分布情况。最内侧圆环分别表示GC含量和GC skew的变化趋势。
从整体结构来看,SEC-488编码基因在染色体上的分布较为均匀,未观察到明显的基因缺失或高度集中区域。GC含量在全基因组范围内呈现相对稳定的波动特征,GC skew 的变化在染色体不同区域呈现正负交替分布。菌株SEC-488的完整基因组序列已提交至美国国家生物技术信息中心(National Center for Biotechnology Information,NCBI)GenBank数据库,登录号为CP137146(BioProject:PRJNA1031329;BioSample:SAMN37933682)。
注:最外圈表示基因组位置,单位为Mb。第二圈和第三圈分别表示位于正链(+)和负链(−)上的编码基因。A表示COG功能注释结果,B表示非编码RNA(ncRNA)。最内侧的两圈分别表示GC含量和GC偏移(GC skew)值,其中橙色表示正值,绿色表示负值。
图6 SEC-488完整基因组的环状染色体图
2.3.3 基于全基因组的系统亲缘关系分析
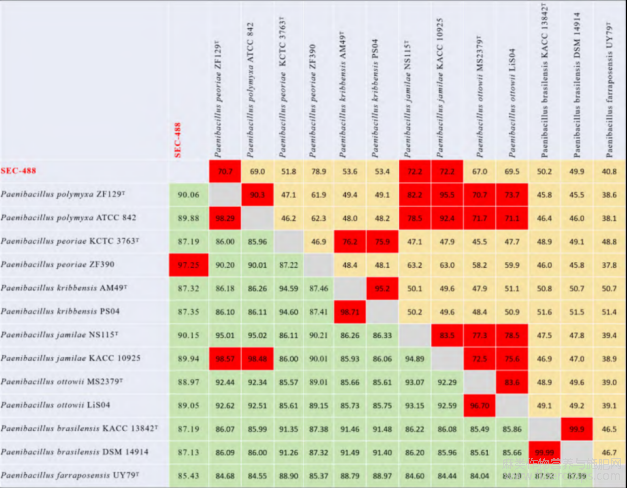
为进一步明确SEC-488在Paenibacillus属中的系统发育地位,基于全基因组序列对其与相关参考菌株之间的平均核苷酸相似性(ANI)和数字化DNA-DNA杂交值(isDDH)进行了比较分析(图7)。
分析结果显示,SEC-488与所选Paenibacillus参考菌株之间的ANI值均低于96%,isDDH值均低于70%。上述结果表明,SEC-488在全基因组水平上与已报道的Paenibacillus物种存在明显差异。
注:T表示在NCBI中注释的参考基因组。上三角(黄色区域)表示isDDH值(%),下三角(绿色区域)表示ANI值(%)。当isDDH≥70%或ANI≥96%时,对应网格以红色标示。
图7基于全基因组序列的各菌株的平均核苷酸一致性(ANI)值和isDDH值
2.4 SEC-488的生防相关遗传潜力解析
2.4.1 碳水化合物活性酶(CAZymes)功能注释分析
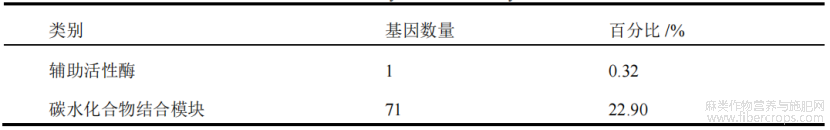
为从基因组层面解析SEC-488的作用特征,对其全基因组序列进行碳水化合物活性酶(carbohydrate-active enzymes,CAZymes)注释分析,结果见表3。共预测到多种CAZymes相关基因,涵盖糖苷水解酶(glycoside hydrolases,GH)、糖基转移酶(glycosyl transferases,GT)、碳水化合物结合模块(carbohydrate-binding modules,CBM)、碳水化合物酯酶(carbohydrate esterases,CE)及多糖裂解酶(polysaccharide lyases,PL)等类别。
表3 碳水化合物活性酶
其中,GH类基因数量最多,占CAZymes总数的47.10%,其次为CBM(22.90%)和GT(17.42%)。此外,还预测到一定数量的CE(8.71%)和PL(3.55%)相关基因。上述结果表明,SEC-488具有较为丰富的碳水化合物代谢酶系。GH、CE和PL参与复杂多糖降解,而真菌及卵菌细胞壁以多糖为主要成分;CBM的富集则有助于提高多糖底物识别与结合效率,从而增强SEC-488在根际环境中的竞争与定殖优势,为其生防功能提供遗传支撑。
2.4.2 SEC-488次级代谢产物生物合成基因簇分析
基于antiSMASH对SEC-488全基因组的分析,共预测获得17个次级代谢产物生物合成基因簇(biosynthetic gene clusters,BGCs)(表4)。涵盖非核糖体肽合成酶(NRPS)及其衍生类型、NRPS–聚酮合酶(PKS)杂合型、核糖体合成并经翻译后修饰肽(RiPPs)、铁载体、膦酸类化合物及环状内酯类自诱导物等多种类型。多条BGC与已知抗菌或抗真菌代谢物生物合成通路高度相似(80%~100%)。其中,鉴定到与抗真菌和抗卵菌活性相关的fusaricidin B类脂肽生物合成基因簇(100%),鉴定到与靶向细菌细胞膜抗菌活性相关的tridecaptin和polymyxin/colistin类非核糖体肽合成酶(NRPS)基因簇(100%),同时鉴定到与近缘菌生态竞争相关的paenilan-like兰硫肽类核糖体合成并经翻译后修饰肽(RiPP)基因簇(100%)。
此外,鉴定到与抗菌脂肽paenilipoheptin生物合成相关的NRPS–PKS杂合型基因簇,以及与铁资源竞争相关的desferrioxamine E类铁载体生物合成基因簇,提示其可能通过抗菌代谢物分泌和铁限制机制参与根际生态位构建。
综上,SEC-488携带多种与抗真菌、抗细菌及资源竞争相关的次级代谢基因簇,为其生防功能提供了重要遗传基础。
表4 SEC-488基因组中经antiSMASH预测的次级代谢产物生物合成基因簇
3 讨论
土传病害是制约苎麻持续生产的重要因素,其中由钟器疫腐霉引起的根褐腐病因防控难度大而长期依赖化学药剂。随着抗药性风险和生态环境压力的增加,筛选拮抗微生物并开展生物防治研究已成为该病害防控的重要方向。已有研究[24]表明,从自然环境中分离拮抗菌株,并结合表型与基因组层面解析其作用特点,是生防菌研究的有效途径。芽孢杆菌及类芽孢杆菌因其代谢产物类型丰富、环境适应能力强而被广泛关注。Ongena等[25]系统总结了芽孢杆菌脂肽类和多肽类次生代谢物在抑制植物病原菌中的作用;Chen等[26]报道Paenibacillus polymyxa可通过产生抗菌物质和竞争营养位点抑制多种土传病原菌;国内研究亦表明,芽孢杆菌在疫霉菌类病害防治中具有良好潜力[27]。
本研究系统评估了类芽孢杆菌菌株SEC-488对苎麻根褐腐病病原钟器疫腐霉的拮抗作用及其遗传基础。结果表明,SEC-488在体外条件下能够稳定抑制钟器疫腐霉的生长。显微镜及扫描电镜观察显示,在SEC-488作用下,病原菌菌丝出现弯曲、膨大及表面塌陷等结构异常,提示其拮抗作用可能与病原菌细胞结构受损相关[28-29]。该结果与既往关于类芽孢杆菌具有理想拮抗能力的研究结论一致[16,30–32]。
基因组分析显示,SEC-488具有结构完整且功能容量较高的基因组特征,其功能注释涉及物质代谢、细胞壁相关过程及次级代谢等多个类别。SEC-488基因组中富集的碳水化合物活性酶,尤其是糖苷水解酶类,提示其具备较强的复杂多糖降解潜力。已有研究[33-34]表明,糖苷水解酶可通过裂解纤维素、半纤维素及β-葡聚糖等细胞壁结构多糖,从而破坏病原菌细胞壁完整性并抑制其生长与侵染过程。此外,Paenibacillus属菌种普遍富集多种CAZymes,表现出显著的多糖降解能力[35]。碳水化合物结合模块(CBMs)可增强酶对多糖底物的识别与结合效率,而糖基转移酶相关基因则与细胞壁结构调控及环境适应密切相关,可能进一步促进微生物在根际环境中的定殖与生态竞争能力[36-37]。
除酶促作用外,SEC-488基因组中还预测到多条与已知抗菌或抗真菌化合物相似的次级代谢产物生物合成基因簇,包括脂肽类和铁载体相关通路。值得注意的是,检测到一条与desferrioxamineE生物合成通路具有一定相似性的铁载体(siderophore)基因簇,表明SEC-488可能具备合成羟肟酸类铁载体并螯合环境中Fe3?的潜在能力[38]。铁竞争被认为是根际生态系统中生防菌发挥作用的重要机制之一,通过分泌高亲和力铁载体,生防菌可优先获取有限的铁资源,从而限制病原菌的生长与定殖[39]。结合本研究中鉴定到的类铁载体生物合成基因簇以及多种抗菌脂肽相关基因簇,表明SEC-488可能通过“直接拮抗+资源竞争”协同机制参与钟器疫腐霉的抑制及根际生态位构建[40-41]。
综上所述,SEC-488对苎麻根褐腐病病原钟器疫腐霉表现出稳定的拮抗表型,其生防潜力可能来源于酶促作用与次级代谢途径的协同。本研究从表型和基因组层面对该菌株的生物防治潜力进行了系统分析,为其在苎麻根褐腐病生物防治中的进一步研究与应用提供了基础,后续仍需在根际或盆栽体系中验证其定殖行为及关键拮抗因子的具体作用。
4 结论
本研究从苎麻土壤中筛选获得一株对苎麻根褐腐病病原钟器疫腐霉具有稳定拮抗活性的类芽孢杆菌菌株SEC-488。结合表型特征、功能特性及全基因组分析结果,SEC-488表现出与生物防治相关的多种功能基础,其拮抗潜力在基因组层面得到支撑。该研究为苎麻根褐腐病生防菌资源的挖掘提供了新的候选菌株,并为后续在根际或盆栽体系中进一步解析其作用机制与应用潜力奠定了基础。
参考文献:
[1]Corbita V,Seco M N,Galvez L,et al.A review on ramie(Boehmeria niveaL.gaudich.):from textile to medicine and the threats of pests and diseases[J].OnLine Journal of Biological Sciences,2025,25(4):873-891.
[2]陈晓霞,于红豆,李梦玮,等.基于文献计量分析的根腐病研究现状及趋势[J].应用与环境生物学报,2024,30(3):623-632.
[3]Yu Y T,Chen J,Gao C S,et al.First report of brown root rot caused by Pythium vexans on ramie in Hunan,China[J].Canadian Journal of Plant Pathology,2016,38(3):405-410.
[4]Yu Y T,Gao C S,Wang T H,et al.Genome sequence resource for the ramie oomycete pathogen Phytopythium vexans HF1[J].Molecular Plant-Microbe Interactions®,2020,33(11):1270-1273.
[5]Rujirawat T,Patumcharoenpol P,Lohnoo T,et al.Probing the phylogenomics and putative pathogenicity genes of Pythium insidiosum by oomycete genome analyses[J].Scientific Reports,2018,8:4135.
[6]边传红,王伟杰,赵世民,等.烟草钟器腐霉的分子鉴定与致病力测定[J].农学学报,2015,5(1):32-36.
[7]苗圃,王海涛,李淑君,等.两种病原真菌在河南危害烟草的首次报道[J].中国烟草科学,2014,35(2):113-116.
[8]陈奕坤.苎麻根褐腐病菌致病力、抗药性及遗传多样性研究[D].北京:中国农业科学院,2020.
[9]Ayaz M,Li C H,Ali Q,et al.Bacterial and fungal biocontrol agents for plant disease protection:journey from lab to field,current status,challenges,and global perspectives[J].Molecules,2023,28(18):6735.
[10]Barka E A,Jeandet P,Lahlali R.The hidden world within plants 2.0[J].Microorganisms,2023,11(12):2903.
[11]陈嘉敏,管维轩,朱洁倩,等.植物病害生防菌株的研究进展[J].微生物前沿,2017,6(2):35-43.
[12]Zou L,Wang Q,Wu R X,et al.Biocontrol and plant growth promotion potential of endophytic Bacillus subtilis JY-7-2L on Aconitum carmichaelii Debx[J].Frontiers in Microbiology,2023,13:1059549.
[13]Legrifi I,Al Figuigui J,El Hamss H,et al.Potential for biological control of Pythium schmitthenneri root rot disease of olive trees(Olea europaea L.)by antagonistic bacteria[J].Microorganisms,2022,10(8):1635.
[14]Kang J A,Lee Y H.Biocontrol of bacterial seedling rot in rice plants using Bacillus velezensis JBCS608 and its formulated products[J].The Plant Pathology Journal,2025,41(6):790-799.
[15]Wang T H,Li W T,Wang F,et al.Biocontrol potential of Bacillus velezensis SEC-024A against southern blight of industrial hemp[J].Industrial Crops and Products,2024,222:119767.
[16]王荣波,陈姝樽,肖小露,等.枯草芽胞杆菌BS193对辣椒疫霉的拮抗作用及其相关生防因子检测[J].农业生物技术学报,2022,30(4):772-782.
[17]赵文娟,付博,徐升运,等.生防菌SF1103、SF1104对黄瓜枯萎病菌的拮抗作用[J].西北农业学报,2017,26(10):1537-1543.
[18]褚睿,李昭轩,张学青,等.黄瓜枯萎病拮抗芽孢杆菌的筛选、鉴定及其生防潜力[J].生物技术通报,2023,39(8):262-271.
[19]孙瑞波,章凤玲,宗静雯,等.微生物在盐碱地改良中的作用研究进展[J].广东农业科学,2025,52(2):14-30.
[20]杨顺,杨婷,林斌,等.两株溶磷真菌的筛选、鉴定及溶磷效果的评价[J].微生物学报,2018,58(2):264-273.
[21]巴翠玉,张林波,张培军,等.2株枯草芽孢杆菌的分离鉴定及特性研究[J].华南农业大学学报,2017,38(3):46-51.
[22]Sun D L,Zhuo T,Hu X,et al.Identification of a Pseudomonas putida as biocontrol agent for tomato bacterial wilt disease[J].Biological Control,2017,114:45-50.
[23]黄慧婧,高香辉,陈舒,等.一株番茄青枯病菌拮抗细菌的筛选、发酵条件优化及田间小区防效[J].微生物学通报,2022,49(2):606-619.
[24]卯婷婷,陶刚,赵兴丽,等.4种微生物菌剂对辣椒主要病害的生物防治作用[J].中国生物防治学报,2020,36(2):258-264.
[25]Ongena M,Jacques P.Bacillus lipopeptides:versatile weapons for plant disease biocontrol[J].Trends in Microbiology,2008,16(3):115-125.
[26]Chen X H,Scholz R,Borriss M,et al.Difficidin and bacilysin produced by plant-associated Bacillus amyloliquefaciens are efficient in controlling fire blight disease[J].Journal of Biotechnology,2009,140(1/2):38-44.
[27]皮娜娜,王玺茜,罗建军,等.贝莱斯芽孢杆菌防控植物病害的研究进展[J].广东农业科学,2024,51(6):48-59.
[28]刘雪娇,李红亚,李术娜,等.贝莱斯芽孢杆菌3A3-15生防和促生机制[J].河北大学学报(自然科学版),2019,39(3):302-310.
[29]马佳,李颖,胡栋,等.芽胞杆菌生物防治作用机理与应用研究进展[J].中国生物防治学报,2018,34(4):639-648.
[30]施春兰,朱国渊,秦得强,等.附子白绢病拮抗细菌CZ1的分离鉴定、发酵条件优化及防效测定[J].微生物学通报,2023,50(10):4485-4498.
[31]Jia S,Song C,Dong H,et al.Evaluation of efficacy and mechanism of Bacillus velezensis CB13 for controlling peanut stem rot caused by Sclerotium rolfsii[J].Frontiers in Microbiology,2023,14:1111965.
[32]穆晓清,鲁耀雄,戴良英,等.贝莱斯芽胞杆菌YFB3-1对辣椒疫霉的抑菌效果及其抑菌物质[J].农业生物技术学报,2024,32(4):859-872.
[33]Kubicek C P,Starr T L,Glass N L.Plant cell wall–degrading enzymes and their secretion in plant-pathogenic fungi[J].Annual Review of Phytopathology,2014,52:427-451.
[34]Peng F F,Li X L,Wei Z X,et al.Biocontrol potential and comparative genomic analysis of two Bacillus velezensis strains against sclerotinosis in mulberry fruit[J].Frontiers in Microbiology,2025,16:1587301.
[35]Mukherjee S,Lodha T D,Madhuprakash J.Comprehensive genome analysis of cellulose and xylan-active CAZymes from the Genus Paenibacillus:special emphasis on the novel Xylanolytic Paenibacillusp.LS1[J].Microbiology Spectrum,2023,11(3):e05028-e05022.
[36]Alshareef S A.Metabolic analysis of the CAZy class glycosyltransferases in rhizospheric soil fungiome of the plant species Moringa oleifera[J].Saudi Journal of Biological Sciences,2024,31(4):103956.
[37]Feng L Y,Liu X,Wang N,et al.Genomic analysis of cadmium-resistant and plant growth-promoting Burkholderia alba isolated from plant rhizosphere[J].Agronomy,2025,15(8):1780.
[38]Barona-Gómez F,Wong U,Giannakopulos A E,et al.Identification of a cluster of genes that directs desferrioxamine biosynthesis in Streptomyces coelicolor M145[J].Journal of the American Chemical Society,2004,126(50):16282-16283.
[39]Gu S H,Wei Z,Shao Z Y,et al.Competition for iron drives phytopathogen control by natural rhizosphere microbiomes[J].Nature Microbiology,2020,5(8):1002-1010.
[40]Chen Y,Chai Y R,Guo J H,et al.Evidence for cyclic di-GMP-mediated signaling in Bacillus subtilis[J].Journal of Bacteriology,2012,194(18):5080-5090.
[41]Yu X M,Ai C X,Xin L,et al.The siderophore-producing bacterium,Bacillus subtilis CAS15,has a biocontrol effect on Fusarium wilt and promotes the growth of pepper[J].European Journal of Soil Biology,2011,47(2):138-145.
文章摘自:邢濮厚,秦菁菁,冯佳,王芳,宋志强,刘华,颜健红,王吐虹,程毅.一株拮抗钟器疫腐霉的类芽孢杆菌 SEC-488 的筛选、鉴定与全基因组分析[J/OL].中国麻业科学.https://link.cnki.net/urlid/43.1467.S.20260331.0936.002