摘要:目的针对大麻Cannabis sativa早期性别鉴定困难及现有分子标记稳定性不足的问题,基于大麻性染色体结构特征,开发稳定、准确的大麻早期性别鉴定分子标记,为生产中的幼苗期性别鉴定提供可靠技术手段。方法综合利用多份染色体级别大麻单倍型基因组数据,通过生物信息学方法系统比对筛选Y染色体特异区段(MSY)中的雄性特异片段;从大片段MSY区域设计特异性分子标记,以36份已知性别大麻样品(包括15份雄株和21份雌株)为材料,通过PCR扩增及琼脂糖凝胶电泳,对分子标记进行特异性与稳定性验证,并与已报道标记(MADC5、MADC6)进行对比分析。结果共筛选获得15 648个Y染色体的特异区段,从中开发出12个SCAR标记。经验证,其中5个标记(MSY99M-3、MSY99M-4、MSY99M-5、MSY100M-1、MSY100M-7)在雄株中均能稳定扩增出清晰特异性条带,而在所有雌株中均无扩增,鉴定准确率达100%,优于部分已报道标记。结论基于Y染色体特异区段开发的SCAR标记具有高度特异性和稳定性,可用于大麻早期性别的快速、精准鉴定,对提高药用大麻相关产品的生产效率具有重要的应用价值。
关键词:大麻;雌雄鉴定;分子标记;Y染色体;SCAR标记
大麻Cannabis sativa L.是一种具有悠久驯化历史的雌雄异株作物,其雌性植株具有更高的经济价值。在药用方面,传统中药火麻仁来源于雌性植株的成熟果实,大麻中的重要活性成分大麻二酚(cannabidiol,CBD)则主要在未授粉的雌性花序中富集[1-2]。大麻因其药用价值在全球范围内已被栽培和利用数千年[3]。在中国,大麻的根、叶、花和种子均可入药,其干燥成熟果实火麻仁具有润肠通便的功效,用于血虚津亏、肠燥便秘等症[4]。除传统中药应用外,活性成分CBD也因其在阿尔茨海默病、癫痫和精神分裂症等疾病治疗中的潜在疗效而成为当前研究的热点[5]。以CBD为单一成分的药物Epidiolex已先后获得美国食品药品管理局、欧盟委员会及英国国家医疗服务体系等批准,用于治疗Lenox-gastuat或Dravet综合征等儿童先天性罕见癫痫[6]。
在实际生产中,大麻作为火麻仁和CBD的植物来源分别以果实和未授粉的雌花为主要采收目标,因此合理调控雌雄比例对提高产值至关重要。由于大麻为风媒植物,花粉扩散能力强,在以CBD提取为目的的栽培中,即使少量雄株也会导致大面积雌株授粉,使花序缩小,CBD产量下降可高达60%[7],造成严重经济损失。因此,大麻幼苗期的性别鉴定具有重要意义。然而,大麻在早期生长阶段性别二型性不明显[8],通常需在开花期才能通过形态特征准确判别,限制了形态学鉴定在早期生产管理的应用。
随着分子生物学、遗传学、生物信息学的发展,分子标记为大麻幼苗期性别鉴定提供了新的途径。目前,常用于植物性别鉴定的分子标记主要包括随机扩增多态性DNA(random amplified polymorphic of DNA,RAPD)、扩增片段长度多态性(amplified fragment length polymorphism,AFLP)、特定序列扩增区域(sequence characterized amplified regions,SCAR)、简单序列重复(simple sequence repeats,SSR)和单核苷酸多态性(single nucleotide polymorphism,SNP)等[9],并已广泛运用于沙棘[10]、银杏[11]、细叶菖蒲[12]、啤酒花[13]、番木瓜[14]等雌雄异株植物。与形态学或化学方法相比,分子标记数量丰富、准确性高,且不受植物生长发育阶段和组织部位影响,检测操作简便快捷,尤其适用于幼苗期性别鉴定。在大麻研究中,已有多个雄性连锁分子标记(如MADC1~MADC6)被开发[15-18],并据此构建了具有较高稳定性和可重复性的SCAR标记[8,15-16,18],此外,赵铭森等[19]通过对已有标记MADC2等的引物再开发,获得的MADC2-8标记在籽用大麻中鉴定准确率达98.34%;孙玉婷等[20]和孙哲等[21]先后证明了OPV-08和SCAR1可在种子和幼苗期精确区分雌雄株。然而这些标记最初基于RAPD和AFLP等随机扩增技术开发,其筛选过程仍需较大工作量、且在特异性与稳定性方面存在一定局限。近年来,随着分子生物学技术的发展,更为稳定、高效的性别分子鉴定策略逐渐建立。例如,陶杰等[22]基于全基因组信息构建的InDel标记Is-02和Is-08在多种质中验证准确率高达100%。这些进展推动了大麻早期性别鉴定分子标记开发由随机策略向高特异性策略的转变,为性别鉴定研究和农业生产提供了有力支持。此外,还有一些雌性特异的分子标记被挖掘[23],但鉴于大麻X/Y型性别决定系统的特性及缺少足够的验证实验,这些标记可能不具有普适性。
大麻的性别主要由X/Y型性染色体系统控制。性染色体通常由1个或2个在减数分裂期仍能配对重组的假常染色体区(pseudoautosomal region,PAR)和一个非配对的性别决定区(Sexdetermining region,SDR)构成[24]。其中,SDR包括雄性特有的Y染色体区域(male-specific of Y,MSY)和X染色体特异区域(X specific region,XSR)[25]。从序列角度观察,PAR区域序列高度同源,而MSY由于重组抑制,与对应的XSR独立进化并逐渐累积序列分歧[26]。近年来,随着大麻基因组组装数量与质量的不断提高[27-29],诸多不同品种的雌、雄株单倍型基因组及性染色体序列相继组装成功并发布[30],为鉴定性别决定区及开发基于MSY区域的雄性特异分子标记提供了坚实基础。本研究基于性染色体结构特征,利用生物信息学方法挖掘基因组中MSY区域序列,以筛选雄性特异片段,为大麻性别鉴定分子标记的开发提供新的思路。
1仪器与材料
1.1仪器
Tissue/Grinder 2020高通量组织研磨机(科瑞恩特(北京)科技有限公司);HB120-S LED数显加热金属浴(大龙兴创实验仪器(北京)股份公司);X1个人型迷你离心机(基因有限公司);OSE-260-03 TGem Pro分光光度计(天根生化科技(北京)有限公司);T20型双槽梯度PCR仪(杭州朗基科学仪器有限公司);DYY-6D型电泳仪(北京市六一仪器厂);GenoSens 2150凝胶成像系统(上海勤翔科学仪器有限公司)。
1.2材料
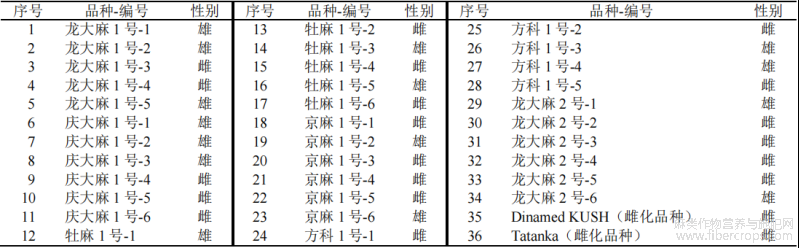
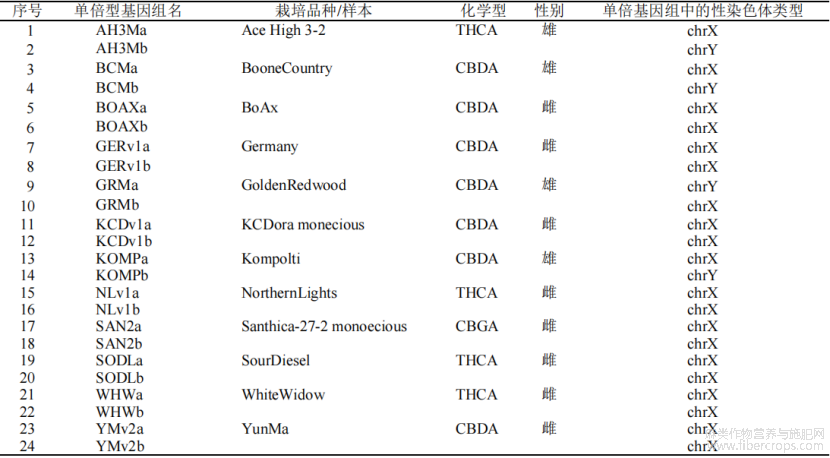
庆大麻1号、牡麻1号、京麻1号等8个大麻品种的种子用于大麻的栽培和表型观察,样品的详细信息见表1,测试样品由中国中医科学院中药研究所孙伟研究员鉴定为大麻C.sativa L.。大麻样品播种后于4~5周龄(约7~9片真叶时)采集部分大麻叶片立刻在硅胶中干燥保存,用于总DNA提取实验和分子标记筛选与验证,样品继续栽培至观察花序表型后,记录样本性别,并采收植株在硅胶中干燥保存。基因组数据来源于Lynch等[30]发布的4份雄性和8份雌性的24个染色体级别单倍型基因组序列(https://resources.michael.salk.edu/root/tools.html?tool=%2Fresources%2Fcannabis_gen omes%2Findex.html),基因组详细信息见表2。绿色荧光核酸染料(北京索莱宝科技有限公司);DC104-01 FastPure Plant DNA Isolation Mini Kit、2×Rapid Taq Master Mix、DL2000 Plus DNA Marker(南京诺唯赞生物科技股份有限公司);TSINGKE TSJ001高纯度低电渗琼脂糖(北京擎科生物科技股份有限公司)。
表1 大麻样品信息
表2 不同品种大麻的参考基因组详细信息
2方法
2.1性染色体比对与特异区段筛选
采用winnowmap v2.03对表2中基因组序列进行相互比对,利用bedtools v2.26.0对比对区间进行处理,包括取并集(merge)、交集(intersect)和补集(complement)操作,并通过getfasta提取相应序列。首先,将BCMb基因组中的Y染色体序列比对至性染色体X型的BCMa单倍型基因组,获得未能比对的候选Y染色体特异区段(数据集1)。随后,将数据集1与其余19份基因组(表2序号:1、5~8、10~13、15~24)中的X染色体序列进行分别比对,取并集后再与数据集1取补集,以过滤掉数据集1中可以比对到含X染色体大麻基因组的序列片段,得到进一步过滤后的Y染色体特异区段(数据集2)。同时将数据集1分别与其余3份基因组(表2序号:2、9、14)中的Y染色体进行比对,取交集,以筛选出不同品种共有的Y染色体特异区段(数据集3)。将数据集2与数据集3取交集,获得最终的Y染色体特异序列(数据集4)。
2.2雄性特异分子标记的设计
对数据集4进行长度排序,选择较长区段作为标记开发候选区域。利用Primer-Blast(https://www.ncbi.nlm.nih.gov/tools/primer-blast)设计特异性引物(扩增片段大小为200~600bp),并由北京六合华大基因科技有限公司合成。随后,采用BLAST v2.10.1的blastn-short模式,将设计的引物比对至雌、雄性单倍型基因组,以验证其在Y染色体上的特异性和一致性。
2.3基因组DNA的提取
取样品适量,使用75%乙醇擦拭表面,吸干表面水分,取约20mg,置1.5mL离心管中,使用高通量组织研磨机研细,采用植物基因组DNA提取试剂盒,参照说明书项下操作提取样品总DNA。采用微量分光光度计检测提取DNA浓度及纯度。
2.4分子标记的筛选与验证
挑选雌、雄植株各3株(表1中的序号2、27、29、33、11和36号样品)作为初筛材料,利用设计的12对引物进行PCR扩增。PCR反应体系为2×Rapid Taq Master Mix 13μL,正向引物1μL,反向引物1μL,ddH2O 9μL,基因组DNA 1μL。PCR反应条件95℃、4min;95℃、30s,55℃、30s,72℃、10s,35循环;72℃、10min。
同时设置ITS2和已报道的雄性特异标记MADC5、MADC6作为阳性对照(SCAR119F/R的退火温度为52℃,其他反应条件不变),空模板作为阴性对照。引物序列见表3。扩增产物经琼脂糖凝胶电泳检测,并通过凝胶成像系统记录结果,筛选出具有良好特异性的候选引物。进一步选取36份已鉴定性别的样本(15雄、21雌)进行扩展验证,PCR反应体系和扩增程序同上,以评估标记的有效性和稳定性。
表3 引物序列
3结果与分析
3.1 Y染色体特异性序列的鉴定
比对分析结果显示,候选Y染色体特异区段(数据集1)共计16120个,平均长度约1003bp。经19份X染色体序列过滤后,获得的数据集2包含29438个区段,平均长度约180bp。经与其他3份Y染色体取交集得到的数据集3包含13496个区段,平均长度约1095bp。最终,结合数据集2与数据集3,筛选出15648条Y染色体特异序列(数据集4),平均长度约275bp,所有区段均分布于BCMb基因组中Y染色体的28.6~107.8Mb,与Lynch等[30]报道的Y染色体SDR区域一致。
3.2雄性特异分子标记的开发
基于ChrY:99.94~99.95Mb和ChrY:100.78~100.79Mb2个较长区段(12025bp和10252bp),共设计获得12对引物。BLAST比对结果表明,所有引物均具有较好的Y染色体特异性和一致性,适合后续验证。
3.3分子标记的特异性与准确性验证
PCR初筛结果显示,12对引物中有8对在雄株中扩增出清晰条带,而在雌株中无扩增产物,表现出雄性特异性;其余4对在部分雌性样品中出现非特异扩增或弱阳性条带。阳性对照ITS2在所有样本中均有扩增,阴性对照无条带,说明实验体系可靠。已报道的MADC6标记在部分雌株中750~1000bp出现非特异性条带,而MADC5标记在部分雌株中出现阳性条带,提示其特异性不足(图1)。
M-Marker;1-龙大麻1 号-2;2-方科1 号-4;3-龙大麻2 号-1;4-龙大麻2 号-5;5-庆大麻1 号-6;6-Tatanka(雌化品种)。
图1 候选雄性特异性分子标记的初筛
进一步的样本扩展验证表明,8对候选标记在36个样本中均表现出100%的鉴定准确率。其中,MSY99M-3、MSY99M-4、MSY99M-5、MSY100M1和MSY100M-7在雄性样品中扩增条带明亮,在雌性样品中无明显目的条带或非特异性扩增条带,特异性和稳定性最佳,可作为大麻幼苗性别鉴定的优选分子标记(图2)。

M-Marker,1-SCAR119,2-SCAR323,3-MSY99M-2,4-MSY99M-3,5-MSY99M-5,6-MSY99M-4,7-MSY100M-1,8-MSY100M-4,9-MSY100M-5,10-MSY100M-7,11-ITS2,12-ITS2(空白模板)。
图2 候选分子标记在不同大麻样本中的验证
4讨论
本研究基于大麻染色体的结构特征,利用生物信息息学方法从基因组层面挖掘Y染色体雄性特异序列片段,并在此基础上设计和验证了一系列雄性特异性分子标记。结果显示,其中5对引物在雄株中均能扩增出清晰且稳定的特异条带,而在雌株中未出现条带,鉴定准确率达100%。这一结果显示,本研究开发的标记在大麻幼苗期的性别鉴定中具有较高的稳定性和应用价值。与已有的OPV-08、SCAR1以及InDel等分子标记的研究结果一致[19-22],本研究进一步证明了基于性染色体序列比对分析的分子标记开发方法是实现大麻早期性别精准鉴定的有效策略。此外,本研究中开发的分子标记也可用于大麻成熟植株的性别鉴定,与苗期鉴定的结果一致。但由于大麻种子的体积和质量较小,本研究尚不能在保证种子正常萌发的基础上完成种子的核酸提取工作,鉴定结果验证困难,因此尚未开展大麻种子的性别分子鉴定工作。未来,本研究将进一步优化种子微创核酸提取方法,以期解决大麻种子的性别鉴定难题。
与以往依赖RAPD、AFLP等随机扩增技术开发的性别标记(如MADC系列)相比,本研究直接利用Y染色体特异区域开发SCAR标记,显著提高了开发效率、可靠性和重复性。例如,验证结果显示MADC5和MADC6在雌株中存在弱阳性条带和非特异性扩增,提示部分早期开发的标记在不同遗传背景下可能存在稳定性不足的问题。本研究采用的方法有效避免了随机扩增标记常见的假阳性和多态性丢失问题,从而提升了性别鉴定的准确度和适用性,并且大量减少实验筛选工作,提高标记开发效率。值得注意的是,尽管已有研究报道了雌性特异性分子标记[23],但鉴于大麻X/Y型性别决定系统的特性及缺乏广泛验证,这类标记的普适性和稳定性仍存在争议。相比之下,基于MSY区域筛选的雄性特异标记在理论基础与实证结果上均更为可靠。
参考文献
[1]Ren G P,Zhang X,Li Y,et al.Large-scale whole-genome resequencing unravels the domestication history of Cannabis sativa[J].Sci Adv,2021,7(29):eabg2286.
[2]Jiang H E,Li X,Zhao Y X,et al.A new insight into Cannabis sativa(Cannabaceae)utilization from 2500year-old Yanghai Tombs,Xinjiang,China[J].J Ethnopharmacol,2006,108(3):414-422.
[3]Luo X Z,Reiter M A,d’Espaux L,et al.Complete biosynthesis of cannabinoids and their unnatural analogues in yeast[J].Nature,2019,567(7746):123-126.
[4]金贤兰.火麻仁的药理作用与临床应用[J].现代医药卫生,2007,23(17):2624-2625.
[5]Burstein S.Cannabidiol(CBD)and its analogs:A review of their effects on inflammation[J].Bioorg Med Chem,2015,23(7):1377-1385.
[6]O’Sullivan S E,Jensen S S,Nikolajsen G N,et al.The therapeutic potential of purified cannabidiol[J].J Cannabis Res,2023,5(1):21.
[7]Lipson Feder C,Cohen O,Shapira A,et al.Fertilization following pollination predominantly decreases phytocannabinoids accumulation and alters the accumulation of terpenoids in Cannabis inflorescences[J].Front Plant Sci,2021,12:753847.
[8]Cristiana Moliterni V M,Cattivelli L,Ranalli P,et al.The sexual differentiation of Cannabis sativa L.:A morphological and molecular study[J].Euphytica,2004,140(1):95-106.
[9]王刚,曹佩,韦学敏,等.分子标记技术在药用植物种质资源研究中的应用[J].中国现代中药,2019,21(11):1435-1444.
[10]Korekar G,Sharma R K,Kumar R,et al.Identification and validation of sex-linked SCAR markers in dioecious Hippophae rhamnoides L.(Elaeagnaceae)[J].Biotechnol Lett,2012,34(5):973-978.
[11]Ling J,Rui-Lin Y,Mao-Xue L I,et al.Identification of a Sex-associated RAPD marker in Ginkgo biloba[J].J Integr Plant Biol,2003,45(6):742.
[12]Sarmah P,Sarma R N.Identification of a DNA marker linked to sex determination in Calamus tenuis Roxb.,an economically important rattan species in northeast India[J].Mol Breed,2011,27(1):115-118.
[13]Patzak J,Vejl P,SkupinováS,et al.Identification of sex in F1 progenies of hop(Humulus lupulus L.)by molecular marker[J].Plant Soil Environ,2002,48(7):318-321.
[14]Chaves-Bedoya G,Nuñez V.A SCAR marker for the sex types determination in Colombian genotypes of Carica papaya[J].Euphytica,2007,153(1):215-220.
[15]Sakamoto K,Shimomura K,Komeda Y,et al.A maleassociated DNA sequence in a dioecious plant,Cannabis sativa L.[J].Plant Cell Physiol,1995,36(8):1549-1554.
[16]Mandolino G,Carboni A,Forapani S,et al.Identification of DNA markers linked to the male sex in dioecious hemp(Cannabis sativa L.)[J].Theor Appl Genet,1999,98(1):86-92.
[17]Sakamoto K,Abe T,Matsuyama T,et al.RAPD markers encoding retrotransposable elements are linked to the male sex in Cannabis sativa L[J].Genome,2005,48(5):931936.
[18]Törjék O,Bucherna N,Kiss E,et al.Novel male-specific molecular markers(MADC5,MADC6)in hemp[J].Euphytica,2002,127(2):209-218.
[19]赵铭森,方书生,陈瑶,等.籽用大麻性别连锁标记的验证及SCAR标记开发[J].热带作物学报,2019,40(10):2076-2082.
[20]孙玉婷,丁美云,王璐瑶,等.工业大麻种子及苗期性别鉴定方法的研究[J].甘肃农业大学学报,2023,58(1):130-136.
[21]孙哲,王金娥,乔永刚.工业大麻发育早期雌雄株鉴定方法的研究[J].农业与技术,2021,41(14):20-24.
[22]陶杰,潘根,黄思齐,等.工业大麻性别连锁Indel标记的筛选与鉴定[J].中国麻业科学,2022,44(3):143-150.
[23]Shao H,Song S J,Clarke R C.Female-associated DNA polymorphisms of hemp(Cannabis sativa L.)[J].J Ind Hemp,2003,8(1):5-9.
[24]Lappin F M,Medert C M,Hawkins K K,et al.A polymorphic pseudoautosomal boundary in the Carica papaya sex chromosomes[J].Mol Genet Genomics,2015,290(4):1511-1522.
[25]Galtier N.Recombination,GC-content and the human pseudoautosomal boundary paradox[J].Trends Genet,2004,20(8):347-349.
[26]Campos J L,Qiu S,Guirao-Rico S,et al.Recombination changes at the boundaries of fully and partially sex-linked regions between closely related Silene species pairs[J].Heredity,2017,118(4):395-403.
[27]van Bakel H,Stout J M,Cote A G,et al.The draft genome and transcriptome of Cannabis sativa[J].Genome Biol,2011,12(10):R102.
[28]Grassa C J,Weiblen G D,Wenger J P,et al.A new Cannabis genome assembly associates elevated cannabidiol(CBD)with hemp introgressed into marijuana[J].New Phytol,2021,230(4):1665-1679.
[29]Laverty K U,Stout J M,Sullivan M J,et al.A physical and genetic map of Cannabis sativa identifies extensive rearrangements at the THC/CBD acid synthase loci[J].Genome Res,2019,29(1):146-156.
[30]Lynch R C,Padgitt-Cobb L K,Garfinkel A R,et al.Domesticated cannabinoid synthases amid a wild mosaic Cannabis pangenome[J].Nature,2025,643(8073):10011010.
文章摘自:樊普丞,林慧慧,段宝忠,等.基于Y染色体特异区段筛选的大麻性别分子鉴定标记开发[J].中草药,2026,57(04):1473-1480.