摘 要:为明确引起胡麻黑斑病病原菌链格孢菌(Alternaria alternata)的生物学特性与其致病机制,研究采用生长速率法与凹玻片萌发法,探究不同培养温度、pH、碳源、氮源对病原菌菌丝生长和孢子萌发的影响,通过酶活测定其细胞壁降解酶的种类及含量。结果表明:病原菌菌丝生长和孢子萌发的最适温度均为25℃,最适pH值均为7;菌丝致死温度为56℃;不同碳、氮源下菌丝生长与孢子萌发情况存在显著差异,菌丝生长最适碳源为麦芽糖、可溶性淀粉,最适氮源为硝酸钾、硝酸钠;孢子萌发最适碳源为葡萄糖、果糖,最适氮源为硫酸铵、硝酸。酶活测定结果表明,该病原菌可产生果胶酶、蛋白酶、纤维素酶,其中果胶甲基半乳糖醛酸酶活性最高,为773.23ng/L。该研究旨在为胡麻黑斑病的抗病育种与田间防治工作奠定基础。
关键词:胡麻;黑斑病;链格孢菌;生物学特性;致病机制
胡麻(Linum usitatissimum L.),又称油用亚麻,是全球范围内历史最为悠久的油料作物之一。作为食品、饲料及工业生产领域的重要原料,其在膳食制作、药物研发及饲料生产等领域具有广泛应用价值[1]。胡麻种子含多种具有独特生物活性的化合物,包括不饱和脂肪酸、木酚素、亚麻胶及可溶性膳食纤维等[2]。其中亚油酸与α-亚麻酸属于人体必需不饱和脂肪酸,其摄入比例对维持人体生长发育至关重要[3]。目前,胡麻在全球50多个国家规模化种植,主产区集中于北半球中高纬度区域[4]。内蒙古自治区为阴山北部高原核心区,胡麻年均播种面积达6.5万公顷,其高原旱地资源与冷凉的气候条件是稳产的重要保障,在我国胡麻产业布局中占据重要战略地位[5]。然而,胡麻生产过程长期面临病害威胁,据统计,胡麻病害种类已超过20种,真菌性病害如胡麻枯萎病(Fusarium oxysporum f.sp.lini)[6]、胡麻炭疽病(Colletotrichum lini)[7],病毒性病害如胡麻花叶病毒(AMV)及细菌性病害胡麻细菌性叶斑病(Pseudomonas syringae pv.linicola)等[8]。2022年,内蒙古产区首次发现由链格孢(Alternaria alternata)引起的胡麻黑斑病,正在严重威胁亚麻产业的发展[8]。
链格孢属真菌是植物病原菌体系里的关键类群,能够诱发多种作物病害。目前已报道的链格孢菌种类超过300种[9],可引发包括百香果果斑病[10]、猕猴桃软腐病[11]、烟草赤星病[12],以及鸢尾生叶斑病[13]等多种病害。该属病原菌的致病机制主要表现为依附于植物体表,通过分泌细胞壁降解酶类破坏植物细胞壁结构,进而侵入组织内部[14]。在内蒙古胡麻种植区,该病集中发生于7月,此时正值胡麻开花结果期,其主要侵害叶片及蒴果外层,染病蒴果外层出现棕褐色或黑褐色斑块,同时表面附着黑色霉层,造成烂果。该病害在内蒙古鄂尔多斯地区发病率达40%~50%,且呈年度周期性发生,对区域胡麻产业构成持续威胁[15]。
为明确引起胡麻黑斑病病原菌的生物学特性,本研究通过设置不同温度、pH、碳源、氮源及细胞壁降解酶活性等条件,测定菌丝及孢子生长情况,以期为后续该病害的精准防控及作物抗病育种相关研究奠定基础。
1 材料与方法
1.1 供试菌株
供试菌株由内蒙古农牧业科学院植物保护研究所提供,采集于内蒙古自治区鄂尔多斯市(39°36′29.3″N,109°46′34.9″E),用于后续生物学特性测定。1.2 供试培养基
PDA培养基、查氏固体培养基、查氏液体培养基、纤维素酶培养基、蛋白酶培养基、果胶酶培养基。
1.3 生物学特性分析
1.3.1 温度对病原菌菌丝生长的影响
将培养7d的黑斑病病原菌菌饼(直径6mm)放置于新鲜的PDA平板中央,分别置于5、10、15、20、25、30、35℃恒温箱中培养(黑暗条件),第7天测量菌落直径,每个处理设置3次重复。
1.3.2 pH对病原菌菌丝生长的影响
用0.1mol/mL NaOH和0.1mol/mL HCL调节培养基pH值,灭菌后倒平板。将病原菌菌饼(直径6mm)分别置于8个不同pH(pH值分别为4、5、6、7、8、9、10、11)的PDA平板中央,在25℃恒温箱中培养7d测量菌落直径,每个处理设置3次重复。
1.3.3 碳、氮源对病原菌菌丝生长的影响
碳源试验:以查氏培养基为基础培养基。用不同碳源(葡萄糖、麦芽糖、可溶性淀粉、乳糖、果糖)等量替换基础培养基中的蔗糖,并以查氏培养基作对照。
氮源试验:以查氏培养基为基础培养基。用不同氮源(硝酸钾、硝酸铵、硫酸铵、氯化铵)等量替换基础培养基中的硝酸钠,并以查氏培养基作对照。将病原菌菌饼(直径6mm)在25℃恒温箱中培养7d测定菌落直径,每个处理设置3次重复。
1.3.4 病原菌致死温度
利用水浴锅设置不同温度(40、45、50、55、60℃)。将病原菌菌饼(直径6mm)放在装有无菌水的试管中,不同温度下分别隔水加热10min,室温冷却后再将菌饼接种到新鲜的PDA平板上,25℃恒温培养7d,随时观察菌丝生长情况。每个处理3次重复。若菌丝不能正常生长,则进一步将温度梯度按1℃间隔划分,最终确定菌丝的致死温度。
1.4 不同培养条件对病原菌孢子萌发的影响
1.4.1 孢子悬浮液的配置
在10×40倍显微镜下,用无菌水将病原菌孢子悬液浓度调至每视野含孢子30~40个(血球计数板计数)。
1.4.2 温度对孢子萌发的影响
取1mL孢子悬浮液,分别在5、10、15、20、25、30、35、40℃恒温培养,每处理重复3次,培养10h后通过显微镜检测孢子萌发情况并计算萌发率,每个处理观测10个不同视野。
1.4.3 pH对孢子萌发的影响
用0.1mol/mLHCI和0.1mol/mLNaOH溶液,将无菌水pH值调节至4、5、6、7、8、9、10、11,吸取1mL孢子悬浮液与不同pH的无菌水等量混合,25℃培养10h后调查孢子萌发情况,每处理重复3次。
1.4.4 碳、氮源对孢子萌发的影响
按照1.3.3中方法配置不同种类的碳、氮源水溶液(不加琼脂),吸取1mL孢子悬浮液与不同的水溶液等量混合,置于25℃下培养10h后调查,每处理重复3次。
1.5 病原菌细胞壁降解酶活性定性测定
果胶酶定性检测:将病原菌菌饼(直径5mm)接种到果胶培养基上,连续培养7d观察病原菌是否生长。纤维素酶定性检测:将病原菌菌饼(直径5mm)接种到纤维素酶分泌检测培养基上,培养7d后用0.1%刚果红水溶液浸染15min,再用1mol/L NaCl水溶液脱色,观察是否会形成透明水解圈。蛋白酶活性检测:将病原菌菌饼(直径5mm)接种到蛋白酶活性培养基上培养7d,用饱和硫酸铵溶液浸没15min,观察是否出现透明水解圈。
1.6 病原菌细胞壁降解酶活性定量测定
将病原菌在PDA培养基上活化5~7d,打取菌饼(直径6mm)接种至液体查氏培养基中,振荡培养3d后用紫外分光光度法测定OD540/232值,根据试剂盒中提供的方法计算PG(多聚半乳糖醛酸酶)、PMG(果胶甲基半乳糖醛酸酶)、PMTE(果胶甲基反式消除酶)、PGTE(多聚半乳糖反式消除酶)酶活性。
2 试验结果
2.1 不同培养条件对病原菌生长的影响
2.1.1 碳源对病原菌生长的影响
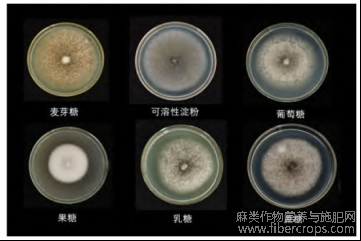
结果表明,该菌株可利用多种碳源,菌丝呈现灰白色,菌落生长伴有轮纹,边缘灰白颜色较浅。对6种供试碳源利用情况存在差异,对麦芽糖和可溶性淀粉利用性最好,其次为蔗糖、葡萄糖、乳糖,对果糖利用性相对较差。
图1 不同碳源对菌丝生长的影响
表1 不同碳源对菌落直径的影响
注:不同小写字母表示差异显著( P<0.05)。下同
2.1.2 氮源对病原菌生长的影响
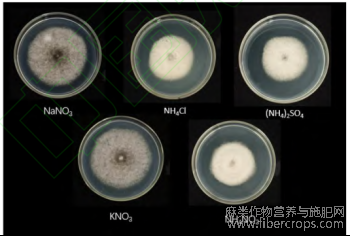
结果表明,在不同氮源培养基中病原菌菌丝生长差异显著。病原菌在以硝酸钾和硝酸钠为氮源的培养基中生长最好,菌落直径也最大,硫酸铵次之,对硝酸铵和氯化铵的利用效果最差、菌落直径最小,菌落颜色渐变为白色,最不利于病菌菌丝的生长。
图2 不同氮源对菌丝生长的影响
表2 不同氮源对菌落直径的影响
2.1.3 温度对病原菌生长的影响
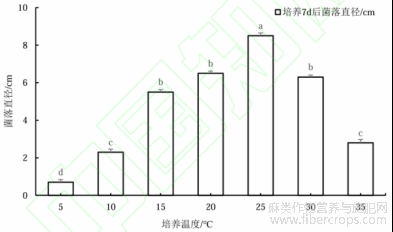
测定结果表明,病原菌在5~35℃均能生长,适宜生长的温度范围比较广泛,但菌落直径存在显著差异。25℃时菌落生长速度最快、菌落直径最大,是病原菌的最适生长温度。10℃以下和35℃生长缓慢,35℃较15℃生长更为缓慢。
图3 不同温度对菌丝生长的影响
2.1.4 pH 对病原菌生长的影响
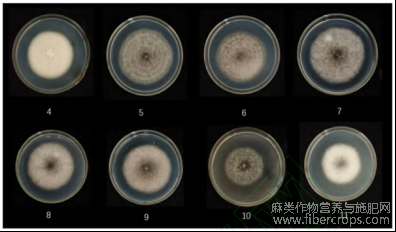
病原菌菌丝生长的pH范围广泛,在pH值4~11范围内均能生长,但不同pH条件下生长情况差异显著。pH值为7时菌落直径最大,菌丝生长情况最好。pH为11时菌落直径最小。病原菌在偏酸或偏碱条件下生长缓慢,菌丝呈白色,pH为7最适其生长。
图4 不同pH下链格孢菌生长情况
表3 不同pH对菌丝生长的影响
2.1.5 病原菌致死温度测定
结果表明,该病原菌耐高温能力较强,温度高于50℃时菌落生长开始变得缓慢,菌丝呈现非正常颜色。当温度达到56℃时,病原菌停止生长,最终确定致死温度为56℃。
表4 菌丝致死温度测定结果(10 min)
注:“+”表示菌丝生长,“-”表示菌丝不生长。
2.2 不同培养条件对病原菌孢子萌发的影响
2.2.1 温度对孢子萌发的影响
病原菌孢子萌发温度范围较广,在5~35℃范围内均能萌发,但不同温度萌发情况存在显著差异。35、5℃时孢子萌发率较低,分别为48.44%和30.98%,20~30℃时萌发率均能达75%以上,最适萌发温度为25℃,萌发率最高,为87.66%,表明病原菌孢子在室温条件下萌发能力较强。
表5 不同温度对病原菌孢子萌发的影响
2.2.2 pH 对孢子萌发的影响
病原菌分生孢子的萌发对pH条件要求不高,孢子在pH4~11均能正常萌发,pH6~9时,孢子萌发情况较好,萌发率均达73%以上。pH为4、11时萌发最差,萌发率分别为49.14%和39.04%,这表明酸碱性对孢子萌发具有一定影响,碱性条件影响更为明显。
表6 不同pH对病原菌孢子萌发的影响
2.2.3 氮源对孢子萌发的影响
结果表明,分生孢子对5种氮源的利用情况存在差异,在(NH4)2SO4、NH4NO3溶液中萌发情况最好,萌发率分别为80.86%和78.55%。NaNO3溶液次之,萌发率为68.99%。NH4Cl溶液和KNO3溶液中萌发率最低,但也高于56%,进一步说明分生孢子萌发能力较强。
表7 不同氮源对病原菌孢子萌发的影响
2.2.4 碳源对孢子萌发的影响
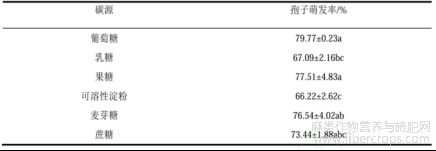
试验结果表明,病原菌分生孢子萌发能力较强,萌发率均达到60%以上。在葡萄糖、果糖的碳源条件下萌发最好,萌发率分别为79.77%、77.51%,且无显著性差异。在蔗糖、麦芽糖溶液中,孢子萌发率较高,均在73%以上。在乳糖、可溶性淀粉中,孢子萌发率相对较低,分别为67.09%和66.22%。
表8 不同碳源对病原菌孢子萌发的影响
2.3 细胞壁降解酶种类及活性测定
2.3.1 细胞壁降解酶的定性测定
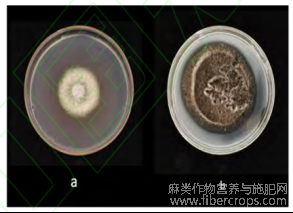
试验结果表明,病原菌在果胶酶、蛋白酶、纤维素酶培养基中均可生长,培养7d后菌落直径与透明圈分别为3.21、6.86、8.28cm。表明该病原菌具有果胶酶、蛋白酶、纤维素酶活性。
图9 病原菌在果胶酶培养基(a)、蛋白酶培养基(b)上的生长期情况
图10 病原菌在 CMC-Na 培养基上的生长情况
2.3.2 细胞壁降解酶定量测定
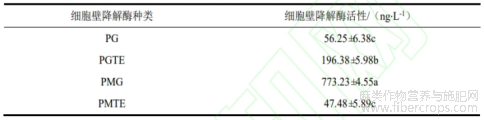
测定结果表明,该病原菌在体外可产生多种细胞壁降解酶,培养3d后,酶活性依次为PMG>PGTE>PG>PMTE,其中,果胶甲基半乳糖醛酸酶(PMG)活性最高,为773.23ng/L,果胶甲基反式消除酶(PMTE)活性最低,为47.48ng/L,多聚半乳糖醛酸酶(PG)和多聚半乳糖反式消除酶(PGTE)的活性分别为56.25、196.38ng/L。
表9 病原菌体外细胞壁降解酶活性
3 讨论
研究表明,链格孢菌 A.alternata 对温度具有较广适应性,但不同种类间的最适生长温度仍存在差异。如乌头黑斑病病原菌链格孢菌在15~35℃范围内均可生长,生长速率在28℃时达到峰值[16];太子参黑斑病病原菌梨黑斑链格孢 A.gaisen 的最适生长温度为25℃[17]。本研究中,胡麻黑斑病病原菌在5~35℃区间内均可生长,且不同温度对链格孢菌的生长速率及孢子萌发等方面均产生明显影响。其中,孢子萌发与菌丝生长的最适温度条件基本一致,均为25℃,病原菌菌丝的致死温度为56℃。其在低温条件下仍可生长,这可能与其独特的地域适应性有关。
病原菌菌丝生长与孢子萌发过程显著依赖对碳源和氮源的利用。菌丝生长对不同碳、氮源的利用表现出一定差异。本研究表明,胡麻黑斑病病原菌对硝酸钠和硝酸钾的利用效率最佳,硫酸铵次之,而氯化铵对菌丝生长具有一定抑制作用,这与张铮等[18]的研究结果相似。研究表明,链格孢菌在碳源利用中更偏向于利用淀粉[19-21],本研究中病原菌对麦芽糖和可溶性淀粉的利用能力最强,其次为蔗糖和葡萄糖,与以上研究结果较一致,推测该病原菌可能通过降解植物中淀粉来进行侵染。在孢子萌发方面,不同碳、氮源条件下孢子萌发率均超过56%,其中硝酸钠、硝酸铵、葡萄糖、麦芽糖条件下萌发效果最优,证明其生态适应性较强且侵染效率高。
pH 作为真菌与宿主相互作用的关键因素,可通过改变酶的活性间接影响病原菌的毒力[22]。该病原菌菌丝生长和孢子萌发对酸碱度的要求较为一致,在pH 4~11条件下均能生长,中性条件下生长和萌发情况较好,偏酸或偏碱条件下影响长势和萌发率,且碱性条件下抑制程度更高,这与赵艳琴等[23]的研究结果较一致。
病原菌致病力强弱与病原菌分泌的细胞壁降解酶活性呈正相关[24],且果胶酶、蛋白酶、纤维素酶可协同作用,加速病原菌的侵染[25]。为进一步解析胡麻黑斑病病原菌的致病机理,本研究对病原菌相关酶活进行测定,结果表明,该病原菌具有较强的产果胶酶、蛋白酶、纤维素降解酶活性,定量测量4种常见的细胞壁降解酶活性,果胶甲基半乳糖醛酸酶活性最高,达773.23ng/L,表明其对植物细胞壁中果胶物质的降解能力较强,推测该病原物具有更强的致病性。病原真菌对寄主的侵染过程涉及复杂的生化机制,现有研究已证实多种病原菌毒素及细胞壁降解酶参与该过程[26]。然而,这些生物活性物质在侵染路径中的协同作用模式及其与寄主防御反应的互作机制,仍需进一步深入研究。
4 结论
胡麻黑斑病是近几年内蒙古胡麻种植区发现的一种新病害,严重影响胡麻产量与品质,本研究对前期分离到的胡麻黑斑病病原菌进行生物学特性分析,结果表明:病原菌菌丝生长和孢子萌发的最适温度均为25℃、最适pH值均为7;菌丝致死温度为56℃;菌丝生长最适碳源为麦芽糖、可溶性淀粉,最适氮源为硝酸钾、硝酸钠;孢子萌发最适碳源为葡萄糖、果糖,最适氮源为硫酸铵、硝酸。酶活测定结果表明,该病原菌可产生果胶酶、蛋白酶、纤维素酶,其中果胶甲基半乳糖醛酸酶活性最高,为773.23ng/L。
参考文献
[1] 王瑞元.我国粮油产销情况喜人[J].中国油脂,2025,50(5):1-4.
[2] 高凤云,伊六喜,周宇,等.亚麻种质资源遗传多样性分析[J].作物杂志,2026(1):60-71.
[3] 何荣军,杨雨,张锦豪,等.萌芽亚麻籽中α-亚麻酸的富集工艺优化及品质分析[J].食品工业科技,2026,47(2):277-286.
[4] Jhala A J, Hall L M. Flax (Linum usitatissimum L.): current uses and future applications[J]. Australian Journal of Basic and Applied Sciences, 2010, 4(9): 4304-4312.
[5] 付可佳,吴馨雨,张鑫,等.我国亚麻种质资源发展现状及存在问题探讨[J].植物学研究,2023(4):185-191.
[6] 潘虹,关凤芝,吴广文,等.尖孢镰刀菌亚麻专化型生物学特性研究[J].东北农业大学学报,2011,42(7):50-56.
[7] 杨学,关凤芝,李柱刚,等.亚麻炭疽病病原菌鉴定及药剂筛选[J].东北农业大学学报,2010,41(3):26-28.
[8] Séguin-Swartz G, Eynck C, Gugel R K, et al. Diseases of Camelina sativa(false flax)[J]. Canadian Journal of Plant Pathology, 2009, 31(4): 375-386.
[9] Ali S, Tyagi A, Rajarammohan S, et al. Revisiting Alternaria-hostinteractions: New insights on its pathogenesis, defense mechanisms and control strategies[J]. Scientia Horticulturae, 2023, 322: 112424.
[10] 赵晓珍,王红林,解璞,等.百香果果斑病的病原鉴定及防控药剂初筛[J].中国植保导刊,2022,42(10):9-14.
[11] 李雨静,庞敏,杜孝田,等.猕猴桃软腐链格孢菌(Alternaria alternata)的鉴定与防治[J].安徽农业科学,2025,53(13):135-139.
[12] 谢林,蔡海林,李建勇,等.长沙烟区烟草赤星病病害调查与病原菌鉴定[J].中国烟草科学,2025,46(2):45-51.
[13] 杜磊,袁信恩,程淑媛,等.鸢尾链格孢叶斑病病原菌鉴定[J].植物保护,2024,50(6):209-214.
[14] 沈钰森,王建升,盛小光,等.十字花科植物黑斑病的研究进展[J].核农学报,2021,35(3):623-634.
[15] Zhao Y Z, Jia X Y, Gao F Y, et al. Flax black spot caused by Alternaria alternata, a new disease afflicting leaves and the exocarps of flax in China[J]. Journal of Phytopathology, 2023, 171(7/8):376-380.
[16] 周佳,王铁霖,苗玉焕,等.乌头黑斑病病原菌的鉴定?生物学特性及其有效杀菌剂研究[J].中国中药杂志,2022,47(5):1215-1221.
[17] 张武君,刘保财,陈菁瑛,等.福建太子参黑斑病病原菌鉴定及生物学特性研究[J].中国中药杂志,2023,48(10):2732-2738.
[18] 张铮,李秀青,刘昱锋.三叶木通叶斑病病原菌的生物学特性及生物防治[J].陕西师范大学学报(自然科学版),2015,43(5):61-66.
[19] 谷清义,黄晨晨,武志鹏,等.芍药黑斑病病原菌的分离鉴定?生物学特性及植物源药剂筛选[J].中药材,2024,47(10):2428-2433.
[20] 淡志伟,初雷霞,杨林林,等.箭叶淫羊藿叶枯病致病菌Alternaria alternata的生物学特性及防治研究[J].中药材,2025,48(1):35-39.
[21] 罗其鑫,杨莹,李思,等.蓝莓叶斑病病原菌鉴定及生物学特性[J].江苏农业科学,2023,51(5):146-154.
[22] 侯杨威,王鑫源,杨林林,等.地黄轮纹病病原菌的细胞壁降解酶活性测定及致病性分析[J].北方园艺,2022(19):106-113.
[23] 赵艳琴,石凯,张丽娟,等.高粱链格孢叶斑病菌生物学特性研究[J].植物保护,2021,47(6):196-200.
[24] 沈煜铠,李昭煜,李佳佳,等.黄芪根腐病菌分离鉴定及细胞壁降解酶活性比较[J].兰州交通大学学报,2021,40(3):101-109.
[25] 金梦军,杨成德,李统华,等.细胞壁降解酶在球刺盘孢侵染过程中的作用[J].植物保护,2024,50(3):88-98.
[26] 郝士鋆.大丽轮枝菌对单/双子叶植物的侵染过程及胞外蛋白组研究[D].北京:中国农业科学院,2021.
文章摘自: 赵远征,宋亚迪,高凤云,张立华,何瑞超,费楠,卢雁媛,余江泳,周宇.胡 麻黑斑病病原菌生物学特性研究[J].中国麻业科学. https://link.cnki.net/urlid/43.1467.S.20260324.1034.006。