摘 要:【目的】建立以发根农杆菌K599诱导红麻产生不定根的转基因诱导体系,为红麻基因功能验证提供参考?【方法】构建含有橘黄色荧光基因td Tomato和红色报告基因RUBY的过表达载体pCAMBIA1305.1,并导入发根农杆菌K599中,穿刺接种于3个红麻品种‘LDF早4’‘中福红2号’‘紫花B1’子叶期幼苗下胚轴处,在90%高湿条件下培养接种材料;通过常规PCR鉴定?qRT-PCR检测?荧光检测和可见光检测,评价过表达载体的转化效果?【结果】采用发根农杆菌K599成功诱导3个品种红麻产生不定根,其毛状根植株诱导率为88.67%~90.67%,毛状根植株阳性率均在85%以上?通过常规PCR鉴定和qRT-PCR检测确定外源片段整合到毛状根基因组中并得到表达,在激发光源下可观察到转基因毛状根有明显橘黄色荧光,且荧光毛状根tdTomato的表达量是对照组的2~5倍,同时能够在可见光下观察到红麻根部出现红色毛状根,由此成功建立了发根农杆菌K599诱导红麻产生不定根的转基因诱导体系?【结论】建立了发根农杆菌K599介导的红麻毛状根诱导体系,其诱导率在3个品种间无显著差异,具有高效?通用且无需组培的特点,可实现基因功能的快速验证?
关键词:红麻;发根农杆菌;毛状根;tdTomato;报告基因
红麻(Hibiscus cannabinus L.)是锦葵科(Mal-vaceae)木槿属(Hibiscus)一年生韧皮纤维作物,具有生物量大?纤维素含量高?耐盐碱?适应性强?栽培管理粗放等特点,是一种宝贵资源[1]?目前,红麻转基因体系尚不完善,转化效率较低,主要受限于组织培养再生困难[2]?农杆菌侵染效率低[3]等因素?现有研究主要通过花粉管途径和茎尖侵染法实现遗传转化,但涉及外源遗传转化的报道较少?发根农杆菌(Agrobacteri umrhizogenes)是根瘤菌科(Rhizobiaceae)农杆菌属(Agrobacterium)的一种革兰氏阴性土壤细菌,从植物伤口入侵后,可通过Ri质粒(root-inducing plasmid)的T-DNA将rol基因稳定整合到宿主植物基因组中,从而诱导植物产生大量高度分枝的毛状不定根[4]?前人研究表明,毛状根培养作为一种体外植物生物技术,具备高生长速率?良好的生物化学稳定性,且无需经历转基因中艰难的再分化过程等特点,这些特点使其在植物生物技术领域崭露头角,为相关研究与应用提供了一种极具潜力的技术手段[5],也为研究植物根部基因功能提供良好的材料?因此建立优良的遗传转化体系对红麻基因的功能研究具有重要意义?近年来,发根农杆菌介导的毛状根遗传转化体系已成功应用在大豆[6]?花生[7]?箭筈豌豆[8]?菠菜[9]等植物中?其中,发根农杆菌K599可诱导多种植物产生毛状根,且保持较高的诱导率?如:周雪婷等[10]通过3种方法采用发根农杆菌K599侵染平邑甜茶,发现3叶龄幼苗期的毛状根植株诱导率高达96%,而5叶龄幼苗的毛状根植株诱导率为65%;陶娜等[11]用发根农杆菌K599对甘薯品种‘泰中6号’进行侵染,其毛状根植株诱导率为59.19%;樊颖伦等[12]以携带红色荧光蛋白基因DsRed2的发根农杆菌K599为载体,对不同品种黄瓜幼苗的下胚轴实施穿刺接种,其毛状根植株诱导率达89%~94%,且阳性植株转化率为55%?目前关于红麻稳定的遗传转化体系的构建鲜有报道,鉴于此,本研究用发根农杆菌K599在红麻上建立高效的毛状根诱导体系,获得具有野生型茎?叶和转基因毛状根的嵌合体植株,旨在为研究红麻基因功能提供新的思路和途径?
1 材料与方法
1.1 材料
供试红麻品种分别为‘LDF早4’‘中福红2号’‘紫花B1’,均来自福建农林大学麻类研究室;发根农杆菌K599?MSU440购于武汉淼灵生物科技有限公司;大肠杆菌DH5α感受态细胞购于上海唯地生物技术有限公司;表达载体的构建以pCAM-BIA1305.1为骨架,由本实验室进行改造与保存,改造后该载体含有橘黄色荧光基因tdTomato,命名为pCHCLXZ?
1.2 方法
1.2.1 菌株的选择与活化
用K599?MSU440菌株在含有对应筛选抗生素的LB固体培养基上划线后,置于培养箱(28℃)中培养使其活化?挑取单菌落分别接种于含有链霉素的LB液体培养基中,于200r·min-1?28℃下培养12h,调节菌液的D600nm为1并置于-80℃条件下保存?
1.2.2 菌株的转化
将保存在-80℃条件下的K599感受态细胞置于冰上融化,在100μLK599感受态细胞中加入1μgpCHCLXZ载体,用移液枪吸打混匀,依次进行冰上静置5min?液氮静置5min?37℃水浴5min?冰浴5min等操作,然后在室温下加入700μLLB液体培养基,于200r·min-1?28℃振荡培养2h,再于6000r·min-1离心1min,收集菌液?将100μL上清重悬菌块涂布于含有50mg·L-1硫酸卡那霉素?50mg·L-1链霉素的LB固体培养基上,筛选阳性单克隆的培养皿并倒置在培养箱(28℃)培养2d?挑取单菌落进行菌落PCR检测,确定目标条带位置正确后,选取阳性克隆菌液,于6000r·min-1?37℃的摇床中振荡培养12h?调节菌液的D600nm为1,用于后续穿刺侵染植株?
1.2.3 红麻种子处理
选取颗粒饱满的红麻种子用0.5%高锰酸钾浸泡25min后用清水冲洗干净,并播种于72孔育苗盘中?选取萌发3~4d,且子叶未展开的植株作为遗传转化起始材料?每50粒种子可用于一个红麻品种转化试验,每个品种设3次重复?
1.2.4 红麻毛状根的诱导
选取子叶未展开?下胚轴为3~5cm的植株,以靠近初生根1~2cm的下胚轴为穿刺位点,用注射器蘸取转化载体后的菌液进行穿刺,重复3次,以注射未转化载体的K599菌液的植株为阴性对照?植株穿刺接种后用湿润的蛭石完全覆盖穿刺位点,并用塑料薄膜覆盖使其保持高湿度,在28℃下避光共培养24h后,转入培养箱[28℃?t(光照)∶t(黑暗)=16h∶8h]继续培养,每天浇灌1/2霍格兰营养液,保持蛭石湿润以诱导产生毛状根?
1.2.5 转基因材料的统计
在红麻幼苗下胚轴穿刺接种菌液后的第14天分别统计3个红麻品种诱导出毛状根的植株数量,毛状根植株诱导率/%=(具毛状根植株数/侵染植株总数)×100?当毛状根长至1cm以上时使用TCSSP8激光共聚焦显微镜(德国徕卡公司),在波长为554nm的激发光源下透过滤光片观察是否有橘色荧光,具有荧光的毛状根植株为阳性毛状根植株?毛状根植株阳性率/%=(具阳性毛状根植株数/具毛状根植株数)×100?
1.2.6 转基因毛状根
PCR和qRT-PCR的检测使用CTAB法[13]提取毛状根DNA,以TO为引物,采用PCR检测目的片段?PCR反应程序:95℃预变性5min;95℃变性30s,60℃退火30s,72℃延伸1min(35个循环);72℃延伸5min;4℃下保存?PCR扩增后进行2%凝胶电泳验证?使用植物RNA提取试剂盒(南京诺唯赞生物科技股份有限公司)提取阴性对照和阳性毛状根的RNA,使用TransScript® One?Step gDNA Removal and cDNA Synthesis SuperMix(北京全式金生物技术股份有限公司)反转录试剂盒,将RNA反转录合成cDNA第1链?设计内参基因Actin7和目的基因tdTomato的qRT?PCR引物序列(表1)?以反转录获得的cDNA为模板,采用PerfectStart® Green qPCR SuperMix(+DyeⅡ)(北京全式金生物技术股份有限公司)荧光定量试剂盒,以红麻肌动蛋白Actin7基因(GenBank登录号:KY382441.1)作为内参基因?反应体系20.0μL,含1.0μLcDNA?上游和下游引物各0.4μL?10.0μL2×PerfectStart® Green qPCR SuperMix(+DyeⅡ)?8.2μLNuclease-freeWater?使用Applied BiosystemsTM7500实时荧光定量PCR系统(美国ThermoFisher公司)进行qRT?PCR检测?反应程序:94℃预变性30s;94℃变性5s,60℃退火15s,72℃延伸10s(40个循环)?每组样品设置3次技术重复?反应结束后采用2-ΔΔCt法进行表达量分析?
表1 本研究使用的引物
1.2.7 含RUBY基因载体的构建及红麻毛状根的诱导
采用SnapGene软件设计连接载体引物(表1),将红色报告基因RUBY与pCHCLXZ表达载体进行连接,随后进行红麻毛状根诱导,其侵染方法与“1.2.4”的相同?
1.2.8 数据处理与分析
采用Microsoft Excel 2019软件对试验数据进行整理,采用SPSS26.0软件对数据进行差异显著性分析?
2 结果与分析
2.1 发根农杆菌对红麻毛状根的诱导效率
采用K599?MSU440菌株对红麻品种‘中福红2号’进行初步诱导的结果表明,K599?MSU440菌株对毛状根植株的诱导率分别为92.66%?80.64%,且K599菌株的诱导率显著高于MSU440菌株,故后续研究中均采用K599菌株进行试验?
2.2 红麻毛状根诱导体系的建立
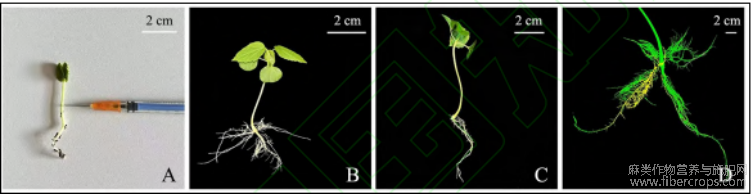
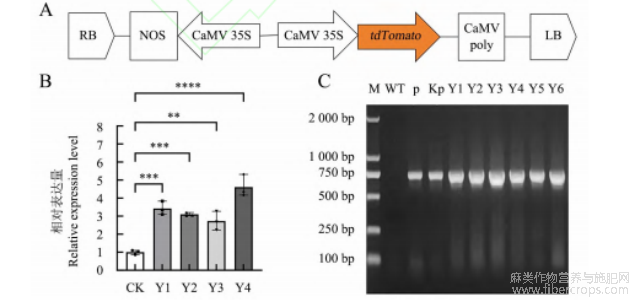
参照已确立的诱导大豆毛状根的穿刺法[6],并进行优化?在子叶未展开的红麻幼苗下胚轴(图1A)处穿刺接种发根农杆菌,两周后从穿刺位点处发出大量毛状根(图1B),在发出毛状根的部位处截断原生主根,此时的植株即为具有野生型茎?叶和毛状根的嵌合植株,并可继续生长(图1C)?为了验证本研究建立的毛状根诱导体系是否有效,采用3种方法对毛状根进行检测?首先在激发光源下透过滤光片可观察到转基因毛状根有明显橘黄色荧光(图1D)?其次提取6条荧光毛状根的DNA并进行PCR检测,在转基因毛状根中获得荧光基因tdTomato,其片段长度为695bp,而对照组未检测到tdTomato(图2C)?最后对荧光毛状根tdTomato的表达量进行qRT?PCR检测,发现4条荧光毛状根tdTomato的表达量是对照组的2~5倍(图2B)?表明毛状根诱导和基因转化均是成功的?
图1 红麻毛状根的诱导及阳性毛状根观测
图2 转基因毛状根荧光基因的鉴定
2.3 毛状根诱导体系在红麻上的普适性
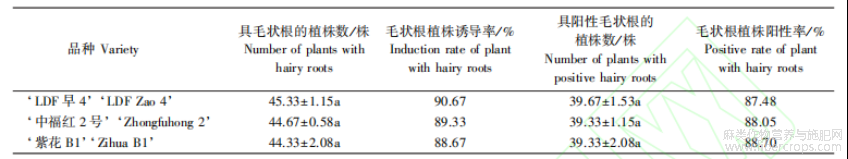
用转化载体后的菌液对红麻进行毛状根诱导,结果(表2)显示:红麻3个品种长出毛状根的植株均达到40株以上,诱导率为88.67%~90.67%;毛状根呈阳性的植株均达35株以上,阳性率为87.48%~88.70%?表明本研究方法可成功诱导红麻产生毛状根,不同基因型的红麻均可适用?
表2 不同品种红麻毛状根植株诱导率和毛状根植株阳性率1
1) 同列数据后附相同字母表示差异不显著(P>0.05)?
2.4 阳性毛状根植株的RUBY鉴定
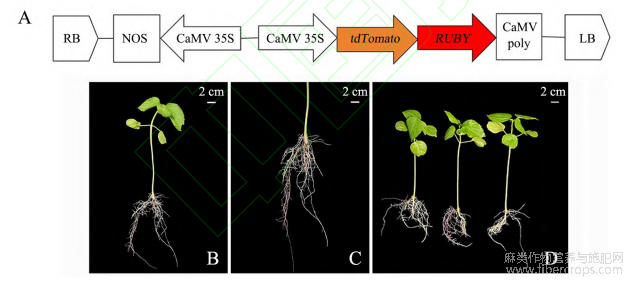
本研究获得的红麻转基因毛状根有明显橘黄色荧光,但需在激发光源下透过滤光片才能观察到?为了能裸眼观察到基因是否成功转入,在改造后的pCHCLXZ载体上进一步插入红色报告基因RUBY(图3A)?在菌液穿刺侵染幼苗后的第10天,能够明显观察到根部出现红色毛状根(图3B-D),红色毛状根的出现表明该基因已成功转入?
A.RUBY?pCHCLXZ载体构建的示意图;B.产生毛状根的植株;C.毛状根局部;D.产生毛状根的3个品种植株?
图3 含RUBY基因的载构建及红麻毛状根的诱导
3 讨论
发根农杆菌的种类较多,其对外植体的侵染率和转化率存在差异[14]?前人研究表明,发根农杆菌K599是西瓜[15]?箭筈豌豆[8]?白羽扇豆[16]?杜梨[17]等产生毛状根的最适菌株,其毛状根植株诱导率分别可达75.0%~90.0%?70.0%?72.5%?85.0%,说明K599菌株对大多数植物的毛状根都具有较高的诱导率?本研究使用发根农杆菌K599?MSU440侵染红麻品种‘中福红2号’幼苗下胚轴,发现K599菌株对毛状根植株的诱导率更高,表明K599菌株比MSU440菌株更适于诱导红麻发根?为验证K599菌株对不同红麻品种的侵染率是否存在差异,本研究继续使用K599菌株对3个红麻品种进行侵染,其诱导率为88.67%~90.67%,表明K599菌株具有适应性广和诱导率高的特点,可用于红麻毛状根的诱导?发根农杆菌对植物毛状根的诱导率受到多种因素的影响,如侵染部位[18]?菌液浓度[19]?菌株类型[9,16,20]等?前人研究表明,发根农杆菌侵染部位多为植株幼嫩组织,因其细胞分裂旺盛,更有利于接受外源DNA的侵染[21]?如甜瓜子叶期幼苗有利于发根农杆菌的顺利侵染[18]?本研究中,发根农杆菌的接种时期为红麻幼苗的子叶期,植株茎尖生长点恰好位于子叶节区域,细胞处于极为活跃的分裂状态,有利于发根农杆菌对毛状根的诱导,此结果与前人的研究结果[21]相同?湿度和光照条件会影响发根农杆菌的侵染效果,因此在穿刺接种后需进行保湿和黑暗处理?其中,黑暗条件是诱导产生毛状根的必要条件之一,如在薄壳山核桃[22]和黄瓜[23]诱导产生毛状根的研究中均采用黑暗处理?本研究将一次性塑料杯倒扣在红麻幼苗上,并用湿润的蛭石覆盖接种部位,确保接种部位处于黑暗条件下?
转基因根系的鉴定是进行基因功能研究的基础[12],目前有多种鉴定方法,如β-葡萄糖苷酸酶(β?glucuronidase,GUS)染色法[24]?荧光蛋白观察法[25]和报告基因PCR鉴定法[11]?其中:GUS染色法材料制备过程繁琐且具有组织破坏性;报告基因PCR鉴定法需对毛状根进行DNA提取和报告基因引物设计,不适合进行大批量转基因毛状根的鉴定;而荧光蛋白观察法所需时间短,对组织和植株的损伤最小,在大量鉴定中具有优势[26]?目前常用的荧光蛋白的颜色有绿色?黄色?红色和蓝色,红色荧光蛋白在植物根系上的应用最为广泛?本研究选取tdTomato基因是因为其在红色荧光蛋白中具备最高的亮度,能够使其在适宜的激发光源下,对转基因根系与非转基因根系进行观测区分?在此基础上,本研究构建了包含裸眼可视报告基因RUBY的pCHCLXZ载体,RUBY基因在阳性植株鉴定中具有独特优势,整个过程无需借助任何化学处理手段或特殊设备,仅凭借裸眼即可直接观察载体是否成功转入基因?故本研究使用包含RUBY的pCHCLXZ载体对红麻根部进行侵染,并产生红色毛状根的结果,与胡晓[27]使用RUBY侵染矮牵牛后根部产生红色毛状根的结果一致,均能在可见光下观察到红色毛状根,表明该体系可高效且便利地实现对外源基因表达的可视化操作?
4 结论
本研究采用发根农杆菌K599成功构建了红麻产生不定根的转基因诱导体系?该体系的接种时期为红麻幼苗子叶期,接种后用蛭石覆盖接种部位,随后进行24h的黑暗培养,并注意保持接种部位持续湿润,植株在接种后10d左右产生毛状根?K599菌株对3个品种红麻毛状根植株诱导率均较高,且毛状根植株阳性率可达85%以上?该体系具有周期短?操作简单且对试验条件的要求不高等特点,可用于红麻基因的遗传转化与功能验证研究?
参考文献
[1]AN X,JING R,ZHANG J Y,et al.Research progress on tissue culture and genetic transformation of kenaf(Hibiscus cannabinus)[J].Open Life Sciences,2017,12(1):465-472.DOI:10.1515/biol-2017-0055.
[2]BANKS S W,GOSSETT D R,LUCAS M C,et al.Agrobacterium?mediated transformation of kenaf(Hibiscus cannabinus L.)with theβ?glucuronidase(GUS)gene[J].Plant Molecular Biology Reporter,1993,11(2):101-104.DOI:10.1007/BF02670466.
[3]HERATH S P,SUZUKI T,HATTORI K.Factors influencing Agrobacterium mediated genetic transformation of kenaf[J].Plant Cell,Tissue and Organ Culture,2005,82(2):201-206.DOI:10.1007/s11240-004-7289-y.
[4]MEHROTRA S,SRIVASTAVA V,RAHMAN L U,et al.Hairy root biotechnology:indicative timeline to understand missing links and future outlook[J].Protoplasma,2015,252(5):1189-1201.DOI:10.1007/s00709-015-0761-1.
[5]汪虞骅,黄思远,郝雪婷,等.植物毛状根研究与应用进展[J].现代农业科技,2024(22):138-142.DOI:10.3969/j.issn.1007-5739.2024.22.033.WANG Y H,HUANG S Y,HAO X T,et al.Research and application progress on plant hairy roots[J].Modern Agricultural Sciences and Technology,2024(22):138-142.DOI:10.3969/j.issn.1007-5739.2024.22.033.
[6]宗晓秋,张东升,黄文坤,等.发根农杆菌诱导大豆毛状根体系的建立[J].华中农业大学学报,2012,31(6):699-703.DOI:10.3969/j.issn.1000-2421.2012.06.007.ZONG X Q,ZHANG D S,HUANG W K,et al.Establishment of soybean hairy root system induced by Agrobacterium rhizogenes[J].Journal of Huazhong Agricultural University,2012,31(6):699-703.DOI:10.3969/j.issn.1000-2421.2012.06.007.
[7]曾丽丹,陈容钦,李晓云,等.AhHDA1影响花生毛状根生长的研究[J].华南师范大学学报(自然科学版),2021,53(6):74-78.DOI:10.6054/j.jscnun.2021094.ZENG L D,CHEN R Q,LI X Y,et al.The effects of AhHDA1 on the growth of peanut hairy roots[J].Journal of South China Normal University(Natural Science Edition),2021,53(6):74-78.DOI:10.6054/j.jscnun.2021094.
[8]梅错,刘志鹏.发根农杆菌介导的箭筈豌豆毛状根遗传转化体系的建立[J].中国草地学报,2020,42(5):1-7.DOI:10.16742/j.zgcdxb.20190305.MEI C,LIU Z P.Agrobacterium rhizogenes?mediated transformation system of common vetch(Vicia sativa subsp.nigra)[J].Chinese Journal of Grassland,2020,42(5):1-7.DOI:10.16742/j.zgcdxb.20190305.
[9]徐悦,曹英萍,王玉,等.发根农杆菌介导的菠菜毛状根遗传转化体系的建立[J].植物学报,2019,54(4):515-521.DOI:10.11983/CBB18257.XU Y,CAO Y P,WANG Y,et al.Agrobacterium rhizogenes?mediated transformation system of Spinacia oleracea[J].Chinese Bulletin of Botany,2019,54(4):515-521.DOI:10.11983/CBB18257.
[10]周雪婷,武凯凯,崔蓝芳,等.平邑甜茶发根农杆菌介导转化体系构建与优化[J].果树学报,2024,41(5):999-1008.DOI:10.13925/j.cnki.gsxb.20240046.ZHOU X T,WU K K,CUI L F,et al.Construction and optimization of transformation system mediated by Agrobacterium rhizogenes in Malus hupehensis var.mengshanensis G.Z.Qian&W.H.Shao[J].Journal of Fruit Science,2024,41(5):999-1008.DOI:10.13925/j.cnki.gsxb.20240046.
[11]陶娜,李茂兴,郭华春.发根农杆菌介导的甘薯遗传转化体系优化[J].生物技术通报,2023,39(10):175-183.DOI:10.13560/j.cnki.biotech.bull.1985.20230369.TAO N,LI M X,GUO H C.Optimization of sweet potato genetic transformation system mediated by Agrobacterium rhizogenes[J].Biotechnology Bulletin,2023,39(10):175-183.DOI:10.13560/j.cnki.biotech.bull.1985.2023-0369.
[12]樊颖伦,徐风琳,周慧珍,等.黄瓜发根农杆菌转化体系的建立[J].分子植物育种,2025,23(1):113-118.DOI:10.13271/j.mpb.023.000113.FAN Y L,XU F L,ZHOU H Z,et al.Establishment of transformation system of Agrobacterium rhizogenes in cucumber[J].Molecular Plant Breeding,2025,23(1):113-118.DOI:10.13271/j.mpb.023.000113.
[13]徐建堂,祁建民,陈涛,等.适合于胞质基因组扩增的红麻成熟叶片DNA提取改良方法[J].植物遗传资源学报,2013,14(2):347-351.DOI:10.13430/j.cnki.jpgr.2013.02.012.XU J T,QI J M,CHEN T,et al.The improvement method of extraction DNA in mature kenaf leaves suitable for cytoplasmic genome amplifying[J].Journal of Plant Genetic Resources,2013,14(2):347-351.DOI:10.13430/j.cnki.jpgr.2013.02.012.
[14]SHARAFI A,HALEH B,SOHI H H,et al.A reliable and efficient protocol for inducing hairy roots in Papaver bracteatum[J].Plant Cell,Tissue and Organ Culture,2013,113(1):1-9.DOI:10.1007/s11240-012-0246-2.
[15]王平勇,徐永阳,赵光伟,等.发根农杆菌介导西瓜转基因过表达体系的建立[J].果树学报,2019,36(12):1763-1770.DOI:10.13925/j.cnki.gsxb.20190454.WANG P Y,XU Y Y,ZHAO G W,et al.Preliminary study on Agrobacterium rhizogenes?mediated gene overexpression system in watermelon[J].Journal of Fruit Science,2019,36(12):1763-1770.DOI:10.13925/j.cnki.gsxb.20190454.
[16]詹玉洁,刘博文,张仟,等.发根农杆菌介导白羽扇豆转基因过表达体系的建立[J].植物生理学报,2021,57(3):655-660.DOI:10.13592/j.cnki.ppj.2020.0452.ZHAN Y J,LIU B W,ZHANG Q,et al.Establishment of Agrobacterium rhizogenes?mediated gene overexpression system in white lupin[J].Plant Physiology Journal,2021,57(3):655-660.DOI:10.13592/j.cnki.ppj.2020.0452.
[17]郝紫微,戴雨沁,张绍铃,等.发根农杆菌介导的杜梨毛状根遗传转化方法[J].湖北农业科学,2021,60(1):151-154,159.DOI:10.14088/j.cnki.issn0439-8114.2021.01.031.HAO Z W,DAI Y Q,ZHANG S L,et al.Genetic transformation method of hairy roots mediated by Agrobacterium rhizogenes for Pyrus betulaefolia[J].Hubei Agricultural Sciences,2021,60(1):151-154,159.DOI:10.14088/j.cnki.issn0439-8114.2021.01.031.
[18]郝金凤,荆培培,张丽,等.应用农杆菌介导的生长点转化方法建立甜瓜遗传转化技术[J].华北农学报,2014,29(2):116-120.DOI:10.3969/j.issn.1000-7091.2014.02.022.HAO J F,JING P P,ZHANG L,et al.Establishment of transformation method for melon using Agrobacterium?mediated plant genetic transformation via plant apical meristem[J].Acta Agriculturae Boreali?Sinica,2014,29(2):116-120.DOI:10.3969/j.issn.1000-7091.2014.02.022.
[19]孙春玉,孙旸,刘庆忠.根癌农杆菌介导的苹果遗传转化研究进展[J].中国农学通报,2010,26(4):231-233.DOI:10.3969/j.issn.1000-4440.2008.02.021.SUN C Y,SUN Y,LIU Q Z.Advances in research of genetic transformation of apples with Agrobacterium[J].Chinese Agricultural Science Bulletin,2010,26(4):231-233.DOI:10.3969/j.issn.1000-4440.2008.02.021.
[20]刘雪羽,杜笑雪,陈思源,等.发根农杆菌介导的光皮桦毛状根高频诱导体系及遗传转化[J].农业生物技术学报,2021,29(3):495-505.DOI:10.3969/j.issn.1674-7968.2021.03.009.LIU X Y,DU X X,CHEN S Y,et al.Agrobacterium rhizogenes mediated high frequency hairy root induction system and genetic transformation in Betula luminifera[J].Journal of Agricultural Biotechnology,2021,29(3):495-505.DOI:10.3969/j.issn.1674-7968.2021.03.009.
[21]熊笙屹,厍润祥,张璐,等.转基因植物发根农杆菌研究的进展及应用[J].农业与技术,2017,37(16):72-74.DOI:10.11974/nyyjs.20170833061.XIONG S Y,SHE R X,ZHANG L,et al.Research progress and application of Agrobacterium rhizogenes in transgenic plants[J].Agriculture and Technology,2017,37(16):72-74.DOI:10.11974/nyyjs.20170833061.
[22]谢晓婷,黄巧宇,温广超,等.非组培依赖的发根农杆菌介导的薄壳山核桃转化体系构建[J].果树学报,2022,39(1):131-140.DOI:10.13925/j.cnki.gsxb.20210383.XIE X T,HUANG Q Y,WEN G C,et al.Construction of Agrobacterium rhizogenes?mediated transformation system of Carya illinoinensis without dependence on tissue culture[J].Journal of Fruit Science,2022,39(1):131-140.DOI:10.13925/j.cnki.gsxb.20210383.
[23]曹庆丰.发根农杆菌K599侵染黄瓜形成转基因毛状根的初步研究及orf14基因的克隆[D].杭州:杭州师范大学,2012.DOI:10.7666/d.y2132082.CAO Q F.Preliminary analysis on transgenic hairy root induced from cucumber by Agrobacterium rhizogenes K599 and cloning of orf14 gene[D].Hangzhou:Hangzhou Normal University,2012.DOI:10.7666/d.y2132082.
[24]冯志娟,刘娜,卜远鹏,等.发根农杆菌介导的菜用豌豆遗传转化体系构建[J].园艺学报,2024,51(10):2439-2448.DOI:10.16420/j.issn.0513-353x.20230944.FENG Z J,LIU N,BU Y P,et al.Establishment of Agrobacterium rhizogenes?mediated genetic transformation system in vegetable pea[J].Acta Horticulturae Sinica,2024,51(10):2439-2448.DOI:10.16420/j.issn.0513-353x.2023-0944.
[25]樊颖伦,徐风琳,周慧珍,等.黄瓜发根农杆菌转化体系的建立[J].分子植物育种,2025,23(1):113-118.DOI:10.13271/j.mpb.023.000113.FAN Y L,XU F L,ZHOU H Z,et al.Establishment of transformation system of Agrobacterium rhizogenes in cucumber[J].Molecular Plant Breeding,2025,23(1):113-118.DOI:10.13271/j.mpb.023.000113.
[26]CROWR M,GARTLAND J S,MCHUGH A T,et al.Real?time GUS analysis using Q?PCR instrumentation[J].Journal of Biotechnology,2006,126(2):135-139.DOI:10.1016/j.jbiotec.2006.04.018.
[27]胡晓.矮牵牛PMADS18和PMADS9基因的定点敲除及RUBY标记基因在矮牵牛中的应用[D].重庆:西南大学,2022.DOI:10.27684/d.cnki.gxndx.2022.001450.HU X.Site?directed knockout of PMADS18 and PMADS9 genes and application of RUBY marker gene in Petunia hybrida[D].Chongqing:Southwest University,2022.DOI:10.27684/d.cnki.gxndx.2022.001450.
文章摘自:李函,赵雅琦,朱仕心,等.发根农杆菌介导的红麻毛状根诱导体系的建立[J/OL].福建农林大学学报(自然科学版),1-8[2025-11-03].https://doi.org/10.13323/j.cnki.j.fafu(nat.sci.).202503013.