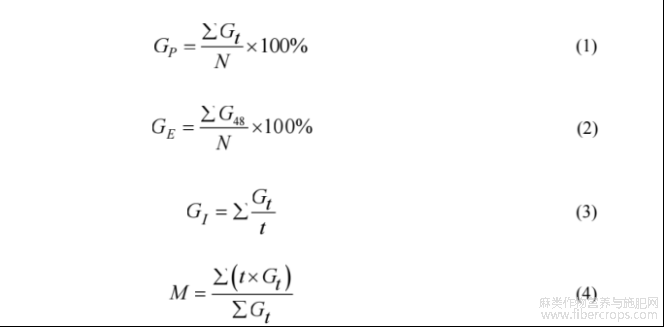摘 要:试验以罗布红麻和大叶白麻为材料,研究不同剂量碳离子束辐照处理对两种罗布麻种子萌发和幼苗生长的影响,以期为罗布红麻和大叶白麻碳离子束辐照诱变育种提供技术支撑。结果表明:碳离子束辐照对罗布红麻的发芽率无显著影响,高剂量显著抑制了发芽势、发芽指数、根长和芽长,延长了发芽时间,低剂量影响不显著;所有辐照处理均提高了其出苗率。大叶白麻的发芽率、发芽势和发芽指数随剂量先升高,在40Gy达到峰值后逐渐降低。低剂量(20Gy)辐照促进了根和芽的生长,随着辐照剂量的升高,根长和芽长逐渐降低。在20~80Gy时出苗率显著提升,更高剂量则转为抑制。碳离子束辐照对两种罗布麻存活率的影响相似,低剂量能够提高幼苗存活率,高剂量显著降低幼苗存活率,但是肩部剂量各不相同,罗布红麻的半致死剂量(LD50)为182Gy,根长半数生长抑制剂量(GR50)为149Gy;大叶白麻的LD50和GR50均为149Gy,表明大叶白麻对于碳离子束辐照更敏感。
关键词:罗布红麻;大叶白麻;碳离子束;种子萌发;幼苗生长
罗布麻是夹竹桃科具有重要经济价值的多年生草本植物,广泛分布于中国北方及西北地区,如新疆、甘肃、青海、内蒙古等地。罗布麻在药用、纺织、饲用等方面具有较高的开发性,同时也是生态治理的理想植物。罗布麻根、茎、叶、花全草均可入药,罗布麻叶也可制保健茶。其纤维性能突出,有“野生纤维之王”的美誉。罗布麻具有较强的耐旱、耐盐碱、耐寒和耐高温等特性,不仅能够改良土壤、调节气候、保持水土、防风固沙,还能为当地动物提供栖息地与食物来源,减少盐渍化发生,提高土壤肥力[1-2]。我国学者将其划分为2属3种,即罗布麻属的罗布麻(Apocynum venetum)、白麻属的白麻(Poacynum pictum)、大叶白麻(Poacynum hendersonii)[3]。新疆是我国罗布麻分布最广的产区,也是罗布麻最佳产地。其中罗布麻花叶药效成分相对较好[4],适宜水分条件较好的环境,在盐碱地改良方面的特性较为突出,耐旱相对较弱;大叶白麻主产纤维、花叶大[5-6],常生长在干旱、盐渍化程度较高的区域,对耐旱耐盐性适应性较强[7-9],是新疆产区2种仅有的可开发利用的罗布麻[1]。
我国野生罗布麻资源曾十分丰富,近年来由于过度开发,加之生境日益恶化,野生资源受到了严重破坏,致使目前我国罗布麻种质资源急剧减少[10]。新疆维吾尔自治区巴音郭楞蒙古自治州尉犁县是国内最大的罗布麻原生地,根据中国纺织工程学会相关报道[11],2023年县域内的罗布麻面积约10.67万hm2,连片密集区1.13万hm2,人工种植2000hm2,具有独特的资源优势,但仍以野生资源为主。野生罗布麻存在株丛衰老、密度下降、产量低、植株矮小稀疏等退化现象,并且缺乏人工选育的专用型品种,不能满足当前罗布麻产业面向现代纤维工业和大规模种植的高产、抗逆、纤维质量优良等的专业育种品种的需求。此外,由于高度自花授粉导致天然杂交率低于0.5%,长期自交易致品种衰退,限制了遗传多样性的获取,目前筛选出了少量农艺性状和黄酮含量突变体,突变频率和表型筛选效率仍有限,在遗传变异方面仍需进一步加强[12-14]。
辐照诱变往往伴随染色体结构变异,能够打破基因连锁,产生全新的性状组合,从而突破遗传瓶颈,显著提升突变频率,为筛选抗逆、增产等新性状提供丰富的遗传材料,实现品种创新[15-16]。重离子束是新的诱变源,具有独特的生物学和物理学优势,包括尖锐的Bragg峰、传能线密度(LET)高、相对生物学效应(RBE)高、局部效应模型(LEM)特性突出、损伤后修复效应小及能量沉积的空间分辨性好等[17-19]。这些特性使得重离子束辐照诱变育种生理损伤小、DNA损伤修复率低,短时间内形成大量新的种质资源,因而在植物诱变育种中具有突变频率高、突变谱广的特点。该技术广泛用于作物品种选育,目前已经选育出了一批高产、抗病、抗旱的优良品种,如“陇辐2号”春小麦[20];选育出了高产、早熟的甜高粱品种“近甜1号”[21];选育出了稳产性好、含油率高、抗病性较强的“近葵1号”[22]。近年来,该技术也逐渐应用于药用植物种质资源创新研究,利用重离子辐照柴胡[23]、青蒿[24]、当归[25]、党参[26]、鸡冠花[27]、灵芝[28]、蛹虫草[29]等获得了一定的成效,选育出了中药材新品种。多年的育种实践表明,重离子束诱变技术是品种改良的重要途径之一。
辐照诱变育种中,剂量是关键因素之一。适宜的辐照剂量可以获得较多有益突变体和丰富的突变谱,既不会因为辐照剂量过低无法达到诱变效果,也不会因为辐照剂量过高导致当代植株存活率降低,减少后代筛选群体的数量。确定精准的诱变剂量,关键在于确定作物品种对诱变剂的耐受水平。植物对辐射的敏感性因物种、品种、器官、含水量、倍性水平和其他生理条件等多种因素而异[30-31]。辐照当代效应的量化研究是获得适宜的辐照剂量的重要步骤。研究人员对大田作物、蔬菜、水果等进行大量研究,测量萌发相关指标、存活率、根长、芽长和结实率等来确定诱变剂量[31-37]。因此,本研究采用碳离子束辐照罗布红麻和大叶白麻种子,对种子萌发和苗期生长的辐照效应进行评估,旨在确定两种罗布麻的适宜辐照剂量,以期为新疆罗布麻进行大规模碳离子束辐照诱变育种提供理论依据。
1 材料与方法
1.1 试验材料及重离子束辐照处理
罗布红麻和大叶白麻种子来自中国科学院新疆生态与地里研究所,4℃冰箱贮藏备用。
利用中国科学院近代物理研究所兰州重离子研究装置(Heavy Ion Research Facility in Lanzhou,HIRFL)产生的碳离子束(Carbon ion beam,CIB)进行辐照处理,初始能量为80MeV/u,总能量为960MeV,传能线密度(LET)为36keV/um,剂量率为60Gy/min,照射剂量为20、40、80、120、200、300、400、500、600、800Gy,对照置于与辐照组相同的环境中但不进行辐照处理,共计10个辐照组和1个对照组(0Gy)。
1.2 植物材料辐照后培养
种子辐照后,先用蒸馏水浸泡30min,再用75%酒精消毒30s,蒸馏水冲洗3~4次,播种于放有三层滤纸的无菌培养皿中,每皿50粒种子,均匀散开。置于培养间中培养,温度26℃,光周期为14h光照/10h黑暗,光强200μmol/m2/s。每天补充无菌水使培养皿内的滤纸保持湿润。每隔12h统计发芽个数(胚根或胚芽突破种皮2mm视为发芽),直至发芽结束。播种15d后每个重复随机选取20~30株测量根长和芽长。另选一部分种子播种于穴盘,每个处理点播50粒种子,培养基质为泥炭土,统计出苗率和存活率。每个处理3个重复。
1.3 指标测定
1.3.1 种子萌发指标测定
种子萌发指标包括发芽率、发芽势、发芽指数和平均发芽时间[38]。其计算公式如下:
式中:GP为发芽率,%;GE为发芽势,%;GI为发芽指数;M为平均发芽时间,h;Gt为在t小时的发芽数;G48为48 h的发芽数;N为种子总数;t为发芽小时数。
1.3.2 根长和芽长测定
将各剂量组的幼苗取出并拍照,利用 ImageJ-2.3.0测定根长和芽长。
根长(cm):从基部到主根根尖的长度;
芽长(cm):从基部到顶芽处茎的长度。
1.3.3 出苗率和存活率测定
在种子种植后每隔7d统计幼苗株数,计算出苗率(子叶出土展开视为出苗)和存活率(长出2对及以上真叶的幼苗记为存活植株)。
式中:E为出苗率,%;S为存活率,%;W为播种粒数;n为出苗数;m为存活数。
1.4 数据统计分析
使用Excel 2021记录数据并整理分析,用SPSS 27中单因素方差分析(ANOVA)的LSD法分析不同剂量处理的种子样本。用 Origin 2022 进行曲线拟合、相关性分析和绘图。图表结果用三次重复的平均值(Mean)±标准差(Standard Deviation, SD)表示。
2 试验结果与分析
2.1 碳离子束辐照对罗布红麻和大叶白麻种子萌发的影响
2.1.1 碳离子束辐照对罗布红麻和大叶白麻种子发芽率、发芽势的影响
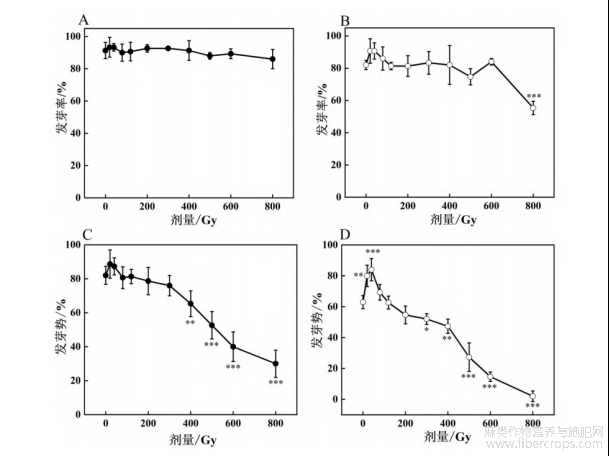
碳离子束辐照对罗布红麻和大叶白麻种子发芽率的影响如图1(A、B)所示。碳离子束辐照处理对罗布红麻种子发芽率的影响不显著。大叶白麻种子的发芽率在不同碳离子束辐照处理下呈先升高后降低趋势。800Gy辐照处理下,大叶白麻种子的发芽率显著下降(p<0.05),与对照相比降低了32.52%。综合各剂量辐照处理下的发芽率可以发现,碳离子束辐照对罗布红麻的发芽率影响不大,但是对大叶白麻的发芽率呈现低剂量刺激效应和高剂量抑制作用。
发芽势是表征种子发芽速度和整齐度的指标。碳离子束辐照对罗布红麻和大叶白麻种子发芽率的影响如图1(C、D)所示。罗布红麻及大叶白麻种子的发芽势在不同剂量碳离子束辐照处理下均呈先升高后降低趋势。罗布红麻的发芽势在400Gy后均受到显著抑制(p<0.05);大叶白麻的发芽势在20Gy和40Gy的处理下与对照相比分别升高了26.98%和33.3%(p<0.05),在300Gy及以后受到显著抑制。综上所述,低剂量碳离子束辐照对罗布红麻和大叶白麻种子发芽速率有一定的促进作用,而高剂量减缓了发芽速率,发芽不整齐,发芽时间有差异。
注:“*”“**”“***”分别表示在p<0.05、p<0.01、p<0.001水平下差异显著。下同
图1 碳离子束辐照对罗布红麻(A、C)和大叶白麻(B、D)种子发芽率和发芽势的影响
2.1.2 碳离子束辐照对罗布红麻和大叶白麻发芽指数、平均发芽时间和发芽数的影响
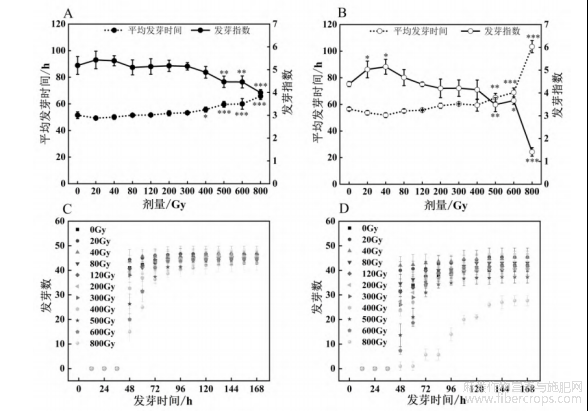
发芽指数是衡量种子活力的指标。由图2(A)可知,罗布红麻发芽指数在20~400Gy时,发芽指数与对照相比变化不显著;随辐照剂量升高(400Gy后),发芽指数逐渐下降,说明高剂量抑制了发芽指数,且剂量越大抑制作用越强。由图2(B)可知,大叶白麻种子的发芽指数在不同碳离子束辐照处理下呈先升高后降低趋势。与对照相比,大叶白麻发芽指数在20Gy和40Gy显著升高(p<0.05),在40Gy时达到最高峰,发芽指数为5.15,上升了17.31%;之后随剂量增加持续下降,800Gy显著降低,发芽指数为1.42,与对照相比降低了67.65%,结果表明,辐照剂量增加对大叶白麻发芽抑制作用明显,且整体抑制趋势比罗布红麻更显著,罗布红麻对辐照剂量耐受性相对更高,大叶白麻更敏感。
从前面发芽势的结果可以看出,辐照影响了两种罗布麻的发芽时间,因此,进一步分析了平均发芽时间。两种罗布麻的平均发芽时间随着剂量的升高而升高(图2A、B)。较高辐照剂量(≥400Gy)使罗布红麻萌发进程明显变慢,但整体变化幅度小,说明罗布红麻对剂量耐受性较强。大叶白麻的平均发芽时间在较高辐照剂量(≥500Gy)下显著延长,800Gy时超过了100h,显示高剂量对发芽延迟作用更强烈。结果表明,与碳离子束辐照对发芽指数的影响一致,高剂量碳离子束辐照对大叶白麻发芽延迟作用更强烈,表明大叶白麻比罗布红麻对碳离子束辐照更敏感。
碳离子束辐照对罗布红麻和大叶白麻种子发芽数的影响如图2(C、D)所示。对照组在48h后有较多发芽,体现自然发芽节奏。罗布红麻在前60h,500~800Gy处理的发芽数显著低于对照组,之后随着时间的延长,发芽数逐渐与对照组相差不大。大叶白麻种子在800Gy辐照处理下,发芽数在整个发芽阶段都显著低于对照组;在48、60h时,20、40Gy辐照处理下的发芽数显著高于对照组,400~600Gy处理下的发芽数显著低于对照组,之后随着时间的增加,发芽数逐渐与对照组相差无几。600、800Gy辐照处理下,发芽数明显减少,反映高剂量抑制发芽,且使发芽同步性差。剂量升高会延长平均发芽时间、降低发芽同步性,且高剂量(500~800Gy)的抑制效应更显著。
图2 碳离子束辐照对罗布红麻(A、C)和大叶白麻(B、D)种子发芽指数、平均发芽时间和发芽数的影响
2.2 碳离子束辐照对罗布红麻和大叶白麻生长的影响
2.2.1 碳离子束辐照对罗布红麻和大叶白麻出苗率和存活率的影响
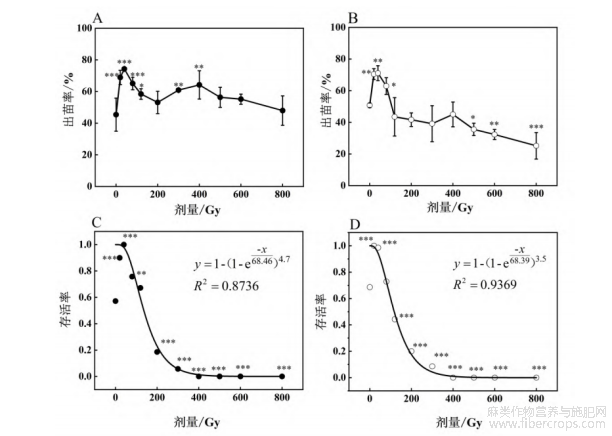
碳离子辐照对罗布红麻和大叶白麻出苗率的影响如图3(A、B)所示。碳离子束辐照处理提高了罗布红麻种子的出苗率(图3A)。40Gy的辐照处理下,罗布红麻的出苗率最高,比对照提高了63.67%。低剂量(20~80Gy)碳离子束辐照提高了大叶白麻的出苗率,与对照相比,分别增加了38.75%、40%和23.9%;600、800Gy碳离子束辐照后,大叶白麻出苗率显著降低,分别降低了36.37%和49.49%。
罗布红麻和大叶白麻种子经不同剂量的高能碳离子束辐照后,其存活率受到不同程度的影响(图3C、D)。低剂量促进了幼苗的存活,较高剂量抑制了幼苗的存活。20~80Gy的碳离子束辐照显著提高了罗布红麻幼苗的存活率,分别显著提升了57.5%、75%和32.5%。
200Gy以后辐照显著降低了存活率,200Gy辐照下存活率降低至12.75%,300Gy的存活率仅为4% ,超过300Gy的幼苗难以存活,全部死亡(图3C)。20~80Gy的碳离子束辐照提升了大叶白麻幼苗的存活率(图3D),20Gy和40Gy 辐照后存活率显著上升,比对照上升了45.83%和43.75% ,高于80Gy的碳离子束辐照抑制了大叶白麻幼苗的生长,300Gy辐照处理下生长抑制效应最为明显,300Gy的存活率仅为6%。
图3 碳离子束辐照对罗布红麻(A、C)和大叶白麻(B、D)出苗率和存活率的影响
2.2.2 碳离子束辐照对罗布红麻和大叶白麻幼苗根长芽长的影响
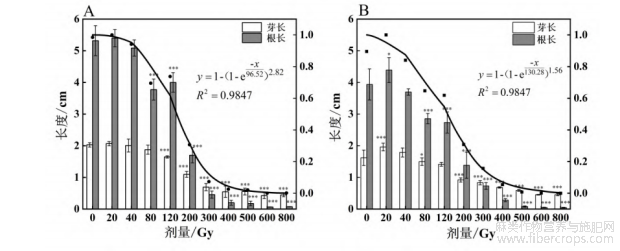
碳离子束辐照下罗布红麻和大叶白麻幼苗根长和芽长的生长受到了不同程度的影响(图4)。与对照相比,较低剂量(20~40Gy)碳离子束辐照对罗布红麻幼苗根的生长没有明显影响,随着辐照剂量增加幼苗生长受到抑制作用,尤其是200Gy 以上的碳离子束辐照极显著抑制了根和芽的生长(p<0.001)。与罗布红麻略有不同,碳离子束辐照后,大叶白麻的根长和芽长均呈现先上升后下降的趋势。20Gy的辐照下,大叶白麻胚根和胚芽的生长受到了显著促进,随着辐照剂量的升高,根长和芽长逐渐降低,剂量越高,胚根和胚芽生长受到的抑制越严重。罗布红麻和大叶白麻的根长和芽长均在200Gy时急剧下降,在超过300Gy后,抑制最为明显,均不能正常生长,在后续生长中都难以存活,600、800Gy的辐照处理下胚根和胚芽已停止生长。相同剂量下,碳离子束辐照对根的生长抑制高于芽的生长,表明根的生长对辐照更敏感。
图4 碳离子束辐照对罗布红麻(A)和大叶白麻(B)幼苗根长和芽长的影响
2.3 罗布红麻和大叶白麻的半致死剂量和半数生长抑制剂量
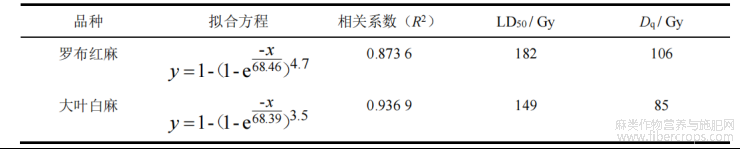
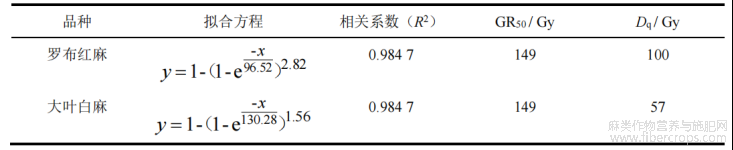
在相同剂量的碳离子束辐照下,两种罗布麻的根生长抑制程度高于芽,说明根对辐照更为敏感,因此,选用存活率和根长进行半数有效剂量的计算。根据单击多靶模型S=1-N,对两种罗布麻的存活率和根长进行拟合,结果如表1和表2所示。碳离子束辐照罗布红麻的肩部剂量(Dq)为106Gy,大于大叶白麻肩部剂量85Gy,说明罗布红麻具有比大叶白麻更加“宽阔”的肩部区域,对低剂量辐照的抵抗性较强。根据拟合曲线计算罗布红麻的LD50为182Gy,GR50为149Gy;大叶白麻的LD50为149Gy,GR50为149Gy。
表1 碳离子束辐照两种罗布麻存活率剂量效应拟合方程
表2 碳离子束辐照两种罗布麻根长剂量效应拟合方程
2.4 碳离子束辐照后罗布红麻和大叶白麻各参数间的相关性分析
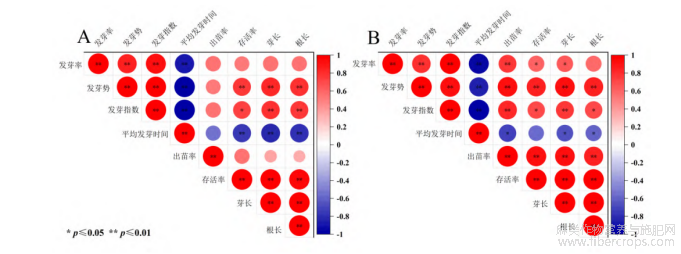
为了进一步探究辐照处理后罗布红麻和大叶白麻发芽率、发芽势、发芽指数、平均发芽时间、出苗率、存活率、根长和芽长之间的关系,对各参数进行Pearson’s相关系数分析。由图5可知,发芽率、发芽势和发芽指数相互间呈极显著正相关,说明种子早期萌发活力、整体发芽能力协同性强。平均发芽时间与发芽率、发芽势和发芽指数呈显著负相关,说明发芽活力越高,平均发芽时间越短。罗布红麻的发芽率和发芽指数与存活率、芽长和根长呈正相关;存活率与芽长和根长呈极显著正相关;平均发芽时间与存活率、芽长和根长呈极显著负相关。由此表明,种子活力高低与幼苗的存活率和生长存在相关性。大叶白麻的发芽率与出苗率、存活率和芽长呈正相关;发芽势和发芽指数与出苗率、存活率、芽长和根长呈极显著正相关;出苗率与存活率、芽长和根长呈极显著正相关;存活率与芽长和根长呈极显著正相关;平均发芽时间与出苗率、芽长和根长呈负相关。由此表明,早期萌发的活力会影响出苗率、存活率和根长芽长。
注:“*”代表p≤0.05 ,“**”代表p≤0.01。
图5 碳离子束辐照后罗布红麻(A)和大叶白麻(B)萌发和生长的相关性分析
3 讨论
辐照剂量是影响育种成效的重要因素,不同作物和品种对辐照的敏感性不同,因此需要选择适宜的辐照剂量以获得最佳诱变效果。一般采用半数有效剂量作为适宜的辐照剂量,采用的指标包含种子发芽率、植株成活率、生长抑制程度和植株的不育程度等[30,32]。本文研究了不同剂量的碳离子辐照处理对罗布红麻和大叶白麻种子萌发特性的影响,发现碳离子束辐照处理对罗布红麻种子的发芽率影响不显著(图1A),除了大剂量(800Gy)辐照降低了大叶白麻发芽率,中低剂量辐照对大叶白麻发芽率没有明显影响(图1B)。这与陆锡宏[39]、刘振昌[40]和管翊君[41]等的结果类似,在试验选择的辐照范围内,辐照对种子的发芽率影响不大。表明碳离子束辐照对种子萌发率的影响可能存在剂量阈值,当辐照剂量超过一定的阈值,会降低种子萌发率[37]。虽然碳离子束辐照对罗布红麻的发芽率没影响,但是影响了其发芽势、发芽指数和平均发芽时间。较高剂量碳离子束辐照抑制了罗布红麻和大叶白麻的发芽势和发芽指数,延长了其发芽时间(图1、2)。Amirikhah等[42]研究发现高剂量(100~400Gy)的伽马辐照显著降低了发芽指数、发芽速度系数和种子储备损耗率,并延长了平均发芽时间;管翊君等[41]的研究结果表明,随着辐照剂量的升高,小麦种子的生活力降低,即高剂量的辐照处理可以延缓小麦种子的发芽。种子萌发在植物生命周期中起着重要作用。发芽势、发芽指数和平均发芽时间是衡量种子发芽能力的重要指标,它们分别反映了种子的发芽速度、发芽能力以及出苗的整齐度和发芽快慢。种子发芽时间的延长表明高剂量辐照对种子的内部组织造成了损伤,影响了细胞的生长和根尖伸长。重离子辐照会引发大量活性氧(ROS)的产生,包括超氧阴离子、羟基自由基和过氧化氢等,大量的ROS会与抗氧化酶、结构蛋白以及遗传物质发生化学反应,从而导致这些生物大分子失去活性、变得不稳定,甚至发生降解,从而扰乱种子正常的代谢过程和生理平衡[43]。生物大分子的损伤同时激活了种子的保护机制和修复系统。通过超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、谷胱甘肽还原酶(GR)等酶促系统,以及抗坏血酸(AsA)、谷胱甘肽(GSH)等非酶促系统来平衡ROS的影响[44],碳离子辐照种子时,高密度的能量沉积会在种子胚胎细胞核中产生团簇的DNA损伤(DSBs),这些复杂的DNA损伤通过非同源末端链接(NHEJ)和同源重组等途径进行修复来维基因组的稳定性[45]。种子自身的保护机制和修复系统抵消一部分碳离子辐射造成的损伤,可能是种子在大剂量辐照受损后仍然能够完成萌发的原因。
碳离子束对植物生长发育具有双重效应,即低剂量辐照具有促进作用,高剂量辐照具有抑制作用。本研究也发现低剂量的碳离子束辐照能够促进大叶白麻种子萌发,提高种子发芽率、发芽势,缩短发芽时间、加快发芽进程(图1、2),同时也促进了幼苗生长,根长和芽长明显增加(图4)。利用重离子辐照小麦[46]种子也有类似现象,低剂量辐照能够促进种子萌发和幼苗生长,以及根尖分生组织细胞有丝分裂,而高剂量辐照则表现出明显的抑制作用。60Co-γ射线辐照紫薇[47]和粉黛乱子草[48]种子也有相似结果,低剂量的辐照能够促进种子的萌发和幼苗的生长,提升一些生理生化指标。低剂量辐射对植物等生物体产生的促进作用被称为辐射刺激效应。这种刺激效应体现在对植物生长、抗性以及代谢物质积累等方面的增强作用[49]。辐射刺激效应已在多种植物中得到证实,并在生物产业中展现出潜在应用价值[50],这为罗布麻产业开发提供了可行的借鉴方向。
萌发(种子发芽)和幼苗生长是植物生命周期中紧密相连但性质不同的两个阶段。虽然碳离子辐照对罗布麻种子发芽没有明显影响,但其对幼苗生长产生了明显的影响(图3、4)。低剂量对罗布红麻和大叶白麻的根长和芽长有一定的促进作用,而高剂量抑制了罗布红麻和大叶白麻幼苗的生长,超过300Gy的碳离子束辐照使两种罗布麻的幼苗难以存活。根生长抑制程度比芽的生长更严重,说明罗布麻根对碳离子辐照更为敏感。重离子辐照能够诱导植物根尖中产生微核和染色体畸变,并且微核和染色体片段数量随着辐照剂量的增加而增加,而高微核率和变异过大导致高致死率,导致幼苗不能存活[51-52]。根长和芽长与发芽势、发芽指数和存活率呈正相关,与平均发芽时间呈负相关,说明早期萌发的活力会影响后期的存活率、根长和芽长(图5)。罗布红麻的发芽率与后期的出苗率、存活率、芽长和根长的相关性是弱正相关,说明它的萌发阶段(发芽)与生长阶段(出苗、根芽生长)之间的“衔接”相对薄弱;大叶白麻前期萌发与后期的生长相关性比较强,它的前期萌发与后期生长表现之间具有高度的一致性。这种差异可能源于两种罗布麻的遗传基因差异。大叶白麻可能在基因层面上对辐照造成的损伤(如DNA损伤、细胞功能受阻)更敏感或更依赖快速修复机制。罗布红麻则可能具备更好的“容错”机制,其生长策略不完全依赖于萌发速度[53]。罗布红麻出苗率与存活率相关性不显著,大叶白麻出苗率和存活率呈显著正相关,说明某些基因(如DNA修复基因)在不同物种或品种之间可能存在突变或表达水平差异[54]。
适宜辐照剂量的选择是重离子束辐照诱变育种成功的关键因素之一,有人用LD30~LD50和GR30~GR50[31],也有人用LD25,50,75和GR25,50,75[55],但多以半致死剂量或者半数生长抑制剂量作为适宜剂量的参考剂量,基于育种目标和工作实际需求,在半致死剂量的基础上调整实际辐照剂量[30-32]。在LD50水平,突变率足以在幸存个体中引发遗传变化,但又不至于导致整个种群的灭绝。GR50是另一个用于衡量辐射影响的重要参数,它表明在这个剂量下,突变很可能发生,但会导致显著的生长变化,而不一定导致死亡。LD50和GR50剂量在存活率和突变诱导之间取得了平衡,使其成为诱变育种计划的有效目标。在本研究中罗布红麻的LD50为183Gy,GR50为149Gy;大叶白麻的LD50为149Gy,GR50为149Gy(表1、2)。罗布红麻的半致死剂量高于大叶白麻的半致死剂量,这表明罗布红麻对辐照剂量耐受性相对更高,大叶白麻更敏感。生物化学层面的差异,尤其是抗氧化能力与代谢途径的不同,在决定植物对辐照的耐受性方面起着重要作用[56]。罗布红麻黄酮类成分的含量高于大叶白麻[57],能够更好地清除自由基。此外,罗布红麻有更高的杂合度,意味着遗传背景更丰富,使其在应对环境剧变时拥有更强的适应与修复潜力[57],它们共同发挥作用抵御辐照引起的氧化应激损伤和细胞损伤,因而对辐照更耐受,具有更高的LD50。有研究表明,碳离子辐照西蓝花种子、火龙果种子和小麦种子的LD50分别为415.89、24、55Gy[33,35,46];60Co-γ射线辐照紫薇、粉黛乱子草和扁穗雀麦种子的LD50分别为197、274、224Gy[34,47-48]。剂量的差异与辐照的辐射源、植物种类以及辐照材料的差异有关[32],因此,在开展大规模诱变育种前,有必要确定每个品种的适宜辐照剂量。后续还需要进行辐照诱变突变体筛选,进一步研究适宜辐照剂量和机理。
4 结论
不同辐照剂量的碳离子束对罗布红麻和大叶白麻种子萌发和幼苗生长的辐照效应不同。两种罗布麻对碳离子辐照敏感性不同,高剂量碳离子束辐照抑制了罗布红麻的发芽势、发芽指数,延长了发芽时间,但是对发芽率影响不大,大多数种子均能够正常萌发,但是会抑制幼苗的生长甚至造成幼苗死亡。大叶白麻整体上呈现先升高后降低的趋势,低剂量促进了大叶白麻的发芽势、发芽指数、出苗率和存活率,以及幼苗的生长,加快了发芽进程,更高剂量则转为抑制,造成幼苗死亡。根据曲线拟合结果,罗布红麻的半致死剂量(LD50)为 182Gy,根长半数生长抑制剂量(GR50)为 149Gy;大叶白麻的半致死剂量(LD50)为 149Gy,根长半数生长抑制剂量(GR50)149Gy。结果表明,大叶白麻对于碳离子束辐照较罗布红麻更为敏感。上述结果可以为罗布红麻和大叶白麻碳离子束辐照诱变的适宜辐照剂量提供参考。
参考文献
[1]杨宏伟,陈茹,姚国民,等.新疆罗布麻产业发展现状分析[J].新疆农业科学, 2024, 61(增刊 1): 163-167.
[2]王悦.罗布麻耐盐性评价及耐盐基因 ApHKT1 表达模式分析[D].北京: 中国农业科学院, 2024.
[3]马浩.种植密度和灌水量对罗布白麻农艺性状、饲用价值和纤维品质的影响[D].新疆农业大学, 2024.
[4]王世聪,王华雨,葛诗慧,等.罗布麻叶的研究进展及质量标志物预测分析[J/OL]. 中华中医药学刊, 1-26[2026-01-29]. https://link.cnki.net/urlid/21.1546.R.20250912.1255.014.
[5]王金玉.大叶白麻可纺性纤维的联合脱胶制备工艺构建及参数优化[D].东华大学, 2022.
[6]史俊友,索有瑞,李国梁,等.大叶白麻叶多糖提取及组分分析[J]. 中成药, 2010,32(01): 102-106.
[7]蔡卿龄,张勇,魏原杰,等.新疆产大叶白麻不同部位黄酮类成分含量分析[J].食品科学,2014,35(22): 211-214.
[8]石秋梅,邓翻云,吴敏言,等.罗布麻和大叶白麻种子萌发及幼苗生长耐盐性研究[J].北方园艺, 2014(12): 128-133.
[9]张博.三种不同环境的罗布麻植物结构研究[D].东北师范大学, 2008.
[10]赵玉凤,郜继红,曾彦军,等.罗布麻属和白麻属种子形态特征及生活力的测定方法[J].草业科学, 2020,37(4): 743-752.
[11]中国纺织工程学会.关于召开2023 首届全国(尉犁)罗布麻产业合作大会的通知[EB/OL]. [2023-10-10]. https://www.ctes.com.cn/ZYTZ/art/2023/art_cdd29d909e5440ffafcfde6c61386dab.html.
[12]王悦,黄晓钰,陈平,等.罗布红麻多倍体诱导条件优化及生物学特征变化分析[J/OL].分子植物育种, 1-14[2026-01-29]. https://link.cnki.net/urlid/46.1068.S.20231114.1504.014.
[13]麻浩,郁崇文,粟建光,等.罗布麻的研究现状与开发利用[J]. 中国麻业科学, 2017,39(3): 146-152.
[14]任婷婷,任宏伟,杜海娜,等.罗布麻 EMS 突变体库构建及黄酮变异突变体筛选[J].植物遗传资源学报, 2020, 21(3): 655-662.
[15]赵星棋,岳明昊,王志新,等.大豆辐射诱变育种相关研究进展[J]. 中国种业, 2025(2): 13-17.
[16]Oladosu Y, Rafii M Y, Abdullah N, et al. Principle and application of plant mutagenesis in crop improvement: a review[J]. Biotechnology & Biotechnological Equipment, 2016,30(1): 1-16.
[17]刘瑞媛,金文杰,曲颖,等.重离子束辐射诱变技术在植物育种中的应用[J].广西科学,2020,27(1): 20-26.
[18]曲颖,李文建,周利斌,等.重离子辐射植物的诱变效应研究及应用[J].原子核物理评论,2007(4): 294-298.
[19]Yamaguchi H, Hase Y, Tanaka A, et al. Mutagenic effects of ion beam irradiation on rice[J]. Breeding Science, 2009, 59(2): 169-177.
[20]李雁民,赵连芝,王勇,等.利用重离子辐射诱变育成小麦新品种陇辐 2 号[J].麦类作物学报,2004(2): 137.
[21]Dong X, Li W. Biological features of an early-maturity mutant of sweet sorghum induced by carbon ions irradiation and its genetic polymorphism[J]. Advances in Space Research, 2012, 50(4): 496-501.
[22]曲颖,周利斌,卯旭辉,等.油用型向日葵新品种近葵 1 号的选育[J]. 中国种业, 2023(1): 101-103.
[23]Liu X, Wang M, Wang Y, et al. Carbon ion beam-induced radiation hormesis in Bupleurum chinense DC.: Insights from growth, physiological, and metabolomic analyses for increased bioactive substances[J]. Plant Stress, 2025: 101037.
[24]梁妍,周翔,郭建钊,等.青蒿新品种“科蒿 1 号”的选育研究[J]. 中国中药杂志,2019,44(24): 5363-5367.
[25]李硕,李成义,李敏,等.离子辐射选育当归新品种安全性评价[J]. 中草药, 2018, 49(11): 2662-2670.
[26]汪淑霞,宋振华.党参新品种渭党3 号选育报告[J].甘肃农业科技, 2015(11): 11-13.
[27]孙兰弟. 12C6+重离子辐照鸡冠花和油菜的诱变效应及霸王组织培养的研究[D].兰州大学, 2008.
[28]李颖颖,谢瑀婷,全卫丰,等.低能 N+离子注入诱变选育灵芝高产菌株的研究[J].药物生物技术, 2011, 18(1):32-37.
[29]刘桂君 ,尚宏忠 ,周 思 静 ,等 . 一 种 离 子 束 注 入 诱 变 选 育 蛹 虫 草 菌 株 的 方 法 和 所 育 菌 株 : CN201510229665.4[P]. 2017-03-29.
[30]赵丽丽,孙小富,黄莉娟,等.辐射诱变突变体鉴定技术[J].贵州大学学报(自然科学版),2020,37(4): 26-29.
[31]Khare V, Gupta S K, Manjaya J G. Exploring differential radiosensitivity in soybean genotypes exposed to gamma rays and determining optimal doses for induced mutagenesis[J]. Applied Radiation and Isotopes, 2025, 220: 111778.
[32]李玉岭,毛欣,张元帅,等.辐射诱变技术在木本植物育种中的应用及展望[J].生物技术通报,2023,39(6): 12-30.
[33]王曼,刘霄,杜艳,等.重离子辐照育种对西蓝花幼苗生长及生理特性的影响[J].辐射研究与辐射工艺学报, 2024, 42(1): 73-86.
[34]袁帅,董志晓,赵煜晗,等.60Co-γ辐射对扁穗雀麦种子萌发及其幼苗生长的影响[J].草业科学,2021,38(7): 1319-1328.
[35]武志江,梁桂东,廖以金,等.碳离子束辐照对火龙果种子萌发、存活率及幼苗生长的影响[J].热带作物学报, 2020, 41(7): 1402-1407.
[36]冯慧,骆善伟,杜艳,等.氩离子束辐照拟南芥干种子的生物学效应[J].辐射研究与辐射工艺学报, 2016,34(1):33-40.
[37]陈晓锋,周利斌,金文杰,等.碳离子束辐照对油葵当代结实特性的影响[J].原子核物理评论,2023, 40(1): 106-112.
[38]他富文,李莲芳,蒙进芳,等.碱溶液浸种对花椒种子发芽的影响[J].西部林业科学,2024,53(4): 29-34.
[39]陆锡宏,石广亮,李雪虎,等.12C6+离子束辐照菘蓝干种子当代效应[J].原子核物理评论,2013,30(4): 477-482.
[40]刘振昌,魏文文.不同剂量 12C6+离子束辐照对苦瓜种子发芽和生物学性状的影响[J].安徽农业科学, 2020, 48(9): 59-61.
[41]管翊君,王浩,吕美澄,等. 电子加速器源射线对小麦根尖染色体及生理特性的影响[J].核农学报, 2023,37(11): 2126-2133.
[42]Amirikhah R, Etemadi N, Sabzalian M R, et al. Gamma radiation negatively impacted seed germination, seedling growth and antioxidant enzymes activities in tall fescue infected with Epichloë endophyte[J]. Ecotoxicology and Environmental Safety, 2021, 216: 112169.
[43]邓本良.活性氧调控作物种子发芽机理的研究进展[J].安徽农业科学, 2020, 48(13): 21-22.
[44]Bailly C. Active oxygen species and antioxidants in seed biology[J]. Seed science research, 2004,14(2): 93-107.
[45]隆静,陈婧敏,刘霄,等.植物 DNA 双链断裂修复机制及其在重离子诱变和基因编辑中的作用[J].生物技术通报, 2024, 40(7): 55-67.
[46]刘青芳,余丽霞,杜艳,等.12C6+离子束辐照对小麦种子萌发、幼苗生长及存活的影响[J].辐射研究与辐射工艺学报, 2013,31(1): 26-30.
[47]彭梦婕,刘丹,牛贺雨,等.60Co-γ辐射对紫薇种子萌发、幼苗生长和生理的影响[J].安徽农业大学学报, 2020, 47(4): 530-537.
[48]姜恒越,高毓翎,李媚晴,等. 60Co-γ射线辐照对粉黛乱子草种子萌发及幼苗生长的影响[J].草地学报, 2022,30(12):3272-3278.
[49]Liu X, Wang M, Wang Y, et al. Carbon ion beam-induced radiation hormesis in Bupleurum chinense DC.: Insights from growth, physiological, and metabolomic analyses for increased bioactive substances[J]. Plant Stress, 2025: 101037.
[50]Kim J H. Radiation hormesis and reactive oxygen species-mediated stress priming in plants[J]. Plant Science, 2025: 112602.
[51]Kikuchi S, Saito Y, Ryuto H, et al. Effects of heavy-ion beams on chromosomes of common wheat, Triticum aestivum[J]. Mutation Research/Fundamental and Molecular Mechanisms of Mutagenesis, 2009, 669(1-2): 63-66.
[52]侯岁稳,钱平平,管利萍,等. 12C6+重离子辐照大葱的细胞学和 RAPD 分析[J].核农学报, 2008(1): 9-13.
[53]朱梅彩,刘子腾,甘沛华,等.不同光质对3 种松树种子萌发及幼苗生长与HY5 基因表达的影响[J].西南林业大学学报(自然科学), 2025, 45(1): 10-17.
[54]冯志杰.高等植物的辐射敏感性[J]. 中国核科技报告, 1992(S3):35-36.
[55]Ghasemi-Soloklui A A, Kordrostami M, Karimi R. Determination of optimum dose based of biological responses of lethal dose (LD25, 50, 75) and growth reduction (GR25, 50, 75) in ‘Yaghouti ’ grape due to gamma radiation[J]. Scientific Reports, 2023, 13: 2713.
[56]Ghasemi-Soloklui A A,Kordrostami M,Jafari M.Determination of optimal gamma radiation dose for mutation breeding in ’Sabz ’ fig (Ficus carica L.) cuttings based on radiosensitivity and phenotypic changes[J]. PLoS One, 2025, 20(1): e0313017.
[57]Gao G, Chen P, Chen J, et al. Genomic survey, transcriptome, and metabolome analysis of Apocynum venetum and Apocynum hendersonii to reveal major flavonoid biosynthesis pathways[J]. Metabolites, 2019, 9(12): 296.
文章摘自:康睿娇,刘泽,杨浩程,周利斌,金文杰,张科,王弋博,邹亚丽,曲颖.碳离子束辐照对新疆两种罗布麻种子萌发和幼苗生长的影响[J/OL].中国麻业科学. https://link.cnki.net/urlid/43.1467.S.20260211.1841.002