摘 要:为探究外源脯氨酸(Proline,Pro)对盐胁迫下红麻幼苗生长及生理响应的调控作用,研究以中红麻21号为材料,在125mmol/L NaCl胁迫条件下设置不同浓度Pro处理(0.05、0.1、0.2、0.4mmol/L),开展红麻幼苗盐胁迫生长与生理特性测定试验。结果表明,与NaCl处理相比,外源Pro能显著缓解盐胁迫对红麻幼苗生长的抑制,具体表现为株高、根长、鲜重、干重及叶绿素相对含量的显著提高。同时,Pro处理显著促进可溶性糖的积累,增强超氧化物歧化酶(SOD)、过氧化物酶(POD)和过氧化氢酶(CAT)活性,降低丙二醛(MDA)含量和相对电导率,有效减轻膜脂过氧化损伤。Pro处理减少了叶片中过氧化氢(H?O?)和超氧阴离子(O?•?)的积累,表明其通过协同调控渗透平衡与抗氧化系统活性,提高了红麻幼苗的耐盐能力。其中,0.2mmol/L Pro处理对盐胁迫的缓解效果最为显著。
关键词:红麻;盐胁迫;脯氨酸;幼苗生长
土壤盐渍化是严重制约全球农业可持续发展和生态安全的重大环境问题[1],也是限制作物生长与产量的主要非生物胁迫之一[2]。据统计,全球受盐渍化影响的土地面积已超过9亿hm2,每年造成的农业经济损失约1900亿元人民币[3]。我国作为受盐渍化影响显著的国家,盐渍土总面积高达3670万hm2,占我国可利用土地面积的4.9%[4]。盐渍土壤中,过量的Na?和Cl?等离子不仅会破坏土壤结构、提高土壤渗透势、阻碍作物对水分的吸收,还会引发离子毒害与次级氧化胁迫,严重干扰植物的正常生理代谢,导致叶片黄化、生长受抑甚至植株死亡[5],从而对国家粮食安全构成严峻威胁。为此,中共中央、国务院在《加快建设农业强国规划(2024—2035年)》中明确将“分区分类开展盐碱耕地治理改良”提升至国家战略层面。我国具备农业开发潜力的盐渍土面积约1300万hm2,接近现有耕地总面积的1/10[6],为保障粮食安全提供了重要的战略后备资源。通过科技创新赋能盐碱地资源高效利用与可持续开发,不仅是拓展农业生产空间、落实“藏粮于技”战略的关键举措,更是全方位夯实国家粮食安全根基的必然要求。
为应对盐胁迫引发的渗透失衡与氧化胁迫双重危害,植物在长期进化过程中形成了以Pro积累为核心的自我保护机制,将其作为关键的相容性溶质参与逆境调节[7]。在盐胁迫条件下,Pro不仅可作为渗透压保护剂维持细胞渗透平衡、稳定蛋白质结构,还能通过增强抗氧化系统活性减轻由活性氧(ROS)过量积累引起的氧化损伤,从而维持细胞的稳态[8-9]。然而,在强盐胁迫环境中,内源Pro的合成与积累常不足以有效缓解渗透胁迫,因此外源Pro的施用被认为是研究植物耐盐机制及提升耐盐性的有效手段之一[3]。已有研究[10-11]表明,外源Pro处理能够显著改善盐胁迫下植物的生长状态,提高光合性能,增强抗氧化酶系统活性,降低过氧化氢和丙二醛积累,减少活性氧损伤,从而有效缓解盐诱导的氧化胁迫并提高植物耐盐性。
红麻(Hibiscus cannabinus L.)隶属于锦葵科(Malvaceae)木槿属(Hibiscus),是一年生重要的纤维型经济作物[12]。该作物具有生长迅速、生物量大、适应性广等特点,对盐碱、干旱及涝渍等多种非生物胁迫表现出较强的耐受能力[13],在盐渍化土地生态修复与综合利用方面具有显著潜力[14]。随着耕地资源日益紧张及粮食安全压力增加,红麻的种植已逐步向盐碱地等边际土地扩展[15]。国家麻类产业技术体系也明确指出,充分挖掘麻类作物在盐碱地、干旱区及重金属污染地等边际土地的生态修复与利用价值,是“十四五”期间的重要研究方向之一。本研究以红麻幼苗为研究对象,通过分析不同浓度外源Pro处理下植株的生长表现及生理响应特征,旨在阐明外源Pro缓解盐胁迫的生理作用机制,为盐碱地改良及红麻在盐渍土资源修复中的应用提供理论依据与技术参考。
1 材料与方法
1.1 试验材料
本试验所用材料为中红麻21号种子,由中国农业科学院麻类研究所南方特色作物遗传育种创新团队提供。Pro购买于上海麦克林生化科技股份有限公司,超氧化物酶试剂盒、过氧化物酶试剂盒、过氧化氢酶试剂盒、丙二醛试剂盒及可溶性糖试剂盒均购自北京索莱宝科技有限公司,DAB染色液和植物超氧阴离子染色液购自南京亿迅生物科技有限公司。花多多水溶肥购自北京荷泰力农业科技有限公司,用作培养营养液。
1.2 试验方法
1.2.1 种子处理与催芽
种子选择与消毒:选取籽粒饱满、无机械损伤的中红麻21号种子,于自来水下冲洗10min。用0.1%次氯酸钠(NaClO)溶液消毒10min,并以无菌蒸馏水冲洗3次,去除残留消毒剂。
催芽:将经消毒的种子均匀点播于铺有湿润滤纸的发芽盒中,放置于恒温光照培养箱内,培养条件为30℃(16h光照/8h黑暗),直至种子萌发。
1.2.2 幼苗培育与处理设计
选取生长整齐、发育一致的幼苗移植至有花多多水溶肥的营养液的水培盆中,在可控温室条件下(25℃,16h光照/8h黑暗)培养至两叶一心期。根据中国农业科学院麻类研究所南方特色作物遗传育种创新团队对该品种的研究结果,中红麻21号幼苗的盐害阈值为125mmol/L[16],因此将该浓度设为红麻盐胁迫浓度。试验设6个处理,分别为CK(不加NaCl、不加Pro)、NaCl(125mmol/L NaCl)、P1(125mmol/L NaCl+0.05mmol/L Pro)、P2(125mmol/L NaCl+0.1mmol/L Pro)、P3(125mmol/L NaCl+0.2mmol/L Pro)、P4(125mmol/L NaCl+0.4mmol/L Pro)。所有处理均以每盆栽植12株幼苗作为1个生物学重复,每个处理共设置3个生物学重复,并每3d更换一次营养液,持续处理15d后取样,测定幼苗的生长指标及各项生理生化参数。
1.3 指标测定与方法
1.3.1 生长指标测定
每个处理随机选取3株红麻幼苗,采用直尺分别测定株高和根长,并称量其鲜重,测定后将样品装入透气纸袋中,置于烘箱内以100℃杀青10min,随后将温度降至50℃,烘干至恒重后称量其干重。1.3.2生理指标测定叶绿素含量采用SPAD-502叶绿素仪测定[17];可溶性糖含量采用蒽酮比色法测定[18];相对电导率按电导仪法测定[19];丙二醛(MDA)含量采用硫代巴比妥酸显色法测定[20];超氧化物歧化酶(SOD)活性采用氮蓝四唑光还原法测定[21];过氧化物酶(POD)活性采用愈创木酚法测定[22];过氧化氢酶(CAT)活性采用过氧化氢分解法测定[23]。所有生理指标均设3次生物学重复。
1.3.3 DAB 与 NBT 染色
为定位分析盐胁迫下红麻叶片中过氧化氢与超氧阴离子的积累分布,本研究分别采用二氨基联苯胺(DAB)和硝基四氮唑蓝(NBT)组织化学染色法进行检测。染色工作液分别为1mg/mL DAB溶液与0.5mg/mL NBT溶液。取样时,分别采集对照组和盐胁迫处理组红麻叶片,清洗表面灰尘后用滤纸吸干。随后将叶片完全浸入对应染色液中,于室温条件下避光反应6h。染色结束后,以无菌蒸馏水漂洗3~5次去除多余染料,再次吸干。随后使用无水乙醇脱色2~3次,直至叶片绿色完全消失。脱色后的样品置于70%乙醇中保存,并使用数码相机拍摄记录染色结果。
1.4 数据分析
采用Microsoft Excel 2021进行数据整理与统计分析,采用Origin 2021进行显著性差异分析及图表绘制,试验影像使用Adobe Photoshop 2019进行处理。
2 结果与分析
2.1 外源Pro对盐胁迫下红麻幼苗生物量的影响
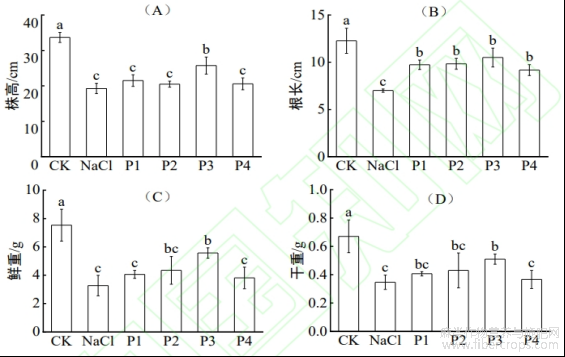
如图1所示,外源Pro处理显著缓解了盐胁迫对红麻幼苗生长的抑制。与单一NaCl处理相比,各浓度Pro处理后的红麻幼苗生长量有所不同,整体呈现先上升后下降趋势,其中以P3效果最为显著。在株高方面,P3处理较NaCl处理提高33.6%,而P1、P2和P4处理分别提高11.6%、6.2%和6.8%,促进作用相对较弱。根长变化趋势与株高相似,P3处理增幅达50.0%,P1、P2和P4处理分别较NaCl处理提高39.0%、40.5%和31.0%。在鲜重方面,P3处理相较于NaCl处理增加70.5%,P2处理和P1处理分别增加32.9%和24.2%,P4处理仅增加16.6%,效果最弱。干重结果亦表现出类似趋势。与NaCl处理相比,CK处理的干重最高,提升93.1%,表明无盐胁迫条件下干物质积累最为充分,P3处理较NaCl处理增加了47.0%,P2处理和P1处理分别增加了23.9%和17.3%,P4处理仅提高5.8%,缓解盐胁迫效果不明显。
图1 盐胁迫下Pro对红麻幼苗生物量的影响
注:不同小写字母表示不同处理之间差异显著(p<0.05)。
2.2 外源Pro对盐胁迫下红麻幼苗叶绿素和可溶性糖含量的影响
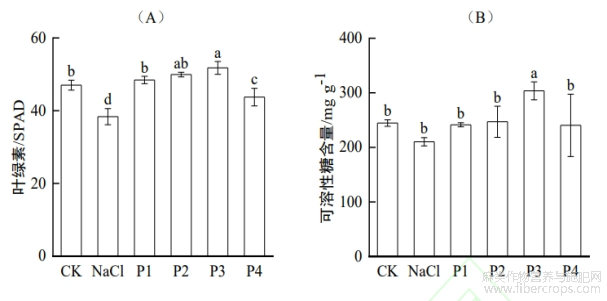
由图2(A)可知,外源Pro处理显著提高了盐胁迫下红麻幼苗叶片的叶绿素相对含量。随着Pro处理浓度的增加,红麻幼苗叶片的SPAD值呈现先升高后降低的变化趋势,其中P3处理效果最为显著,较NaCl处理提高34.9%,P2和P1处理的SPAD值分别较NaCl处理提高了30.1%和26.2%,而P4处理仅提高14.0%,其促进效应明显减弱。
由图2(B)可知,外源Pro处理显著提高了盐胁迫下红麻幼苗叶片中可溶性糖的含量。随着Pro浓度的升高,可溶性糖含量逐渐增加,至P3处理达到最高值,较NaCl处理显著提高44.40%。P1和P2处理分别较NaCl处理提高14.84%和17.45%,而P4处理虽较NaCl处理仍高14.33%,但相比P3处理呈下降趋势。结果表明,适量外源Pro可有效促进红麻幼苗渗透调节物质的积累,从而增强其抗盐胁迫能力。
图2 盐胁迫下Pro对红麻幼苗叶绿素和可溶性糖含量的影响
注:不同小写字母表示不同处理之间差异显著(p<0.05)。
2.3 外源Pro对盐胁迫下红麻幼苗相对电导率和MDA含量的影响
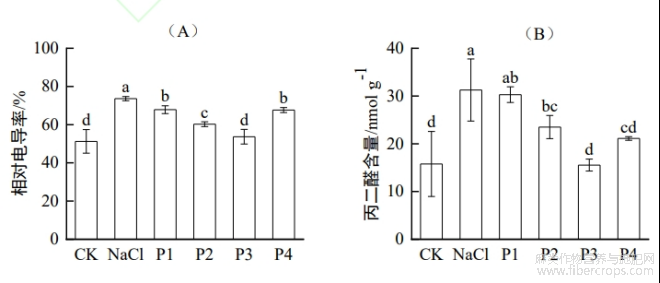
由图3可知,外源Pro处理显著降低了盐胁迫下红麻幼苗的相对电导率和MDA含量。以NaCl处理为参照,CK组的相对电导率和MDA含量分别较NaCl组降低30.3%和49.5%,表明无盐胁迫条件下红麻细胞膜完整性较好,脂质过氧化水平较低。外源Pro处理可不同程度缓解盐胁迫造成的膜系统损伤,其中以P3处理效果最为显著,其相对电导率和MDA含量分别较NaCl处理降低27.0%和50.3%,显示出较强的抗盐能力。P2处理的相对电导率和MDA含量较NaCl处理降低了18.1%和24.8%,表现出一定的缓解作用;P1和P4处理的相对电导率较NaCl处理分别降低了7.9%和8.2%,MDA含量分别降低了3.1%和32.5%,其中P4处理在减轻氧化损伤方面效果优于P1处理。总体来看,P3处理在维持细胞膜完整性和减轻氧化损伤方面表现最为显著,而P1处理的效果相对较弱。
图3 盐胁迫下Pro对红麻幼苗相对电导率和MDA含量的影响
注:不同小写字母表示不同处理之间差异显著(p<0.05)。
2.4 外源Pro对盐胁迫下红麻幼苗抗氧化酶活性的影响
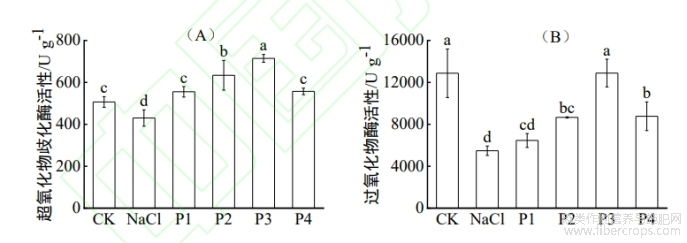
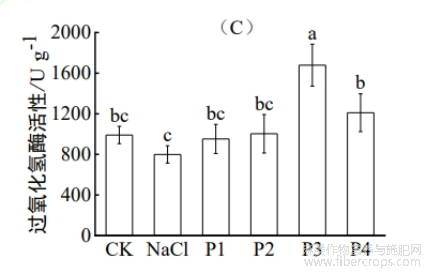
由图4可知,外源Pro处理显著提高了盐胁迫下红麻幼苗的抗氧化防御能力。随着Pro处理浓度的提高,红麻幼苗SOD、POD、CAT酶活性均呈现先升高后降低的变化趋势。与NaCl处理相比,P3处理组的SOD、CAT、POD活性均显著提高,CK处理下SOD和POD活性均显著高于NaCl处理,而CAT活性虽有所升高,但差异未达到显著水平。其中P3处理的SOD活性和CAT活性分别较NaCl处理增加了66.1%和109.9%,POD活性与CK组接近,较NaCl处理增加了135.3%,表明P3处理在增强抗氧化系统活性和清除活性氧方面效果最佳。P2和P4处理的酶活性总体高于NaCl处理,其中P4处理的酶活性水平均显著高于NaCl处理,P2处理的SOD和POD活性显著高于NaCl处理。其中P2处理的SOD和CAT活性分别较NaCl处理增加了47.4%和25.5%,P4处理的POD活性较NaCl处理提高60.0%,显示出一定的抗盐缓解作用。P1处理的抗氧化酶活性提升幅度最小,SOD和CAT活性分别较NaCl处理增加了29.1%和19.1%,POD活性仅提高17.9%,表明其抗盐调控效果相对较弱。总体来看,P3处理在增强抗氧化酶活性方面表现最为突出。
图4 盐胁迫下Pro对红麻幼苗抗氧化酶活性的影响
注:不同小写字母表示不同处理之间差异显著(p<0.05)。
2.5 外源Pro对盐胁迫下红麻幼苗H2O2和O2•?含量的影响
如图5所示,外源Pro处理显著缓解了盐胁迫引发的活性氧过量积累。DAB染色结果显示,与CK组相比,NaCl处理组叶片中棕褐色沉淀显著增多,表明在盐胁迫条件下H?O?大量积累。而施用不同浓度外源Pro后,叶片棕褐色沉淀密度均出现不同程度降低,说明H?O?积累得到有效抑制。其中,P3处理组的染色最浅,表明该浓度处理在降低H?O?含量方面效果最佳。NBT染色结果进一步显示,盐胁迫诱导O?•?的大量生成,NaCl处理组叶片中蓝色甲臜沉淀显著增多,远高于CK组,而经外源Pro处理后,叶片染色程度明显减轻。P1、P2、P4处理组的蓝色沉淀面积介于NaCl组与CK组之间,显示其对O?•?积累具有一定的抑制作用,但效果均低于P3处理。外源Pro可有效减轻盐胁迫下红麻幼苗叶片中过氧化氢和超氧阴离子的异常积累,且以P3浓度处理的缓解效果最为显著。
图5 盐胁迫下 Pro 对红麻幼苗过氧化氢及超氧阴离子含量的影响
3 讨论
3.1 外源Pro对盐胁迫下红麻幼苗生物量的影响
盐胁迫对植物生长的抑制,直观体现为生长迟缓、生物量减少及叶色失绿等表型变化,并进一步干扰正常生理代谢,最终导致作物产量下降与品质劣变[24-25]。生物量作为衡量植物抗逆能力及外源调节物质缓解效果的重要指标,能直观反映胁迫程度与植株恢复水平[26]。已有研究[16]表明,盐胁迫可显著抑制红麻幼苗的生长,其株高、根长、叶面积以及鲜、干重等生长指标随NaCl浓度升高显著下降。本研究结果显示,外源施加Pro能有效缓解盐胁迫对红麻幼苗的生长抑制作用,表现为株高显著增加、根系伸长及干鲜重积累提升,与Pro在盐胁迫下促进芹菜生长的研究结果一致[27]。根系是植物感知与响应盐分胁迫的首要器官,其结构与功能的完整性在决定植株耐盐性中发挥关键作用。Pro作为关键的渗透调节物质,可通过维持根系细胞水势、稳定细胞膜结构并保护根尖分生组织活性,有效减轻盐胁迫对根系生长的不利影响[28-29]。进一步研究[30]表明,外源Pro可通过促进水分吸收、抑制Na?过量积累,从而维持细胞渗透稳态并保障代谢活动的正常进行。本试验中,0.2mmol/L的Pro处理表现出最佳缓解效果,浓度过高或过低均会削弱其生理功能,这可能与植物体内Pro积累存在一定阈值有关,适宜的外源补充可激活其渗透保护与信号调控功能,而过量积累则可能干扰细胞稳态,从而降低其促生效果[8]。
3.2 外源Pro对盐胁迫下红麻幼苗生理特性的影响
叶绿素含量是衡量植物光能利用效率及耐盐能力的重要生理指标[11,31]。本研究结果表明,盐胁迫显著降低了红麻叶片的叶绿素含量,可能源于叶绿素合成受阻或降解速率加快,而外源Pro处理则有效缓解了该下降趋势。由于叶绿素为膜结合色素,其稳定性高度依赖于膜结构完整性,Pro可能通过稳定类囊体膜结构,间接保护叶绿素分子免受盐胁迫破坏,从而减轻其对光合体系的抑制效应[32]。多项研究表明,外源Pro处理能显著改善盐胁迫植物的光合色素含量与气体交换特性。Wani等[33]报道,Pro处理显著提高了盐胁迫下芥菜的净光合速率、气孔导度及光系统II的光化学效率;Nawaz等[34]的研究亦发现,Pro可显著增加高粱叶片的总叶绿素含量,进一步证实了Pro在提高植物耐盐性中的积极作用。
在盐胁迫条件下,外界渗透势的急剧降低会显著抑制植物根系的水分吸收能力[35]。植物通常通过积累渗透调节物质以维持细胞水势平衡和膨压,从而应对胁迫环境[36],可溶性糖作为主要渗透调节物质,不仅可通过降低细胞水势维持细胞伸展,还能为代谢提供能量和碳骨架,并通过羟基结构稳定膜系统、缓解离子毒害[37]。本研究结果显示,盐胁迫显著降低了红麻幼苗的可溶性糖含量,而外源Pro处理可有效逆转这一趋势,使叶片可溶性糖含量维持在较高水平。这表明Pro处理显著增强了红麻幼苗的渗透调节能力,进而提升其耐盐性。鲁克嵩等[8]的研究亦发现,0.5mmol/L外源Pro可显著提高盐胁迫油菜叶片中的可溶性糖含量,与本研究结果一致。
细胞膜系统的完整性是植物耐盐性的关键表征,其损伤程度可通过相对电导率反映。相对电导率越高,表明细胞膜透性增强、结构受损越严重[38]。MDA是膜脂过氧化的典型产物,其积累程度可准确反映氧化胁迫强度。当MDA过度积累时,会破坏膜脂流动性及膜蛋白结构,进而影响膜结合酶及离子通道功能[39]。本研究中,盐胁迫处理显著提高了红麻幼苗的相对电导率和MDA含量,说明其膜系统遭受明显氧化损伤。外源Pro处理则显著降低了上述指标,表明其具有膜保护作用。该结果提示Pro可能通过增强活性氧清除能力来减轻盐胁迫诱导的氧化损伤。陈奋奇等[40]的研究同样表明,Pro可有效降低盐胁迫玉米叶片的相对电导率与MDA含量,进一步验证了其抗氧化保护作用。
在盐胁迫条件下,植物体内活性氧的过量积累可引发氧化胁迫,植物通过形成以SOD、POD和CAT为核心的抗氧化防御系统,协同清除过量ROS,保护细胞膜、蛋白质及核酸免受损伤[41]。其中,SOD是抗氧化防御的第一道屏障,负责催化O?•?歧化生成H?O?和O?;POD与CAT则进一步分解H?O?为水和氧气,从而防止其积累造成细胞伤害[42]。除酶促防御体系外,Pro作为重要的相容性溶质,可直接清除ROS,并在稳定蛋白构象、维持氧化还原平衡中发挥重要作用[43]。本研究结果显示,外源Pro处理显著提高了盐胁迫下红麻幼苗叶片中SOD、POD和CAT的活性,说明Pro能通过增强抗氧化酶系统的协同效能,提升ROS的清除能力,减轻膜脂过氧化,最终增强红麻幼苗的耐盐性。该结果与Mu等[44]在水稻及Wani等[32]在油菜中的研究结论一致,进一步支持了Pro在植物盐胁迫缓解中的积极作用。盐胁迫下Pro含量升高可能与蛋白质水解加快有关[45],外源Pro的施用不仅促进其自身积累,还可能通过转录与翻译水平调控增强抗氧化酶活性[46]。此外,Pro作为膜稳定剂,能够改善水分吸收、维持叶片水势并抑制H?O?积累,从而协同缓解盐胁迫引起的氧化损伤[47]。综上,外源Pro可通过协调酶促与非酶促抗氧化途径,系统提升红麻幼苗的生理稳态与抗逆能力。
3.3 外源Pro缓解盐胁迫并促进红麻幼苗生长的生产应用前景
在红麻生产实践中,外源Pro的应用多通过叶面喷施、根际灌施及营养液补施等方式实施,可有效提高盐碱地幼苗的成活率与抗逆性[43,48]。结合本研究结果,0.2mmol/L Pro在红麻幼苗期表现出最显著的盐胁迫缓解效果,具有较高的可推广性,可作为盐敏感阶段的常规调控措施纳入育苗管理流程[49]。在盐渍化地块生产中,可于移栽前使用Pro叶面喷施,以增强幼苗早期的逆境适应能力;在育苗基质盐分偏高或再生植株更新期,则可通过营养液补施方式维持根系发育与植株稳态。该措施不仅有助于提高苗期管理质量,还有望在红麻规模化生产、耐盐品种选育及盐碱地资源高效利用中发挥潜在应用价值。未来,应在盐碱化地块开展大田验证实验,进一步优化Pro的施用浓度、频次及方法,从而构建适用于盐碱地红麻生产的大规模推广技术体系。
4 结论
本研究表明,外源Pro可显著缓解盐胁迫对红麻幼苗生长与生理特性的抑制作用。具体表现为增加了红麻幼苗的株高、根长、鲜重和干重,提高了叶片中叶绿素相对含量,增加了渗透调节物质可溶性糖含量,提高了抗氧化酶SOD、CAT和POD活性,降低了MDA含量和相对电导率,并减少H?O?和O?•?的积累。不同浓度的Pro处理均在一定程度上改善了红麻幼苗的生理状态,其中以0.2mmol/L处理效果最佳。本研究结果为阐明Pro在红麻耐盐机制中的作用提供了理论依据,并为其在盐渍环境下的高效栽培与生产应用提供了科学参考。
参考文献
[1] Zhou H P, Shi H F, Yang Y Q, et al. Insights into plant salt stress signaling and tolerance[J].Journal of Genetics and Genomics,2024,51(1):16-34.
[2] Van Zelm E, Zhang Y X, Testerink C. Salt tolerance mechanisms of plants[J]. Annual Review of Plant Biology,2020,71:403-433.
[3] Hossain M A, Fujita M. Evidence for a role of exogenous glycinebetaine and proline in antioxidant defense and methylglyoxal detoxification systems in mung bean seedlings under salt stress[J]. Physiology and Molecular Biology of Plants,2010,16(1):19-29.
[4] 杨劲松,姚荣江,王相平,等.中国盐渍土研究:历程?现状与展望[J].土壤学报,2022,59(1):10-27.
[5] 齐琪,马书荣,徐维东,等.盐胁迫对植物生长的影响及耐盐生理机制研究进展[J].分子植物育种,2020,18(8):2741-2746.
[6] 王佳丽,黄贤金,钟太洋,等.盐碱地可持续利用研究综述[J].地理学报,2011,66(5):673-684.
[7] Hernández J A, Olmos E, Corpas F J, et al. Salt-induced oxidativestress in chloroplasts of pea plants[J]. Plant Science,1995,105(2):151-167.
[8] 鲁克嵩,闫磊,侯佳玉,等.盐胁迫下外源脯氨酸对油菜Na+/K+平衡?生长及抗氧化系统的影响[J].华中农业大学学报,2023,42(5):141-148.
[9] Krishnan N, Dickman M B, Becker D F. Proline modulates the intracellular redox environment and protects mammalian cells against oxidative stress[J]. Free Radical Biology and Medicine,2008,44(4): 671-681.
[10] De Freitas P A F, De Carvalho H H, Costa J H, et al. Salt acclimation in sorghum plants by exogenous proline: physiological and biochemical changes and regulation of proline metabolism[J]. PlantCell Reports,2019,38(3):403-416.
[11] 唐依萍,张晓艳,刘士壮,等.外源脯氨酸对NaCl胁迫下番茄幼苗光合特性的影响[J].安徽农业科学,2015,43(24):9-11.
[12] Chen P, Li Z Q, Luo D J, et al. Comparative transcriptomic analysis reveals key genes and pathways in two different cadmium tolerance kenaf (Hibiscus cannabinus L.) cultivars[J]. Chemosphere,2021,263:128211.
[13] Ramesh M. Kenaf (Hibiscus cannabinus L.) fibre based bio-materials: a review on processing and properties[J]. Progress in Materials Science,2016,78/79:1-92.
[14] 熊和平.我国麻类生产的现状与政策建议[J].中国麻业科学,2010,32(6):301-304.
[15] Li H, Li D F, Chen A G, et al. RNA-seq for comparative transcript profiling of kenaf under salinity stress[J]. Journal of Plant Research,2017,130(2):365-372.
[16] 杨大为.NO缓解红麻盐胁迫的功能分析[D].北京:中国农业科学院,2022.
[17] 周倩文,杨瑞芳,王昕慧,等.SPAD-502叶绿素计在苎麻高光效种质筛选上的应用研究[J].现代农业科技,2022(3):40-43.
[18] Buysse J, Merckx R. An improved colorimetric method to quantify sugar content of plant tissue[J]. Journal of Experimental Botany,1993,44(267):1627-1629.
[19] 陈爱葵,韩瑞宏,李东洋,等.植物叶片相对电导率测定方法比较研究[J].广东教育学院学报,2010,30(5):88-91.
[20] 高俊凤.植物生理学实验指导[M].北京:高等教育出版社,2012:210-211.
[21] Clare D A, Darr D, Archibald F, et al. Effects of molecular oxygen on detection of superoxide radical with nitroblue tetrazolium and on activity stains for catalase[J]. Analytical Biochemistry, 1984,140(2):532-537.
[22] 张志良,瞿伟菁,李小方.植物生理学实验指导[M].4版.北京:高等教育出版社,2009:123-124.
[23] 邹琦.植物生理学实验指导[M].北京:中国农业出版社,2003:167-169.
[24] Khalifa G S, Abdelrassoul M, Hegazi A M, et al. Attenuation of negative effects of saline stress in two lettuce cultivars by salicylic acid and Glycine Betaine[J]. Gesunde Pflanzen,2016,68(4):177-189.
[25] Chen Z H, Soltis D E. Evolution of environmental stress responses in plants[J]. Plant, Cell & Environment,2020,43(12):2827-2831.
[26] 贾邱颖,吴晓蕾,冀胜鑫,等.盐胁迫下番茄砧木对嫁接苗生物量?氨基酸含量和活性氧代谢的影响[J].应用生态学报,2020,31(9):3075-3084.
[27] 高彦强.外源脯氨酸对芹菜盐胁迫的缓解效应[D].兰州:甘肃农业大学,2023.
[28] Kavi Kishor P B, Sreenivasulu N. Is proline accumulation per se correlated with stress tolerance or is proline homeostasis a morecritical issue [J]. Plant, Cell & Environment,2014,37(2):300-311.
[29] Verbruggen N, Hermans C. Proline accumulation in plants: a review[J]. Amino Acids,2008,35(4):753-759.
[30] Naliwajski M, Sk?odowska M, Naliwajski M, et al. The relationship between the antioxidant system and proline metabolism in the leavesof cucumber plants acclimated to salt stress[J].Cells,2021, 10(3):609-624.
[31] 王卓沛.外源褪黑素和2,4-表油菜素内酯对无刺蔷薇盐碱胁迫的缓解效应[D].泰安:山东农业大学,2023.
[32] Wani A S, Ahmad A, Hayat S, et al. Is foliar spray of proline sufficient for mitigation of salt stress in Brassica juncea cultivars [J]. Environmental Science and Pollution Research,2016,23(13):13413-13423.
[33] Wani S H, Kumar V, Shriram V, et al. Phytohormones and their metabolic engineering for abiotic stress tolerance in crop plants[J]. The Crop Journal,2016,4(3):162-176.
[34] Nawaz K, Talat A, Iqra K H, et al. Induction of salt tolerance in two cultivars of sorghum (Sorghum bicolor L.) by exogenous application of proline at seedling stage[J]. World Applied Sciences L, 2010, 10: 93-99.
[35] Munns R, Tester M. Mechanisms of salinity tolerance[J]. Annual Review of Plant Biology,2008,59:651-681.
[36] 毛爽,周万里,杨帆,等.植物根系应答盐碱胁迫机理研究进展[J].浙江农业学报,2021,33(10):1991-2000.
[37] Verslues P E, Agarwal M, Katiyar-Agarwal S, et al. Methods and concepts in quantifying resistance to drought, salt and freezing, abiotic stresses that affect plant water status[J]. The Plant Journal,2006,45(4):523-539.
[38] 王京华.外源褪黑素对杜梨耐盐碱能力的影响[D].泰安:山东农业大学,2024.
[39] Shulaev V, Oliver D J. Metabolic and proteomic markers for oxidative stress. New tools for reactive oxygen species research[J]. Plant Physiology,2006,141(2):367-372.
[40] 陈奋奇,方鹏,白明兴,等.外源脯氨酸缓解玉米幼苗盐胁迫的效应[J].草业科学,2022,39(4):747-755.
[41] 雷新慧,万晨茜,陶金才,等.褪黑素与2,4-表油菜素内酯浸种对盐胁迫下荞麦发芽与幼苗生长的促进效应[J].作物学报,2022,48(5):1210-1221.
[42] García-Caparrós P, Defilippis L, GUL A, et al. Oxidative stress and antioxidant metabolism under adverse environmental conditions: a review [J]. The Botanical Review,2021,87(4):421-466.
[43] Elmoukhtari A, Cabassa-Hourton C, Farissi M, et al. How does proline treatment promote salt stress tolerance during crop plant development[J]. Frontiers in plant science,2020,11:1127.
[44] Mu D W, Feng N J, Zheng D F, et al. Physiological mechanism of exogenous brassinolide alleviating salt stress injury in rice seedlings[J]. Scientific Reports,2022,12:20439.
[45] Kiyosue T, Yoshiba Y, Yamaguchi-Shinozaki K, et al. A nuclear gene encoding mitochondrial proline dehydrogenase, an enzyme involved in proline metabolism, is upregulated by proline but downregulated by dehydration in Arabidopsis[J].The Plant Cell,1996,8(8):1323-1335.
[46] Cuin T A, Shabala S. Compatible solutes reduce ROS-induced potassium efflux in Arabidopsis roots[J].Plant, Cell & Environment,2007,30(7):875-885.
[47] Islam M M, Hoque M A, Okuma E, et al. Exogenous proline and glycinebetaine increase antioxidant enzyme activities and confer tolerance to cadmium stress in cultured tobacco cells[J].Journal of Plant Physiology,2009,166(15):1587-1597.
[48] Nounjan N, Theerakulpisut P. Effects of exogenous proline and trehalose on physiological responses in rice seedlings during salt-stress and after recovery[J]. Plant, Soil and Environment,2012,58(7):309-315.
[49] 董合忠.滨海盐碱地棉花成苗的原理与技术[J].应用生态学报,2012,23(2):566-572.
文章摘自:苏雨娟,钟海龙,唐慧娟,栾明宝,李建军,邓勇,黄思齐.外源脯氨酸对盐胁迫下中红麻21号幼苗的缓解效应[J].中国麻业科学.https://link.cnki.net/urlid/43.1467.s.20260211.1849.006。