摘 要:为探讨亚麻饼粕蛋白质与亚麻籽多酚通过碱法形成共复物的特性及抗氧化性能,采用碱溶酸沉法制备纯度为86.60%的亚麻饼粕蛋白,并通过碱法共价共轭制备亚麻饼粕蛋白质与亚麻籽多酚共复物,研究其结构表征、功能特性和抗氧化活性。结果表明,通过傅里叶变换红外光谱和凝胶电泳证实形成共复物,表现为酰胺A带、酰胺I带和酰胺II带最大吸收波长发生红移或蓝移,共复物分子质量主要分布在50~70ku,并出现新条带。多酚与蛋白共价化合后,酪氨酸和脯氨酸含量上升,其它氨基酸含量呈不同程度的下降,特别是亲核的赖氨酸和蛋氨酸的消耗显著(P<0.05)。此外,亚麻饼粕蛋白-多酚共复物的抗氧化性能较单一蛋白得到显著提升,DPPH和ABTS自由基清除率均显著高于单一蛋白(P<0.05),10mg/mL质量浓度下分别为95.68%和91.246%。这表明亚麻饼粕蛋白质与亚麻籽多酚的共复物通过影响蛋白结构与性能,提高其抗氧化性能,研究结果为这一天然复合物的应用提供了理论参考。
关键词:亚麻饼粕蛋白;亚麻籽多酚;共复物;蛋白表征;抗氧化性
亚麻(俗称胡麻)主要分布于我国西北、华北地区,为当地的重要植物油原料来源[1]。亚麻饼粕是亚麻籽经溶剂浸出法或压榨法制成油后生成的副产物。在亚麻籽食用油生产过程中会产生大量的亚麻饼粕,通常少部分作为动物饲料或直接废弃,未能得到高效利用。大量研究表明,亚麻饼粕是非常好的氨基酸、蛋白质、酚类等生物活性物质的低成本来源,先前的报道从亚麻饼粕中检出17种氨基酸,包括7种必需氨基酸和10种非必需氨基酸[2]。亚麻饼粕分离蛋白具有良好的乳化性、起泡性和泡沫稳定性等性质。Karami等[3]的研究表明,亚麻饼粕中含有丰富的蛋白质和多酚类化合物,利用亚麻饼粕提取物开发新的生物活性化合物,在抗糖尿病、抗氧化、降压、抗炎和抗癌等方面可能发挥重要的生物学作用。Kotecka-Majchrzak等[4]分析发现亚麻饼粕蛋白中释放的许多肽具有生物活性,即ACE抑制活性、抗氧化活性、抗炎、抗菌、降血糖或心脏保护作用。此外,亚麻饼粕中还含有丰富的木质素、尼古酸、泛酸和核黄素[5-6]。值得注意的是,亚麻饼粕还具有较高的微量元素含量优势。何生虎等[7]研究发现亚麻饼粕含钙元素和磷元素较多,植酸磷的含量占总磷的50%以上,铁元素、锌元素含量均高于豆饼,铜元素、硒元素含量高于豆饼、棉籽饼、菜籽饼。然而,目前亚麻饼粕尚未得到有效利用,以其所含蛋白质和多酚为原料的深加工产品有限。
蛋白质具有乳化、发泡、凝胶、低毒性和生物相容性,并且蛋白质表面具有多种功能基团,使其能与多种物质相互作用,从而促进疏水和亲水生物活性分子的传递[8]。多酚类化合物是植物体内重要的次生代谢产物,具有显著的抗氧化和抗菌特性,然而其性质不稳定,易受降解过程影响,溶解性差,导致生物利用度相对较低[9]。将蛋白质与多酚类化合物复合能够有效改善单一蛋白质和多酚类化合物的功能特性,从而扩大其应用领域[10]。蛋白质和多酚类化合物作用机制主要分为可逆相互作用和不可逆相互作用,可逆相互作用主要涉及范德华力、疏水键和氢键等非共价键,虽具有低能量、不稳定的特点,但在自然界中普遍存在[11]。不可逆相互作用涉及共价键和离子键,其中蛋白质和多酚类化合物的共价结合方法主要有3种,分别为碱法、自由基接枝法和酶法,经不可逆相互作用形成的共价键产物作用力强且很稳定[12],其中最常见的是碱法,是制备具有生物活性高的蛋白质-多酚共复物的有效合成方法。
本研究以亚麻饼粕为试验材料,将提取的亚麻饼粕蛋白(FPP)及其多酚类化合物(FPI)经碱法共价结合形成共复物(FPI-FPP),分析其结构、功能特性和抗氧化性,以期为亚麻饼粕深加工利用提供理论参考。
1 材料与方法
1.1 材料与试剂
亚麻饼粕,购于宁夏固原市;亚麻饼蛋白、亚麻饼蛋白-多酚复合物,由实验室制备;亚麻籽油,购于新百超市。
1,1-二苯基-三硝基肼(DPPH)、2,2-联氮双(3-乙基苯并噻唑啉-6-磺酸)(ABTS)、牛血清白蛋白,上海麦克林生化科技有限公司;叠氮化钠(分析纯级),上海伊恩化学技术有限公司;凝胶电泳试剂盒,武汉金开瑞生物工程有限公司;溴化钾(光谱纯级)、十二烷基硫酸钠(SDS),上海阿拉丁生化科技股份有限公司;透析袋(8ku分子质量),宁夏世纪国康化学试剂有限公司;PBS缓冲液(分析纯级),武汉普诺赛生命科技有限公司;其它试剂(未特殊标明)均为国产分析纯级。
1.2 仪器与设备
DF-110S集热式磁力搅拌器,杭州旌斐仪器科技有限公司;FD-1A-50真空冷冻干燥机,北京博医康仪器有限公司;DYCZ-25E凝胶电泳仪,济南欧莱博科学仪器有限公司;T6紫外-可见光分光光度计,北京普析通用仪器有限责任公司;K1100凯氏定氮仪,上海沛欧分析仪器有限公司;SZF-06A脂肪测定仪,济南阿尔瓦仪器有限公司;SX2-LT马弗炉,郑州安晟电炉公司;XD-5205旋转蒸发仪,广州沪瑞明仪器;L8900全自动氨基酸分析仪,北京普析通用仪器有限责任公司;Vertex70傅里叶变换红外光谱仪,美国Bruker光学公司;S-4800扫描电子显微镜(SEM),日本日立;Litesizer™500纳米粒度及Zeta电位分析仪,安东帕(上海)商贸有限公司;ThetaFlow接触角分析仪,瑞典百欧林;高速剪切均质机(FSH-2A),上海一科仪器有限公司。
1.3 方法
1.3.1 亚麻饼粕蛋白质-多酚共复物的形成及结构表征
1.3.1.1 亚麻饼蛋白-多酚共复物的制备
参考Pham等[13]的方法并稍作修改,将FPP与FPI共价加合,羟基酪醇(HT)作为阳性对照。将FPI和酚类化合物(FPP和HT)分别分散在去离子水中,以所需的比例混合,并将混合物的pH值调至9.0。在室温下加入0.02%的叠氮化钠做抑菌剂,在氧气存在的条件下800r/min搅拌共轭24h。将反应后的混合物与水透析20h除去未反应的多酚化合物和盐离子,将未加入酚类化合物的原生蛋白同样进行上述操作。在真空冷冻干燥,得到FPI-FPP共复物粉末。
1.3.1.2 亚麻饼粕-多酚共复物主要成分的测定
水分含量参考《食品安全国家标准食品中水分的测定》(GB 5009.3—2016)中的方法进行测定;灰分含量参考《食品安全国家标准食品中灰分的测定》(GB 5009.4—2016)中的方法进行测定;蛋白质含量参考《食品安全国家标准食品中蛋白质的测定》(GB 5009.5—2016)中的方法进行测定;粗纤维含量参考《植物类食品中粗纤维的测定方法》(GB/T 5009.10—2003)中的方法进行测定;脂肪含量参考《食品安全国家标准食品中脂肪的测定》(GB 5009.6—2016)中的方法进行测定。
1.3.1.3 亚麻饼粕-多酚共复物总酚含量的测定
将亚麻饼粕粉末按体积比1:6与正己烷混合脱脂12h,离心(3000r/min,20min)后取沉淀物在40℃下热风干燥,得到脱脂亚麻饼粕粉样品。准确称取样品3g,加入60%乙醇溶液,封口,超声,抽滤,收集提取液。取30mL提取液,加入10mL 1mol/L的氢氧化钠(NaOH)溶液,将提取液中NaOH浓度调整至0.25mol/L,反应2h。反应结束后,向烧杯中加入1mol/L的盐酸调节pH值至4.0。用0.45μm滤膜过滤,滤液减压浓缩后,加入30mL60%乙醇溶液复溶,使用比色法测定总酚含量。取0.3mL提取后的总酚复溶,然后加入1mL 1mol/L福林酚试剂,涡旋混合反应1min,再加入3mL 7.5%碳酸钠溶液振摇,加入70%乙醇溶液至10mL,于45℃水浴中反应1.5h.以不加标准溶液为空白对照,在波长765nm处测定吸光值,通过标准曲线计算样品中的总酚含量。以质量浓度分别为0,10,20,30,40,50μg/mL的没食子酸标准溶液,制作标准曲线。
1.3.1.4 亚麻饼粕蛋白质-多酚共复物氨基酸分析
采用全自动氨基酸分析仪测定水解产物的氨基酸含量。在进样之前对样品进行简单的前处理,然后用滤膜过滤,用外标法测定样品溶液中游离氨基酸含量,其脯氨酸检测波长为440nm,其它氨基酸检测波长为570nm,上机测试。
1.3.1.5 傅里叶变换红外光谱
亚麻饼粕蛋白-多酚复合物粉末使用KBr压片法[14]测定。将粉末样品和KBr粉末按1∶100的比例称取,于玛瑙研钵中研磨,在干燥室内按照标准程序压片并上机测定。所有的测量数据都在400~4000cm-1之间采集,每个样品扫描16次。
1.3.1.6 聚丙烯酰胺凝胶电泳
参考Yan等[15]的方法将冻干蛋白质溶解在样品缓冲液中,配制成10mg/mL的样品溶液。使用Tris-甘氨酸缓冲液(pH2.3)在10%电泳缓冲液中以10mA凝胶进行电泳迁移6h。用0.1%考马斯亮蓝对凝胶的蛋白质分子进行染色,然后用脱色溶液洗涤后得到带有不同分子质量条带的凝胶。
1.3.1.7 扫描电镜(SEM)
通过扫描电镜(SEM)观察对照亚麻饼粕蛋白、亚麻饼粕蛋白-多酚复合物以及阳性对照的形貌特征。将适量的冻干样品安装在铜导电粘合剂上,并去除多余的样品。在离子溅射仪吸尘后将样品涂上金然后上机测试。
1.3.1.8 溶解度、ζ-电位和粒径
参考Boyes等[16]的方法,将蛋白质分散到1%PBS缓冲液中,调节pH值为3,4,5,6,7,8,9并搅拌30min,12000r/min下离心15min。用定量考马斯亮蓝测定法测定上清液中蛋白质质量浓度,并使用牛血清白蛋白作为标准品分别配制20,40,60,80,100μg/mL的标准溶液,绘制标准曲线。
根据参考文献[17]的方法并稍作修改来测量蛋白质的粒径、ζ电位。分析前用去离子水稀释样品,避免多重散射效应。测量温度为25℃,平衡时间设置为60s,使用纳米粒度及Zeta电位分析仪平行测定3次计算平均值。
1.3.1.9 接触角
根据参考文献[18]的方法对每种粉状固体产品的接触角进行测量。在干净的载破片上加1%的分散体(蒸馏水中的样品)制备每个样品的薄膜,65℃下干燥10min,在薄膜表面滴加一滴去离子水沉积,测定水滴和颗粒薄膜之间的接触角,需测定3滴,计算平均值。
1.3.2 功能特性
1.3.2.1 乳化性
乳化活性指数(EAI)和乳化稳定性指数(ESI)通过比浊法测定[19]。将150mL样品分散在30mL 0.1mol/L的磷酸盐缓冲液(pH7.0)中,与10mL亚麻籽油混合,将混合物在20000r/min的转速下均质1min,形成乳剂。取100μL均质化0min和10min的乳液,用9.9mL的0.1%十二烷基硫酸钠(SDS)稀释,在波长500nm处测量稀释后乳液的吸光度。EAI和ESI按照式(1)和(2)计算。

式中:A0为稀释后的乳液在均质化后0min的吸光度;c为乳液形成前水相中每单位体积蛋白质的质量,g/mL;Φ为乳液的油相体积分数,%;At是0~10min之间的吸光度变化;t为时间间隔,10min;D为乳状液的稀释倍数。
1.3.2.2 发泡性
乳液发泡性能按参考文献[20]中的方法,在2℃下表征样品的发泡性能。使用高剪切混合器对15mL的测试溶液进行机械剪切(10000r/min,90s)以产生泡沫.然后使用以下公式(3)和(4)计算每个测试样品的起泡性(FC)和泡沫稳定性(FS)。

式中:V为剪切前测试样品的体积,15mL;V0为剪切后出现的泡沫体积,mL;Vt为剪切后60min的泡沫体积,mL。
1.3.3 抗氧化性能
DPPH自由基清除率的测定参考文献[21]中的方法,并做修改。配制2×10-4mol/L的DPPH乙醇溶液。分别吸取2mL质量浓度为0.2,0.4,0.6,0.8,1.0mg/mL的样品溶液于试管中,加入2mLDPPH乙醇溶液,振荡混匀后避光反应30min,置于波长517nm处,以蒸馏水参比,分别测定吸光度值。按照公式(5)计算样品DPPH自由基清除能力:
![]()
式中:A1是样品中加入DPPH的吸光度;A2是样品中加入无水乙醇的吸光度。
ABTS清除率的测定参考文献[22]的方法并稍作修改。将7mmol/LABTS和2.45mmol/L过硫酸钾溶液等比例混合,避光在室温下反应12~16h,然后用无水乙醇稀释,使波长734nm处的吸光度值为0.7±0.02(用无水乙醇调整至零)以获得ABTS工作溶液。吸取3.9mL ABTS工作液于试管中,分别加入0.1mL质量浓度为0.2,0.4,0.6,0.8,1.0mg/mL的样品溶液,振荡后静置6min,于波长734nm处测得吸光度值。根据公式(6)计算样品ABTS清除能力:
![]()
式中:A4为样品中加入ABTS的吸光度;A3为蒸馏水加入ABTS的吸光度。
1.4 数据统计与分析
试验数据均采用Origin 2022分析与绘图,差异性分析使用SPSS分析,通过单因素方差(One-wayANOVA)分析中的Kruskal-Wallis法及邓肯式多重比较(Duncan's multiple comparisons test)检验组间差异显著性,P<0.05表示差异显著。本试验各指标均重复测定3次,结果以平均值±标准差表示。
2 结果与分析
2.1 亚麻饼粕蛋白质-多酚共复物的形成及结构表征
2.1.1 亚麻饼粕-多酚共复物主要成分
亚麻饼粕蛋白质-多酚共复物总酚含量测定标准曲线如图1,回归方程为Y=0.0057X+0.0114,R²=0.9913。

图1 亚麻饼粕蛋白质-多酚共复物总酚含量测定标准曲线
亚麻饼粕、亚麻籽胶、亚麻饼蛋白的主要成分含量测定结果如表1所示。
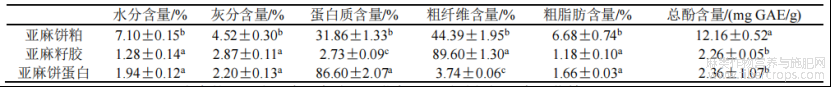
表1 基本理化指标
注:表中的不同小写字母代表同一指标不同试验组间具有显著差异,P<0.05。
由表1可知,亚麻饼粕中粗纤维和蛋白质含量占比较高,分别为44.39%和31.86%,其它组分水分、灰分、粗脂肪、总酚含量分别为7.10%,4.52%,6.68%和12.16%,这与齐文良[23]的研究相符。亚麻饼蛋白中蛋白质含量为86.60%,粗纤维含量为3.74%,这可能是由于pH值从9.0附近降低到蛋白质的等电点过程中,酸性氨基酸的侧链(如天冬氨酸或谷氨酸)质子化,潜在促进正电荷部分(-NH3+)与去质子化的半乳糖醛酸(—COO)相互作用,生成可溶性复合物,进而导致亚麻饼蛋白的蛋白质提取率降低。与此同时,pH值接近或超过亚麻籽蛋白的等电点并进一步向酸性区域移动时,来自亚麻饼粕的蛋白质表面电荷由负转正。此时,在阴离子黏液存在下,两者发生电荷中和作用,最终形成蛋白质-黏液共沉淀[24]。
2.1.2 亚麻饼粕蛋白质-多酚共复物的酚类物质含量
空白亚麻饼蛋白(FPI)、蛋白-多酚复合物(FPI-FPP)以及亚麻饼蛋白-羟基酪醇(FPI-HT)的多酚含量如图2所示。

图2 亚麻饼粕蛋白质-多酚共复物多酚物质含量
注:图中的不同小写字母代表同一指标不同试验组间具有显著差异,P<0.05。
由图2可知,FPI-HT中酚类物质含量最高,为111.31mg GAE/g,FPI-FPP中酚类物质含量为92.56mg GAE/g,FPI中酚类物质含量显著低于二者,为23.61mg GAE/g。这可能是因为碱性条件下,蛋白质与酚类物质反应的主要途径是不可逆共价相互作用[25],酚类物质在碱性条件下被氧化为醌,醌类化合物与蛋白质侧链中含有氨基或巯基的亲核基团发生加成或席夫碱反应,形成C—S或C—N键。由于单位质量的HT中具有较多羟基的结构,可以通过氢键、疏水作用力与蛋白质反应,而氢键、疏水相互作用、离子键为可逆共价相互作用,因此在FPI-HT中可以检测到更高含量的酚类物质。
2.1.3 亚麻饼粕蛋白质-多酚共复物氨基酸分析
制备蛋白质-多酚共复物后,对其氨基酸组成进行分析,FPI、FPI-HT、FPI-FPP的氨基酸组成如表2所示。
表2 亚麻饼粕蛋白质-多酚共复物氨基酸组成

蛋白质与多酚类化合物的共价相互作用,是指多酚在酶或氧气氧化的过程中产生中间产物醌,其中多数为亲核残基的半醌自由基,它们可以与蛋白质侧链上的氨基酸(如蛋氨酸、赖氨酸)相互作用[26]。若多酚被部分氧化,其产物邻醌可与蛋白质中的氨基酸残基发生反应,主要涉及半胱氨酸的硫醇基团、赖氨酸的ε-氨基以及其它氨基酸的α-氨基,进而形成共复合物。由表2可知,FPI-FPP的氨基酸中,酪氨酸和脯氨酸的含量均高于空白组FPI,分别为35.35mg/g和34.15mg/g,并且FPI-HT中这2种氨基酸含量最高的,分别为38.66mg/g和35.50mg/g,其它试验组氨基酸的含量相较于空白组均有降低,这与Bashir等[27]的研究结果一致,多酚类化合物与氨基酸的α-氨基基团结合形成复合物的描述相符,说明经过试验,这些氨基酸均有不同程度的消耗,因此含量下降,同时说明所做试验使蛋白质和多酚类化合物发生了共价作用。经过分析发现,FPI-HT中有些关键氨基酸含量高于FPI-FPP,由此证明2.1.2节中HT通过其它化学键与蛋白质结合的可能性。
2.1.4 亚麻饼粕蛋白质-多酚共复物傅里叶变换红外光谱
对FPI、FPI-HT、FPI-FPP进行傅里叶变换红外光谱扫描,通过检查特征光谱峰的强度和位置来提供蛋白质的结构变化和相互作用的信息,探究空白组与试验组中蛋白质与多酚类化合物的结构变化和相互作用。

图3 傅里叶变换红外光谱图
由图3可知,空白组FPI的特征峰包括酰胺I带、酰胺II带以及酰胺A带。酰胺A带的差异主要源自于多酚类化合物中O—H和蛋白质中N—H的共振拉伸。与FPI相比,FPI-FPP和FPI-HT的酰胺A带峰形相似,FPI的吸收峰位于3292cm-1,而FPI-FPP和FPI-HT则分别蓝移至3286cm-1和3281cm-1,表明多酚类化合物与FPI发生了共价结合。FPI的酰胺I带吸收峰约在1650cm-1,而FPI-FPP和FPI-HT则分别红移至1657cm-1和1653cm-1。FPI的酰胺II带吸收峰约在1536cm-1,而FPI-FPP
和FPI-HT则分别红移至1538cm-1和1539cm-1,这表明FPI的二级结构发生了变化[24]。高峰出现在3392cm-1左右,可以归因于酚羟基的O—H拉伸。
2.1.5 亚麻饼粕蛋白质-多酚共复物聚丙烯酰胺凝胶电泳
如图4所示为聚丙烯酰胺凝胶电泳分析FPI和共复物FPI-FPP、FPI-HT的分子质量谱。在15ku以下几乎无条带,这是因为低于14ku的蛋白质条带与白蛋白成分有关,通常pH值高于5.0时表达明显。共复物FPI-FPP、FPI-HT在大约10~50ku的范围内显示出极大的相似性,并且条带主要分布在50~70ku范围内,证明多酚修饰可能未显著改变核心蛋白亚基的分子质量,而在70ku出现了FPI没有的条带,说明共复物中蛋白质和多酚类化合物之间适当络合,这与Guo等[28]的研究相符。

图4 聚丙烯酰胺凝胶电泳
2.1.6 亚麻饼粕蛋白质-多酚共复物扫描电镜
如图5所示为FPI,配合物FPI-FPP、FPI-HT的SEM图(放大倍数分别为500×、2000×),利用微观结构图可确认FPI以及其多酚类物质配合物。如图所示,对照组FPI的SEM图中显示出大量明显的颗粒状结构,呈较为完整的球形,在2000倍下可以观察到大体积的蛋白是由小颗粒状的蛋白结块构成。与FPI相比,共复物FPI-FPP、FPI-HT的蛋白结构更为完整光滑并且无小形颗粒物,这可能是由于蛋白质和多酚类物质之间的共价作用形成二元共价复合物所引起的,这也与聚丙烯酰胺凝胶电泳中二者出现大分子质量条带一致。共复物FPI-FPP、FPI-HT表面平整、均匀,而FPI的块状结构疏松,表面虽平整但呈现出多孔状,这可能是蛋白质链的展开导致层状结构的紊乱。

注:(a)FPI;(b)FPI-FPP;(c)FPI-HT。
注:左侧图的放大倍数为500×,右侧图的放大倍数为2000×。
图5 亚麻饼粕蛋白质-多酚共复物的微观结构
2.1.7 溶解度、ζ-电位和粒径
亚麻饼粕蛋白质-多酚共复物蛋白质质量浓度标准曲线如图6所示,回归方程为Y=0.0051X+0.0275,R²=0.9908。亚麻饼蛋白及其蛋白-多酚复合物的溶解度以上清液蛋白质浓度占总蛋白质浓度的百分比表示。

图6 亚麻饼粕蛋白质-多酚共复物蛋白质质量浓度标准曲线
溶解度是决定蛋白质乳化性质的重要因素。图7为FPI、共复物FPI-FPP、FPI-HT的溶解度,FPI在pH4.0和8.0附近时具有相对较高的溶解度,而在5.0附近时溶解度最低,为12.516μg/mL,共复物FPI-FPP和FPI-HT同样在pH5.0时溶解度最低,分别为11.764μg/mL和13.039μg/mL,此现象的原因是该值接近FPI的等电点,这与图8中蛋白质的电位数据所得出的等电点基本一致。由图8可知,当pH值从4.0提升至5.0时,FPI的电位从6.93mV变为-15.5096mV,并且FPI的电位绝对值始终高于共复物FPI-FPP和FPI-HT。
蛋白质与极性多酚类化合物共价键和,溶解度的变化可能是由于酚羟基的加入,改变了蛋白质的电荷性质[29]。因此,FPI与多酚类化合物偶联在一定程度上改变了溶解度,在pH5.0~9.0范围较高,而在pH2.0~4.0范围较低。可以推断,非共价相互作用对FPI的溶解度有轻微影响,在某些情况下,蛋白质的亲水区域可能会被阻断,考虑到蛋白质在等电点附近的溶解度最低,等电点的偏移可能解释了溶解度增加的原因,共复物FPI-FPP、FPI-HT的溶解度有轻微差异,可能是因为共复物中游离氨基减少,蛋白质的等电点降低。
如图7所示,共复物FPI-HT的溶解度增加是由HT络合引起的FPI构象变化的积分效应所引起,FPI的疏水基团在于HT反应时被阻断,来自HT的亲水基团(如羟基)被引入蛋白质链[30]。如图9所示,FPI、共复物FPI-FPP、FPI-HT体积占比加权平均粒径为422.882,830.073nm和1169.495nm。FPI-HT的粒径最大且分布最为分散,这是因为蛋白质与多酚类化合物结合导致分子质量增大。

图7 亚麻饼粕蛋白质-多酚共复物溶解度

图8 亚麻饼粕蛋白质-多酚共复物不同pH值下的电位

图9 亚麻饼粕蛋白质-多酚共复物的粒径分布
2.1.8 接触角
接触角大小在一定程度上可以反映蛋白质的表面疏水性,接触角越大蛋白质表面疏水性越好。如图10所示为亚麻饼粕蛋白质和共复物的接触角结果,三者表面接触角均<65°,说明亚麻饼粕蛋白及其共复物均呈亲水性;其中FPI-HT的表面接触角为58.8°,FPI-FPP的表面接触角为55.5°,FPI的表面接触角为51.2°,表明蛋白质与多酚物质的共价作用增强了蛋白质的疏水性。

注:(a)FPI;(b)FPI-FPP;(c)FPI-HT。
图10 亚麻饼粕蛋白质-多酚共复物的接触角
2.2 乳化性、发泡性
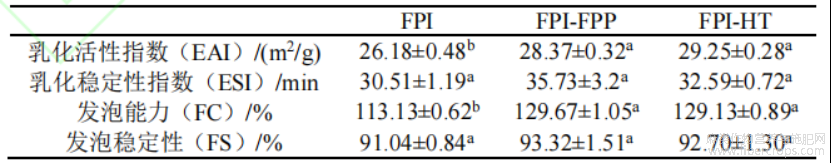
FPI、共复物FPI-FPP、FPI-HT的EAI和ESI值如表3所示。FPI的EAI、ESI值分别为26.18m2/g和30.51min,与之相比共复物的均有所提高但差异不显著,FPI-FPP的EAI和ESI值最高,分别为28.37m2/g和35.73min,这表明共复物乳液的乳化活性和稳定性增强。
由表可知,共复物的FC值显著提高,FS值也有所提升但差异并不显著,FPI-FPP的FC和FS值最高为129.67%和93.32%,这表明泡沫的形成及其稳定性可以随着共价作用而提高。
表3 亚麻饼粕蛋白质-多酚共复物的乳化性和发泡性
注:表中的不同小写字母代表同一指标不同试验组间具有显著差异,P<0.05。
2.3 亚麻饼粕蛋白质-多酚共复物自由基清除率
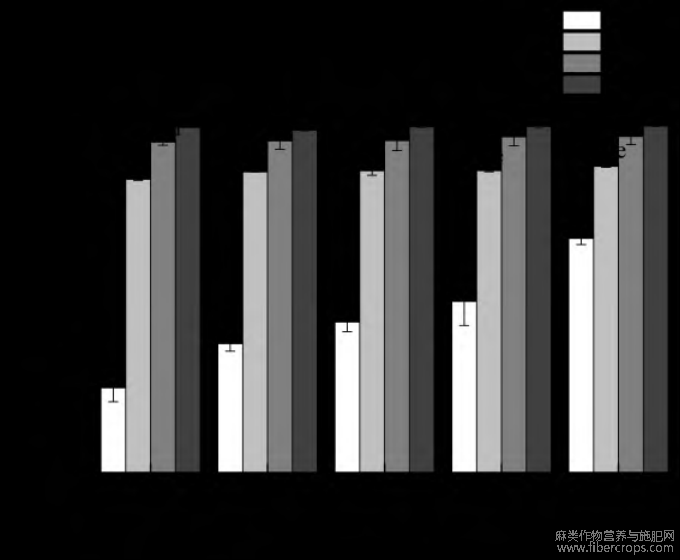
如图11所示,不同质量浓度下DPPH自由基清除率(VC为阳性对照),可知,FPI的自由基清除率随质量浓度的增加而上升,质量浓度为2mg/mL时自由基清除率为23.41%;质量浓度为10mg/mL时自由基清除率为64.69%。FPI、FPI-FPP、FPI-HT的自由基清除率全部低于对照组,而配合物FPI-FPP、FPI-HT的自由基清除率均显著高于FPI,且随质量浓度的升高无显著变化,同时FPI-FPP与FP-HT的DPPH自由基清除率在试验质量浓度范围内无显著差异,FPI-FPP表现出较高的自由基清除能力,清除率最高可达95.68%,表明FPI与FPP的共复物能够清除自由基,形成更稳定产物,从而终止自由基链式反应。因此,亚麻饼粕蛋白质-多酚共复物可增强抗氧化能力,以此可提高其相关产品的氧化稳定性。
图11 亚麻饼粕蛋白质-多酚共复物的DPPH自由基清除率
注:图中的不同小写字母代表同一指标不同试验组间具有显著差异,P<0.05。
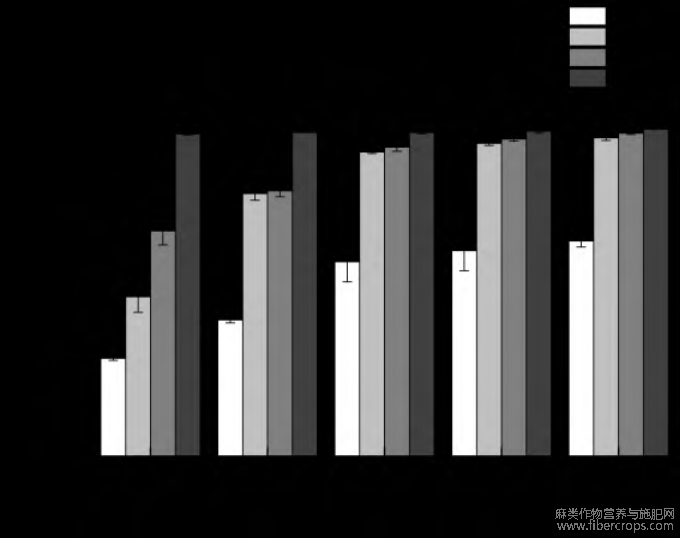
图12 亚麻饼粕蛋白质-多酚共复物的ABTS清除率
注:图中的不同小写字母代表同一指标不同试验组间具有显著差异,P<0.05。
复合物的ABTS结果趋势与DPPH基本一致,如图12所示。在试验质量浓度范围内FPI的ABTS清除率呈显著上升趋势,质量浓度为2mg/mL时清除率最低为27.99%,质量浓度为10mg/mL时清除率最高为61.5%,显著低于FPI-FPP和FPI-HT组。FPI-FPP和FPI-HT的ABTS清除率在2mg/mL的质量浓度下清除率最低,分别为45.55%和64.38%,在10mg/mL的质量浓度下清除率最高,分别为90.99%和92.32%;与DPPH自由基清除率不同的是,FPI-FPP和FPI-HT的ABTS清除率在2~6mg/mL范围内呈显著上升趋势,这表明蛋白质与多酚类化合物的共价作用可以显著提高蛋白质的ABTS清除率,这可能是因为大多数多酚类物质在芳环上有2个相邻的羟基,并且在共价物形成过程中整个多酚分子没有破坏,第2环上的羟基可能仍然在游离,并具有抗氧化活性[31],这与2.1.2节亚麻饼粕蛋白质-多酚配合物的酚类物质含量中分析多酚含量的推测相符。
3 结论
本研究通过碱法共价共轭制备亚麻饼粕蛋白质与亚麻籽多酚共复物(FPI-FPP)。FPI-FPP中酚类物质含量高达92.56mgGAE/g,且各氨基酸含量相较于FPI均有所降低,初步证实共价作用。傅里叶变换红外光谱分析显示,FPI-FPP和FPI-HT的酰胺A带发生蓝移,酰胺I带和酰胺II带发生红移,表明其结构发生了明显变化。聚丙烯酰胺凝胶电泳结果则揭示了FPI-FPP与FPI-HT在分子质量分布上的相似性,而二者在70ku出现了FPI所没有的条带,这进一步证明了共价作用的发生及共复物的形成,扫描电子显微镜观察显示,共价作用对蛋白质的微观结构产生了显著影响,使得FPI-FPP和FPI-HT表现出更为平整、均匀且疏松的表面结构,并呈现出多孔状特征,研究还发现FPI-FPP在pH5.0附近的溶解度最低,而与FPI相比,其溶解度仍保持在一定水平。粒径分析显示,FPI-FPP的体积占比加权平均粒径增大,分布趋于分散,表面接触角测量结果表明,FPI-FPP具有更高的蛋白质疏水性;功能特性方面,FPI-FPP具有最高的EAI和ESI值,分别为28.37m2/g和35.73min,这表明配合物乳液的乳化活性和稳定性增强,FPI-FPP的FC和FS值也显著提高,表明其泡沫能力和泡沫稳定性得到了增强;抗氧化性能方面,FPI-FPP的DPPH和ABTS清除率均显著高于FPI(P<0.05),在10mg/mL质量浓度下分别达到95.68%和91.25%,表明其抗氧化性能得到了显著提高。综上所述,本研究从亚麻饼粕蛋白质与亚麻籽多酚共复物出发,深入探究了共复物的结构、功能特性及抗氧化性能。研究结果不仅为蛋白质与多酚的应用提供了新的思路和方法,同时也为亚麻饼粕分离物的有效利用及其生物利用率的提高提供了重要的科学依据,有助于减少资源浪费并推动相关产业的可持续发展。
参考文献:
[1]吕蕾,曹凤.亚麻籽粕综合利用的初步研究[J].农产品加工,2022(15):87-91.
LÜ L;CAO F.Preliminary study on comprehensive utilization of flaxseed meal[J].Farm Products Processing,2022(15):87-91.
[2]金丽娜,李琳,郭佩佩,等.不同压榨方式对亚麻籽饼粕营养成分及结构的影响[J].食品与发酵工业,2023,49(24):
164-169.
JIN L N,LI L,GUO P P,et al.Effects of different pressing methods on nutrients and structure of flaxseed meal[J].Food and Fermentation Industry,2023,49(24):164-169.
[3]KARAMI Z,AKBARI-ADERGANI B,DUANGMAL K.Recent development on recovering bioactive peptides and phenolic compounds from under-utilised by-products during production of certain edible oil plants: Current situation and future perspectives[J]. International Journal of Food Science & Technology,2022,57(8):4894-4905.
[4]KOTECKA-MAJCHRZAK K,SUMARA A,FORNAL E,et al.Oilseed proteins-Properties and application as a food ingredient[J].Trends in Food Science & Technology,2020,106(1):160-170.
[5]SURI K,SINGH B,KAUR A,et al.Influence of microwave roasting on chemical composition,oxidative stability and fatty acid c omposition of flaxseed (Linum usitatissimum L.)oil[J].Food Chemistry,2020,326(1):126974.
[6]李燕平,牛晓艳,曹亮,等.胡麻饼在畜禽生产中的应用情况[J].中国养兔杂志,2021(1):30-33.
LI Y P,NIU X Y,CAO L,et al.Application of caraway cake in livestock and poultry production[J].China Rabbit Journal,2021(1):30-33.
[7]何生虎,王明成.胡麻饼(粕)的营养学与毒理学研究进展[J].宁夏农学院学报,2004(2):76-79.
HE S H, WANG M C.Progress of nutritional and toxicological studies on caraway cake[J].Journal of Ningxia Agricultural College,2004(2):76-79.
[8]TEIMOURI S,KASAPIS K,DOKOUHAKI M.Diffusional characteristics of food proteinbased materials as nutraceutical delivery systems:A review[J].Trends in Food Science & Technology,2022,122(1):201-210.
[9]MILINCIC D D,POPOVIC D A,LEVIC S M,et al.Application of polyphenol-loaded nanoparticles in food industry[J].Nanomaterials (Basel),2019,9(11):1-21.
[10]杨慧,曲也直,高雅然,等.植物多酚-蛋白质复合物生物活性及应用研究进展[J].食品科学,2022,43(3):258-266.
YANG H,QU Y Z,GAO Y R,et al.Progress of biological activity and application of plant polyphenol-protein complexes[J].Food Science,2022,43(3):258-266.
[11]王远利,康心蕊,陶亮,等.蛋白质与多酚的互作机制及其应用[J].中国食品学报,2024,24(2):357-372.
WANG Y L,KANG X R,TAO L,et al.Interaction mechanism between proteins and polyphenols and its application[J].Journal of Chinese Institute of Food Science and Technology,2024,24(2):357-372.
[12]赵钜阳,袁惠萍,孙昕萌.蛋白质-多酚复合物的形成机制及其功能性变化研究进展[J].食品工业科技,2022,43(8):416-425.
ZHAO J Y,YUAN H P,SUN X-M.Progress in the study of the formation mechanism of protein-polyphenol complexes and their functional changes[J].Food Industry Science and Technology,2022,43(8):416-425.
[13]PHAM L B,WANG B,ZISU B,et al.Covalent modification of flaxseed protein isolate by phenolic compounds and the structure and functional properties of the adducts[J].Food Chemistry,2019,293:463-471.
[14]ZHAO J,CUI J K,CHEN R X,et al.Real-time in-situ quantification of protein secondary structures in aqueous solution based on ATR-FTIR subtraction spectrum[J].Biochemical Engineering Journal,2021,176:108225.
[15]YAN S,XIE F,ZHANG S,et al.Effects of soybean protein isolate polyphenol conjugate formation on the protein structure and emulsifying properties:Protein polyphenol emulsification performance in the presence of chitosan[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2021,609:125641.
[16]BOYES S,STRÜBI P,DAWES H.Measurement of protein content in fruit juices,wine and plant extracts in the presence of endogenous organic compounds[J].LWT-Food Science and Technology,1997,30(8):778-785.
[17]SUN J,LIU W Y,FENG M Q,et al.Characterization of olive oil emulsions stabilized by flaxseed gum[J].Journal of Food Engineering,2019,247:74-79.
[18]CÉSAR B D,WANDERSLEBEN T,OLIVOS M,et al.Food-grade Pickering stabilizers obtained from a protein-rich lupin cultivar(AluProt-CGNA):Chemical characterization and emulsifying properties[J].Food Hydrocolloids,2019,87(1):847-857.
[19]PEARCE K N,KINSELLA J E.Emulsifying properties of proteins:Evaluation of a turbidimetric technique[J].Food Hydrocolloids,1978,26(3):716-723.
[20]CHEN X,CHEN Y,ZOU L Q,et al.Plant-based nanoparticles prepared from proteins and phospholipids consisting of a core-multilayer-shell structure:Fabrication,stability,and foamabilit[J].Agricultural and Food Chemistry,2019,67(1):6574-6584.
[21]GU L P,SU Y J.Protection of beta-carotene from chemical degradation in emulsion-based delivery systems using antioxidant interfacial complexes:Catechin-egg white protein conjugates[J].Food Research International,2017,96(1):84-93.
[22]TLAIS A, TROSSOLO E, TONINI S,et al. Fermented whey ewe’s milk-based fruit smoothies:Bio-recycling and enrichment of phenolic compounds and improvement of protein digestibility and antioxidant activity[J].Antioxdants,2023,1091(12):2-19.
[23]齐文良.胡麻饼粕微生物脱毒工业化生产技术研究[D].太原:山西农业大学,2019.
QI W L.Research on industrialized production technology of microbial detoxification of huisache cake meal[D].Taiyuan:Shanxi Agricultural University,2019.
[24]JIANG L,LIU Y,LI L,et al.Covalent conjugates of anthocyanins to soy protein:Unravelling their structure features and in vitro gastrointestinal digestion fate[J].Food Research International,2019,120(1):603-609.
[25]HELLEBOIS T,FORTUIN J,GAIANI C,et al.Impact of flaxseed gums on the colloidal changes and in vitro digestibility of milk proteins[J].Foods,2022,11(24):4096.
[26]黄丹泥,夏义苗,陈复生,等.蛋白/多酚复合物的形成机制、影响因素及研究方法进展[J].食品科技,2024,49(9):266-275.
HUANG D N,XIA Y M,CHEN F S,et al.Advances in the formation mechanism,influencing factors and research methods of protein/polyphenol complexes[J].Food Science and Technology,2024,49(9):266-275.
[27]BASHIR M A,WEI J,WANG H,et al.Recent advances in catalytic oxidative reactions of phenols and naphthalenols[J].Organic Chemistry Frontiers,2022,9(19):5395-5413.
[28]GUO Y,BAO Y,SUN K,et al.Effects of covalent interactions and gel characteristics on soy protein-tannic acid conjugates prepared under alkaline conditions[J].Food Hydrocolloids,2021,112:106293.
[29]KE C,LIU B,DUDU O E,et al.Modification of structural and functional characteristics of casein treated with quercetin via two interaction modes:Covalent and non-covalent interactions[J].Food Hydrocolloids,2023,137:108394.
[30]JAKOBEK L.Interactions of polyphenols with carbohydrates,lipids and proteins[J].Food Chemistry,2015,175(1):556-567.
[31]QUAN T H,BENJAKUL S,SAE-LEAW T,et al.Protein–polyphenol conjugates:Antioxidant property,functionalities and their applications[J].Trends in Food Science & Technology,2019,91(1):507-517.
文章摘自:张雨婷,唐新,刘敦华,王小雅,杨龙,金万红.亚麻饼粕蛋白质-多酚共复物的特性及抗氧化性能[J/OL].中国食品学报.https://link.cnki.net/urlid/11.4528.TS.20260130.1616.006