摘 要:目的 研究汉麻Cannabis sativa根部的化学成分。方法 采用硅胶柱色谱及HPLC等色谱技术进行分离纯化,通过理化性质与波谱数据分析鉴定化合物的结构。结果 从汉麻根甲醇提取液正己烷和醋酸乙酯萃取物中分离得到17个化合物,分别鉴定为(7S,8E)-3-羟基-1,3,5,8,10-没药烷五烯-9,12-内脂(1)、木栓酮(2)、β-谷甾醇(3)、齐墩果酸(4)、苯甲酸(5)、对羟基苯甲醛(6)、香草醛(7)、对羟基苯甲酸(8)、香草酸(9)、2α-羟基齐墩果酸(10)、顺式阿魏酸酰对羟基苯乙胺(11)、反式阿魏酸酰对羟基苯乙胺(12)、N-反式对羟基肉桂酰基对羟基苯乙胺(13)、2,5-二叔丁基苯酚(14)、(E)-N-(2-hydroxy-2-(4-hydroxyphenyl)ethyl)-3-(4-hydroxyphenyl)acrylamide(15)、(S)-N-[2-hydroxy-2-(4-hydroxyphenyl)ethyl]-3-(4-hydroxy-3-methoxyphenyl)acrylamide(16)、9S,12S,13S-三羟基-10E,15Z-十八碳二烯酸(17)。结论化合物1为新化合物,命名为汉麻根素;化合物4~9、11~14、16、17为首次从汉麻根中分离得到。化合物10、15为首次从该属植物中分离得到。
关键词:汉麻;汉麻根素;酪酰胺;2α-羟基齐墩果酸;顺式阿魏酸酰对羟基苯乙胺
汉麻Cannabis sativa L.为桑科(Moraceae)大 麻属Cannabis L.植物,其四氢大麻酚质量分数低于0.3%,又被称作工业大麻[1],在纺织[2]、食品[3]、医药[4]等领域具有广泛应用。汉麻根在中医学里俗称麻根,在我国拥有悠久的药用历史,《肘后备急方》[5]记载:“麻根十枚、水五升,煮取二升,一服,可治淋下血”,《中华本草》[6]记载:“取麻根9~15g煎汤或捣汁内服便可祛瘀活血”。近年来国内外学者对汉麻进行了广泛的研究,但对其根部化学成分及药理作用研究相对较为缺乏,对其化学成分的报道主要为三萜类和甾醇类[7]。为进一步开发利用汉麻资源,本研究对汉麻根甲醇提取液正己烷和醋酸乙酯萃取物的化学成分进行了研究,从中分离得到17个化合物,分别鉴定为汉麻根素(cannabisnoid,1)、木栓酮(friedelin,2)、β-谷甾醇(β-sitosterol,3)、齐墩果酸(oleanolic acid,4)、苯甲酸(benzoic acid, 5)、对羟基苯甲醛(p-hydroxybenzaldehyde,6)、香草醛(vanillin,7)、对羟基苯甲酸(p-hydroxybenzaldehyde,8)、香草酸(vanillic acid,9)、2α-羟基齐墩果酸(2α-hydroxy-oleanolic acid,10)、顺式阿魏酸酰对羟基苯乙胺[N-(cis-teruloyl) tyramine,11]、反式阿魏酸酰对羟基苯乙胺[N-(trans-teruloyl) tyramine,12]、N-反式对羟基肉桂酰基对羟基苯乙胺[N-(trans-p-coumaroyl) tyramine,13]、2,5-二叔丁基苯酚(2,5-di-tert-butylphenol,14)、(E)-N-(2-hydroxy-2-(4-hydroxyphenyl) ethyl)-3-(4-hydroxyphenyl)-acrylamide(15)、(S)-N-[2-hydroxy-2-(4-hydroxyphenyl)-ethyl]-3-(4-hydroxy3-methoxyphenyl)-acrylamide(16)、9S,12S,13S-三羟 基-10E,15Z-十八碳二烯酸(9S,12S,13S-trihydroxy10,15-octadecadienoic acid,17)。其中化合物 1 为新 化合物,命名为汉麻根素,化合物4~9、11~14、16、17为首次从汉麻根中分离得到。化合物10、15为首次从该属植物中分离得到。
1 材料与仪器
X-6型显微熔点测定仪(北京泰克仪器有限公司);BrukerAV-600型核磁共振波谱仪(瑞士Bruker公司,TMS为内标);Xevo Q-TOF型质谱仪(美国Waters公司);Lamda 35型紫外可见分光光度计(美国PE公司);Magna FTIR-750 型傅里叶变换红外光 谱仪(美国Nicolet公司);圆二色谱仪(J-1500 CD光谱仪,日本分光株式会社);半制备高压液相色谱 仪(日本日立公司,LC-6AD 泵,Shodex RI SE-61视差折光检测器);PREP-SIL(250 mm×10 mm,5 mm)及 PREP-ODS(250 mm×10 mm,5 μm)不锈钢色谱柱;柱色谱用硅胶(200~300目)为青岛海洋化工厂产品;薄层色谱硅胶板为烟台化工厂生产。有机溶剂为国药集团上海试剂厂产品,其他试剂为分析纯。
汉麻根于2020年11月3日采自黑龙江省昶丰生物科技有限公司,室内阴干,经大兴安岭金亿顺汉麻种植专业合作社刘祥忠高级农艺师鉴定为汉麻 C. sativa L.的根部。标本(CSL-20201103)收藏于 齐齐哈尔大学天然产物研究室。
2 提取与分离
干燥的汉麻根4.7kg,切碎,用甲醇室温浸泡提取3d后滤过,重复3次,合并浸提液,浓缩至小体积,加水混悬,依次用正己烷、醋酸乙酯各萃取5次,合并相同溶剂萃取液,浓缩至恒定质量,得到汉麻根正己烷萃取物52.2g、醋酸乙酯萃取物57.5g。
取汉麻根正己烷萃取物12.5g,用硅胶柱色谱分离,依次用正己烷-醋酸乙酯(9∶1,5.0L;7∶3,4.0L;5∶5,4.0L)、醋酸乙酯(2.0L)、甲醇(2.0L)洗脱,经TLC检测合并、浓缩,得到11个组分(FH-1~FH-11)。FH-3(800.0mg)利用硅胶柱色谱分离,用正己烷-醋酸乙酯(9∶1,0.8L;6∶4,0.5L),醋酸乙酯(0.5L)依次洗脱,经TLC检测合并、浓缩,得到9个组分(FH-3-1~FH-3-9)。FH-3-3(59.4mg)用甲醇重结晶,得化合物2(3.0mg)。FH-7(1.5g)经硅胶柱色谱分离,再用正相高效液相色谱分离[正己烷-醋酸乙酯(85∶15),4.0mL/min]得化合物3(12.5mg,tR=18.1min)。FH-8(0.5g)用甲醇重结晶,得化合物4(3.0mg)。
取汉麻根醋酸乙酯萃取物30.0g,用硅胶柱色谱进行分离,依次用正己烷-醋酸乙酯(5∶5,7.0L;2∶8,6.0L)、醋酸乙酯-甲醇(9∶1,6.0L;5∶5,4.0L)、甲醇(3.0L)洗脱,经TLC检测合并、浓缩,得到8个组分(FE-1~FE-8)。FE-2(247.7mg)采用硅胶柱色谱分离,依次用正己烷-醋酸乙酯(9∶1,1.0L),醋酸乙酯(0.2L)洗脱,经TLC检测合并、浓缩,得到3个组分(FE-2-1~FE-2-3)。FE-2-1(163.4mg)经正相高效液相色谱分离[正己烷-醋酸乙酯(95∶5),4.0mL/min]得化合物5(1.4mg,tR=23.6min)。FE-2-2(95.1mg)经正相高效液相色谱分离[正己烷-醋酸乙酯(9∶1),4.0mL/min]得化合物1(1.0mg,tR=30.5min)。FE-2-3(19.5mg)经正相高效液相色谱分离[正己烷-醋酸乙酯(9∶1),4.0mL/min]得化合物6(1.3mg,tR=34.0min)。FE-3(467.0mg)经硅胶柱色谱分离,得到3个组分(FE-3-1~FE-3-3)。FE-3-1(227.4mg)经正相高效液相色谱分离[正己烷-醋酸乙酯(8∶2),4.0mL/min]得化合物7(1.4mg,tR=14.8min)。FE-3-2(391.2mg)经正相高效液相色谱分离[正己烷-醋酸乙酯(8∶2),4.0mL/min]得化合物8(3.3mg,tR=18.9min),FE-3-3(61.5mg)经正相高效液相色谱分离[正己烷-醋酸乙酯(8∶2),4.0mL/min]得化合物9(7.8mg,tR=24.3min)。FE-4(654.3mg)用甲醇重结晶,得到化合物10(18.0mg)。FE-6(2.4g)经硅胶柱色谱分离得到6个组分(FE-6-1~FE-6-6)。FE-6-3(990.3mg)经反相高效液相色谱分离[甲醇-水(4∶6),4.0mL/min]得化合物11(2.0mg,tR=26.5min)、12(34.7mg,tR=54.5min)。FH-6-4(280.9mg)经反相高效液相色谱分离[甲醇-水(5∶5),4.0mL/min]得化合物13(18.0mg,tR=17.5min)。FE-7(1.9g)经硅胶柱色谱分离得到8个组分(FE-7-1~FE-7-8)。FH-7-1(131.6mg)经反相高效液相色谱分离(甲醇,4.0mL/min)得化合物14(5.9mg,tR=13.8min)。FE-7-4(980.0mg)经反相高效液相色谱分离[甲醇-水(3∶7),4.0mL/min]得化合物15(7.0mg,tR=20.0min)、16(6.9mg,tR=25.1min)。FE-7-6(160.0mg)经反相高效液相色谱分离[甲醇-水(7∶3),4.0mL/min]得化合物17(1.4mg,tR=11.0min)。
3 结构鉴定
化合物1:无色脂状物;HR-ESI-MS m/z:243.1024[M-H]−给出分子式为C15H6O3(计算值243.1021);UVλMeOH max(nm):277(0.7);IRνKBr max(cm−1):3439,2924,2860,1743,1620,1588,1455,1073,879,807。1H-NMR谱(表1)中,δ6.77(1H,dd,J=7.6,1.2Hz),7.06(1H,d,J=7.6Hz),6.71(1H,brs)给出3个芳香氢,根据峰型及偶合常数判断其可能为典型的ABX系统质子信号,δ2.21(3H,s)和1.99(3H,s)给出2个与不饱和碳相连的甲基,δ1.42(3H,d,J=7.0Hz)给出1个双峰甲基;13C-NMR谱(表1)中,给出15个碳,其中δ171.1可能为1个酯羰基,δ153.9,146.8,143.7,138.0,131.2,129.5,121.9,119.1,118.6和113.6给出10个不饱和碳,δ21.1,36.1,15.3和10.6给出4个饱和碳,预示可能含有1个苯环及2个双键,推测可能为1个高度不饱和的倍半萜。
表1 化合物 1 的核磁共振波谱数据 (600/150 MHz, CDCl3)
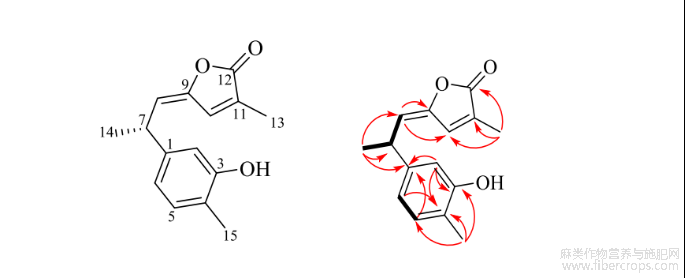
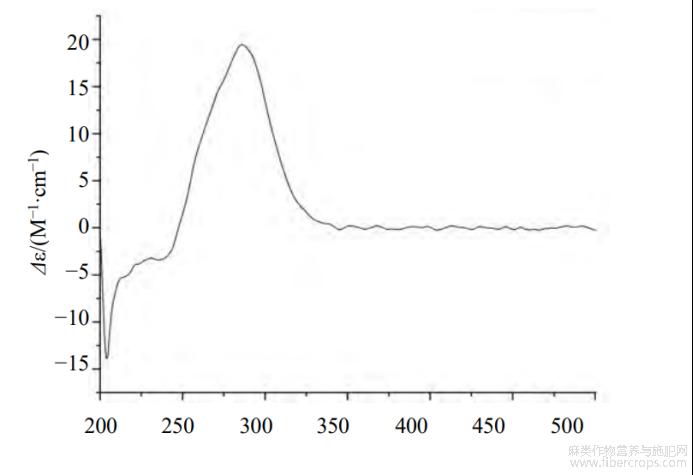
由HMBC谱可知,H-2(δ6.71)与C-1(δ143.7),C-3(δ153.9),C-4(δ121.9)相关,H-5(δ7.06)与C-15(δ15.3)相关,H-7(δ4.11)与C-14(δ21.1)相关,H-8(δ5.22)与C-9(δ146.8),C-10(δ138.0),C-14(δ21.1)相关,H-10(δ5.22)与C-8(δ119.1),C-13(δ10.6)相关,预示含有1个五元内酯环,H-13(δ1.99)与C-10(δ138.0),C-11(δ129.5),C-12(δ171.1)相关,H-14(δ1.42)与C-1(δ143.7),C-7(δ36.1),C-8(δ119.1)相关,H-15(δ2.21)与C-3(δ153.9),C-4(δ121.9),C-5(δ131.2)相关,表明1个甲基与苯环相连;由1H-1H COSY谱可知,H-5(δ7.06)与H-6(δ6.77)相关,H-8(δ5.22)与H-7(δ4.11)相关,H-7(δ4.11)与H-14(δ1.42)相关,由此推得化合物1的平面结构(图1);对化合物1进行ECD光谱测试,其在280nm处表现为正Cotton效应(图2),结合文献报道[8],判断C-7为S构型;并由NOESY可知,H-10(δ6.96)与H-14(δ1.42)具有相关性,判断C8-C9为E构型;经检索,该化合物为未见报道的新化合物,命名为汉麻根素。
图1 化合物1主要的HMBC(H→C)和1H-1H COSY相关
图2 化合物1的ECD图
化合物2:白色片状结晶(甲醇);HR-ESI-MS m/z:427.3940 [M+H]+;mp 265.1~267.6℃;1H-NMR(600MHz,CDCl3)δ:2.38(1H,m,H-2a),2.30(1H,dd,J=13.4,7.2Hz,H-2b),2.24(1H,m,H-4),1.18(3H,s,H-28),1.05(3H,s,H-27),1.01(3H,s,H-26),1.00(3H,s,H-29),0.95(3H,s,H-23),0.88(3H,s,H-30),0.87(3H,s,H-25),0.73(3H,s,H-24);13C-NMR(150MHz,CDCl3)δ:213.3(C-3),59.5(C-10),58.2(C-4),53.1(C-8),42.8(C-18),42.2(C-5),41.6(C-2),41.3(C-6),39.7(C-13),39.3(C-22),38.3(C-14),37.5(C-9),35.6(C-11),36.0(C-16),35.4(C-19),35.0(C-30),32.8(C-15),32.4(C-21),32.1(C-28),31.8(C-29),30.5(C-12),30.0(C-17),28.2(C-20),22.3(C-1),20.3(C-26),18.7(C-27),18.3(C-7),18.0(C-25),14.7(C-24),6.8(C-23)。以上数据与文献报道基本一致[9],故鉴定化合物2为木栓酮。
化合物3:白色针状结晶(氯仿);HR-ESI-MS m/z:437.3759[M+Na]+;mp 135.1~136.2℃;薄层喷硫酸-乙醇溶液加热显紫红色,不同的薄层展开剂展开,与β-谷甾醇对照品比较,其Rf值基本一致,混合后熔点不下降,故鉴定化合物3为β-谷甾醇。
化合物4:白色粉末;HR-ESI-MS m/z:457.3676 [M+H]+;mp 259.3~263.3℃;1H-NMR(600MHz,CDCl3)δ:3.22(1H,dd,J=11.4,4.2Hz,H-3),1.25(3H,s,H-27),1.13(3H,s,H-25),0.99(3H,s,H-29),0.93(3H,s,H-30),0.91(3H,s,H-24),0.77(3H,s,H-23),0.76(3H,s,H-26);13C-NMR(150MHz,CDCl3)δ:183.4(C-28),143.6(C-13),122.6(C-12),79.0(C-3),55.2(C-5),47.6(C-9),46.5(C-17),45.9(C-19),41.6(C-14),40.9(C-18),39.3(C-8),38.7(C-4),38.4(C-1),37.1(C-10),33.8(C-21),33.1(C-29),32.6(C-2),32.4(C-22),30.7(C-20),28.1(C-23),27.7(C-15),27.2(C-2),25.9(C-27),23.6(C-16),23.4(C-30),22.9(C-11),18.3(C-6),17.1(C-26),15.5(C-24),15.3(C-25)。以上数据与文献报道基本一致[10],故鉴定化合物4为齐墩果酸。
化合物5:无色片状结晶(醋酸乙酯);HR-ESI-MS m/z:123.0441 [M+H]+;mp 122.2~123.4℃;1H-NMR(600MHz,CDCl3)δ:8.12(2H,d,J=8.0Hz,H-2,6),7.62(1H,t,J=7.4Hz,H-4),7.49(2H,t,J=7.8Hz,H-3,5);13C-NMR(150MHz,CDCl3)δ:171.9(C-7),133.7(C-4),130.1(C-1),129.2(C-2,6),128.5(C-3,5)。以上数据与文献报道基本一致[11],故鉴定化合物5为苯甲酸。
化合物6:无色针状结晶(甲醇);HR-ESI-MS m/z:123.0441 [M+H]+;mp 110.5~114.3℃;1H-NMR(600MHz,CDCl3)δ:9.58(1H,s,H-7),7.82(2H,d,J=8.6Hz,H-3,5),6.97(2H,d,J=8.6Hz,H-2,6);13C-NMR(150MHz,CDCl3)δ:190.7(C-7),161.0(C-4),132.4(C-2,6),128.9(C-1),115.9(C-3,5)。以上数据与文献报道基本一致[12],故鉴定化合物6为对羟基苯甲醛。
化合物7:无色油状物;HR-ESI-MS m/z:153.0546 [M+H]+;1H-NMR(600MHz,CDCl3)δ:9.82(1H,s,H-7),7.43(1H,s,H-2),7.44(1H,d,J=7.2Hz,H-5),7.05(1H,d,J=8.2Hz,H-6),3.97(3H,s,-OCH3);13C-NMR(150MHz,CDCl3)δ:191.0(C-7),151.7(C-3),147.1(C-4),129.9(C-1),127.6(C-2),114.4(C-5),108.7(C-6),56.1(C-OCH3)。以上数据与文献报道基本一致[13],故鉴定化合物7为香草醛。
化合物8:白色片状结晶(甲醇);HR-ESI-MS m/z:137.0231[M-H]−;mp 210.3~212.4℃;1H-NMR(600MHz,CDCl3)δ:7.79(2H,d,J=8.6Hz,H-2,6),6.82(2H,d,J=8.6Hz,H-3,5);13C-NMR(150MHz,CDCl3)δ:167.6(C-7),162.0(C-4),132.0(C-2,6),121.8(C-1),115.6(C-3,5)。以上数据与文献报道基本一致[14],故鉴定化合物8为对羟基苯甲酸。
化合物9:白色针状晶体(甲醇);HR-ESI-MS m/z:167.0339[M-H]−;mp 210.5~212.2℃;1H-NMR(600MHz,DMSO-d6))δ:7.45(2H,m,H-5,6),6.84(1H,d,J=7.8Hz,H-7),3.80(3H,s,-OCH3);13C-NMR(150MHz,DMSO-d6))δ:167.7(C-7),151.5(C-4),147.7(C-3),123.9(C-6),122.1(C-1),115.5(C-5),113.2(C-2),56.0(C-8)。以上数据与文献报道基本一致[15],故鉴定化合物9为香草酸。
化合物10:白色粉末;HR-ESI-MS m/z:473.3625 [M+H]+;mp 242.5~244.3℃;1H-NMR(600MHz,DMSO-d6))δ:5.17(1H,s,H-12),3.33(1H,s,H-3),2.74(1H,m,H-18),1.09(3H,s,H-27),0.92(6H,s,H-23,24),0.88(6H,s,H-25,26),0.70(3H,s,H-29,30);13C-NMR(150MHz,DMSO-d6))δ:179.1(C-28),144.4(C-13),121.9(C-12),82.7(C-3),67.6(C-2),55.2(C-5),47.5(C-9),47.3(C-1),46.1(C-19),45.9(C-17),41.8(C-14),41.2(C-18),40.0(C-8),39.4(C-4),38.1(C-10),33.9(C-21),33.3(C-7),32.8(C-29),32.6(C-22),30.9(C-23),29.3(C-20),26.1(C-27),27.6(C-15),23.8(C-16),23.5(C-30),23.0(C-11),18.5(C-6),17.6(C-24),17.3(C-26),16.8(C-25)。以上数据与文献[16]基本一致,鉴定为2α-羟基齐墩果酸。
化合物11:无色脂状物;HR-ESI-MS m/z:314.1387 [M+H]+;1H-NMR(600MHz,DMSO-d6))δ:9.29(1H,brs,7-OH),9.17(1H,brs,OH-6′),8.11(1H,brs,N-H),7.70(1H,s,H-5),7.09(1H,d,J=8.2Hz,H-9),6.99(2H,d,J=7.4Hz,H-4′,8′),6.71(1H,d,J=8.2Hz,H-8),6.67(2H,d,J=7.4Hz,H-5′,7′),6.49(1H,d,J=13.4Hz,H-3),5.77(1H,d,J=13.4Hz,H-2),3.74(3H,s,-OCH3),3.26(2H,m,H-1′),2.62(2H,t,J=7.4Hz,H-2′);13C-NMR(150MHz,DMSO-d6))δ:166.7(C-1),156.1(C-6′),147.8(C-7),147.3(C-6),137.3(C-3),130.0(C-3′),129.9(C-4′,8′),127.3(C-4),124.8(C-9),121.5(C-2),115.6(C-5′,7′),115.3(C-8),114.7(C-5),55.9(-OCH3),41.4(C-1′),34.7(C-2′)。以上数据与文献报道基本一致[17],故鉴定化合物11为顺式阿魏酸酰对羟基苯乙胺。
化合物12:白色粉末;HR-ESI-MS m/z:314.1387 [M+H]+;mp 81.4~83.5℃;1H-NMR(600MHz,DMSO-d6))δ:7.30(1H,d,J=15.6Hz,H-3),7.11(1H,s,H-5),7.01(2H,d,J=7.6Hz,H-4′,8′),6.98(1H,d,J=8.0Hz,H-9),6.78(1H,d,J=8.0Hz,H-8),6.68(2H,d,J=7.6Hz,H-5′,7′),6.42(1H,d,J=15.6Hz,H-2),3.74(3H,s,H-1′′),3.32(2H,m,H-1′),2.64(2H,t,J=7.2Hz,H-2′);13C-NMR(150MHz,DMSO-d6))δ:165.8(C-1),156.1(C-6′),148.7(C-7),148.3(C-6),139.3(C-3),130.0(C-3′),129.9(C-4′,8′),126.9(C-4),122.0(C-9),119.5(C-2),116.1(C-8),115.6(C-5′,7′),111.2(C-5),56.3(-OCH3),41.1(C-1′),34.9(C-2′)。以上数据与文献报道基本一致[18],故鉴定化合物12为反式阿魏酸酰对羟基苯乙胺。
化合物13:白色粉末;HR-ESI-MS m/z:284.1281 [M+H]+;mp 261.3~262.3℃;1H-NMR(600MHz,CDCl3)δ:6.41(1H,d,J=15.6Hz,H-2),7.39(1H,d,J=8.2Hz,H-3),7.32(2H,d,J=15.6Hz,H-5,9),6.69(2H,d,J=8.2Hz,H-6,8),3.49(2H,t,J=7.4Hz,H-1'),2.65(2H,t,J=7.4Hz,H-2'),7.02(2H,d,J=8.0Hz,H-4',8'),6.79(2H,d,J=8.0Hz,H-5',7');13C-NMR(150MHz,CDCl3)δ:165.8(C-1),159.2(C-7),156.1(C-6'),139.0(C-3),130.0(C-5,9),129.9(C-4',8'),129.6(C-4),126.4(C-3'),119.2(C-2),116.2(C-6,8),115.6(C-5',7'),41.2(C-1'),34.9(C-2')。以上数据与文献报道基本一致[19],鉴定为N-反式对羟基肉桂酰基-对羟基苯乙胺。
化合物14:白色粉末;HR-ESI-MS m/z:205.1598[M-H]−;mp 140.2~142.7℃;1H-NMR(600MHz,CDCl3)δ:7.54(1H,d,J=8.4Hz,H-3),7.36(1H,brs,H-6),7.14(1H,brd,J=8.4Hz,H-4),1.33(9H,s,H-9~11),1.28(9H,s,H-12~14);13C-NMR(150MHz,CDCl3)δ:147.7(C-1),138.5(C-2),124.5(C-3),124.0(C-4),147.6(C-5),119.1(C-6),34.5(C-7),34.9(C-8),31.4(C-9~11),30.2(C-12~14)。以上数据与文献报道基本一致[20],鉴定化合物14为2,5-二叔丁基苯酚。
化合物15:无色油状物;HR-ESI-MS m/z:300.1230 [M+H]+;1H-NMR(600MHz,DMSO-d6))δ:7.37(2H,d,J=8.6Hz,H-5,9),7.31(1H,d,J=15.6Hz,H-3),7.14(1H,d,J=8.4Hz,H-4',8'),6.78(1H,d,J=8.6Hz,H-5',7'),6.71(2H,d,J=8.4Hz,H-6,8),6.49(1H,d,J=15.6Hz,H-2),4.54(1H,m,H-2'),3.18(1H,m,H-1′a),3.36(1H,m,H-1′b);13C-NMR(150MHz,DMSO-d6))δ:166.0(C-1),159.3(C-7),156.9(C-6'),139.1(C-3),134.6(C-5,9),129.7(C-3'),127.6(C-4),126.4(C-4',8'),119.3(C-2),116.2(C-5',7'),115.2(C-6,8),73.7(C-2'),47.5(C-1')。以上数据与文献对照基本一致[21],故鉴定化合物15为(E)-N-(2-hydroxy-2-(4-hydroxyphenyl)ethyl)-3-(4-hydroxyphenyl)acrylamide。
化合物16:淡黄色脂状物;HR-ESI-MS m/z:330.1336 [M+H]+;1H-NMR(600MHz,DMSO-d6))δ:7.14(2H,d,J=8.4Hz,H-4′,8′),7.11(1H,s,H-5),6.98(1H,d,J=7.8Hz,H-9),6.78(1H,d,J=7.8Hz,H-8),6.71(2H,d,J=8.4Hz,H-5′,7′),7.30(1H,d,J=15.6Hz,H-3),6.53(1H,d,J=15.6Hz,H-2),3.80(3H,s,H-1′′),3.38(1H,m,H-1′a),3.19(1H,m,H-1′b),4.53(1H,t,J=6.6Hz,H-2′);13C-NMR(150MHz,DMSO-d6))δ:166.0(C-1),156.9(C-6'),148.7(C-7),148.3(C-6),139.4(C-3),134.5(C-3'),127.6(C-4',8'),126.9(C-4),122.0(C-9),119.6(C-2),116.1(C-8),115.2(C-5',7'),111.2(C-5),71.7(C-2'),56.0(C-1''),47.5(C-1')。以上数据与文献对照基本一致[22],故鉴定化合物16为(S)-N-[2-hydroxy-2-(4-hydroxyphenyl)ethyl]-3-(4-hydroxy-3-methoxyphenyl)acrylamide。
化合物17:淡黄色脂状物;HR-ESI-MS m/z:485.3989 [M+H]+;1H-NMR(600MHz,DMSO-d6))δ:5.58(2H,m,H-10,11),5.38(2H,m,H-15,16),3.89(1H,m,H-9),3.88(1H,m,H-12),3.32(1H,m,H-13),2.16(2H,m,H-14),1.97(2H,t,J=7.2Hz,H-2),1.90(1H,m,H-8a),1.47(2H,m,H-17),1.38(3H,m,H-8b,7),1.28(8H,m,H-3~6),0.91(3H,t,J=3.6Hz,H-18);13C-NMR(150MHz,DMSO-d6))δ:174.6(C-1),134.6(C-10),131.9(C-11),129.4(C-16),126.7(C-15),74.0(C-13),73.6(C-12),70.5(C-9),40.1(C-8),37.4(C-2),30.0(C-14),29.0(C-4),28.8(C-5),28.6(C-6),25.0(C-7),24.6(C-3),20.2(C-17),14.1(C-18)。以上数据与文献对照基本一致[23],故鉴定化合物17为9S,12S,13S-三羟基-10E,15Z-十八碳二烯酸。
4 讨论
通过对汉麻根化学成分的研究,从中分离得到6个酚类、5个酪酰胺类、3个三萜类、1个倍半萜、1个多羟基十八碳烯酸、2个其他类化合物。该结果与汉麻地上部分对比,虽然具体化学成分在结构上有所不同,但化合物种类趋于一致,以酚类、酪酰胺为主,含部分萜类和多羟基十八碳烯酸等。根据文献报道,分离得到的化合物具有较好的生物活性,其中酚类成分对羟基苯甲醛(6)通过激活过氧化物酶体增殖物激活受体γ或AMP依赖的蛋白激酶信号通路和抑制细胞核内核转录因子-κB信号通路从而调控促炎因子的释放,具有抗炎作用[24],香草醛(7)通过调节信号通路抑制神经炎症,具有神经保护作用[25]。香草酸(9)可通过诱导自噬,从而缓解PA诱导的人肝癌HepG2细胞脂肪变性[26]。酪酰胺类成分:顺式阿魏酸酰对羟基苯乙胺(11)、反式阿魏酸酰对羟基苯乙胺(12)与(S)-N-[2-hydroxy-2-(4-hydroxyphenyl)-ethyl]-3-(4-hydroxy-3-methoxyphenyl)-acrylamide(16)均具有较强的抗氧化活性[27-28]。反式对羟基肉桂酸酰对羟基苯乙胺(13)对α-葡萄苷酶有明显抑制作用[29]。三萜类成分:木栓酮(1)有抗肿瘤活性[30]。齐墩果酸(3)具有保肝、抗炎、镇痛、抗肿瘤、抗病毒、抗焦虑等多种生物活性[31-33]。本研究进一步丰富了汉麻根的化学成分,为后续开展相关药理学研究等提供了物质基础。
利益冲突 所有作者均声明不存在利益冲突
参考文献
[1] 李俊,朱雪雯,万会花,等.大麻中大麻素类化学成分及其分析方法研究进展[J].中草药,2020,51(24):6414-6425.
[2] 肖乐,黄伟军,严桂香.汉麻色纺花式复合针织产品研发[J].天津纺织科技,2019(6):47-50.
[3] 张建春,关华,刘雪强,等.汉麻种植与初加工技术[M].北京:化学工业出版社,2009:255-256.
[4] 黄泰康.现代本草纲目[M].北京:中国医药科技出版社,2001:2634.
[5] 晋?葛洪撰.葛洪肘后备急方(八卷)[M].北京:人民卫生出版社,1963:121-147.
[6] 中华本草编委会.中华本草[M].第2册.上海:上海科学技术出版社,1999:475.
[7] Kornpointner C, et al. Chemical composition and antioxidant potential of Cannabis sativa L. roots[J].Ind Crops Prod, 2021, 165: 113422.
[8] Xia J H, Zhang S D, Li Y L, et al. Sesquiterpenoids and teiterpenoids from Abies holophylla and their bioactivities[J]Phytochemistry, 2012, 74: 178-184.
[9] 赵媛,夏琳,王丹,等.苹果树皮正己烷提取物化学成分研究[J].齐齐哈尔大学学报:自然科学版,2019,35(4):58-60.
[10] 邹娟,董明洪,周浪,等.荔波产香茶菜化学成分研究[J].中草药,2020,51(17):4405-4410.
[11] 徐阳宏,乌兰托娅,黄淑蕾,等.东北岩高兰正己烷萃取物的化学成分研究[J].齐齐哈尔大学学报:自然科学版,2019,35(4):61-62.
[12] Pettit G R, Du J, Pettit R K, et al. Antineoplastic agents. 554. the Manitoba bacterium Streptomyces sp.[J]J Nat Prod, 2006, 69(5): 804-806.
[13] 周宇娟,王俊豪,薛亚甫,等.铁皮石斛醋酸乙酯部位化学成分研究[J].中草药,2021,52(17):5218-5225.
[14] 刘绍华,王延亮,白家峰,等.岩木瓜茎干化学成分及PTP1B抑制活性研究[J].天然产物研究与开发,2016,28(11):1741-1746.
[15] 杜伟东,吴蓓,李志峰,等.小花清风藤化学成分的分离与鉴定(II)[J].中草药,2019,50(18):4277-4280.
[16] 徐凡,吴中含,易侨祺,等.老鸦糊乙酸乙酯部位化学成分及其抗炎活性[J].中成药,2021,43(10):2718-2723.
[17] 刘志华,王金兰,赵明,等.工业大麻地上部分化学成分研究[J].中草药,2021,52(15):4463-4472.
[18] 王金兰,李灵娜,贺礼东,等.牵牛全草的化学成分研究[J].天然产物研究与开发,2007,19(3):427-429.
[19] 郭志琴,郭强,朱枝祥,等.藏药多刺绿绒蒿的化学成分研究[J].中国中药杂志,2014,39(7):1152-1156.
[20] 夏少立,曹悦,李庆林,等.新疆一枝蒿的化学成分研究[J].中草药,2020,51(13):3393-3398.
[21] Wang X W, Zhao Y, Dong X Q, et al. Amides and lignans from Solanum lyratum[J]Phytochem Lett, 2021, 45: 25-29.
[22] Li X, Li X M, Xu G M, et al. Antioxidant metabolites from marine alga-derived fungus Aspergillus wentii EN-48[J]Phytochem Lett, 2014, 7: 120-123.
[23] Qiu Y K, Zhao Y Y, Dou D Q, et al. Two new alpha-pyrones and other components from the cladodes of Opuntia dillenii[J]Arch Pharm Res, 2007, 30(6): 665-669.
[24] 许晓飞,罗爱林,徐笑天,等.基于PPARγ/AMPK/NF-κB信号通路研究对羟基苯甲醛对TNBS诱导的小鼠克罗恩病的治疗作用[J].天然产物研究与开发,2022,34(6):925-933.
[25] 汤丽萍,闫瑾,范芳,等.香草醛对新生大鼠缺氧缺血性脑损伤的神经保护作用研究[J].现代生物医学进展,2021,21(20):3833-3840.
[26] 陈倩,伊力亚斯·艾萨,雷秀英,等.香草酸通过诱导自噬缓解HepG2细胞脂肪变性[J].中国临床药理学杂志,2021,37(19):2622-2626.
[27] 王路,孙睿,徐萌,等.阿魏化学成分?药理作用及毒理研究进展[J].世界中医药,2020,15(24):3887-3894.
[28] 张爱莲,于敏,徐宏化,等.齿瓣石斛的化学成分及其抗氧化活性[J].中国中药杂志,2013,38(6):844-847.
[29] Liu X C, Luo J G, Kong L Y. Phenylethyl cinnamides as potential alpha-glucosidase inhibitors from the roots of Solanum melongena[J]Nat Prod Commun, 2011, 6(6): 851-853.
[30] 张嵘,刘卓刚.木栓酮调控K562细胞增殖和细胞周期机制的初步研究[J].山西医药杂志,2012,41(11):1093-1095.
[31] 张明发,沈雅琴.齐墩果酸的药动学研究进展[J].药物评价研究,2017,40(11):1664-1670.
[32] de Melo C L, Queiroz M G R, Fonseca S G C, et al. Oleanolic acid, a natural triterpenoid improves blood glucose tolerance in normal mice and ameliorates visceral obesity in mice fed a high-fat diet[J]Chem Biol Interact, 2010, 185(1): 59-65.
[33] Kim S H, Hong J H, Lee Y C. Oleanolic acid suppresses ovalbumin-induced airway inflammation and th2- mediated allergic asthma by modulating the transcription factors T-bet, GATA-3, RORγt and Foxp3 in asthmatic mice[J]Int Immunopharmacol, 2014, 18(2): 311-324.
文献摘自:佟雪琦,赵明,李军,王金兰,时志春,王丹,孙立秋,赵英楠,张树军.汉麻根化学成分研究[J].中草药,2022,53(24):7649-7655.