摘 要:四环素类抗生素因其用量大、难生物降解和潜在的生态毒性而日益受到关注。此外,传统的污水处理方法难以去除这些污染物。本研究采用高温煅烧-磺化法制备磺化改性苎麻生物炭(SBC),并将其作为过硫酸盐活化剂,实现了对水中盐酸四环素(TCH)的高效去除。通过扫描电子显微镜(SEM)、比表面积分析仪(BET)、傅里叶变换红外光谱(FT-IR)对SBC的形貌和结构进行表征,研究了溶液初始pH值、SBC投加量、PS投加量对SBC/PS体系中TCH降解效果的影响,并考察了SBC的重复利用性能。研究结果表明,SBC为片层介孔材料,其表面含有丰富的含氧官能团和黄原酸酯官能团。在初始pH为3,PS投加量为10mmo/lL,SBC投加量为0.5g/L的最优条件下,反应180min后,SBC/PS体系对TCH的去除率达到89.1%,明显优于SBC、苎麻秸秆原始生物炭(BC)、PS和BC/PS体系。在实验考察范围内,SBC/PS体系对TCH的降解性能随pH值(pH=3-11)的升高呈先降低后升高再降低的趋势;随SBC和PS的投加量的升高,TCH的去除率呈先上升后下降的趋势。自由基淬灭实验和电子顺磁共振(EPR)实验表明,SBC/PS体系降解TCH的过程中产生了硫酸根自由基(SO-4·)、羟基自由基(·OH)、超氧自由基(O·2·)和单线氧(1O2),1O2起主导作用。循环利用实验结果表明,SBC表现出良好的重复利用性能。研究认为SBC是一种环境友好、高效的非金属碳基过硫酸盐活化剂,具有良好的应用前景。
关键词:生物炭、过硫酸盐活化剂、盐酸四环素、磺化改性、催化降解
四环素类抗生素是一类水溶性较好的广谱抗生素,被广泛应用于养殖业和医疗行业[1-2]。四环素类抗生是由四个苯环或氢化苯环直向并联组成的抗生素,其主要包括四环素(TC)、土霉素(OTC)和金霉素(CTC),盐酸四环素(TCH)是四环素盐酸盐,其更容易被人体和动物吸收,使用更为广泛[3]。但是,四环素类抗生素不能被动物或人体完全吸收,也难以通过常规污水处理方法去除[4],这导致四环素类抗生素极易进入自然水体。目前已在自然水体中广泛检测到四环素类抗生素的存在[5]。过量使用四环素类抗生素会导致其在环境中的大量累积并产生抗性基因进而威胁到人类和动植物的生存[6-7]。因此,亟需研制一种有效的四环素类抗生素的去除技术。
基于过硫酸盐的高级氧化技术可通过多种方式活化过硫酸盐产生硫酸根自由基(SO-4),相比于羟基自由基(OH),SO-4具有更高的氧化还原电位、更长的半衰期、更广的pH适用范围[8-9],具有降解四环素类抗生素的巨大潜能被广泛应用于抗生素等有机污染物的去除[10-12]。声、光、热、电在活化过硫酸盐的同时伴随着大量的能量损耗;过渡金属离子活化效率高,但反应过快导致试剂不能充分利用;非均相过渡金属虽然利用率高,但存在金属离子浸出引发二次污染的环境风险[13]。因此,开发活化性能更高、更稳定、更环境友好的过硫酸盐活化剂是当下研究的热点。非金属碳基材料具有结构丰富、环境友好、催化高效、无二次污染的优点[14]。氧化石墨烯、活性炭、碳纳米管、生物炭等非金属碳基材料已应用于过硫酸盐活化[15]。原子掺杂是碳材料重要的改性方法,原子掺杂可以增加碳材料表面官能团和表面缺陷,为过硫酸盐活化提供更多活性位点[13]。目前掺杂的原子种类有氮、硫、磷、硼,其中硫原子掺杂的相关研究较少,但已有研究表明硫掺杂非金属碳基材料具有高效活化过硫酸盐去除有机污染物的能力[14-16]。硫掺杂非金属碳基材料可通过一锅煅烧法和后处理法制备[13]。磺化改性是一种后处理法,通过这种方法制备硫掺杂碳材料活化过硫酸盐降解TCH的效果还未知。近年来,为促进农业废弃物的资源化利用,实现农业可持续发展,以农业废弃生物质制备生物炭材料用于环境治理的研究成为热点。苎麻秸秆生物炭属于非金属碳基材料,其含有丰富的含氧官能团[17],含氧官能团被认为是活化过硫酸盐的主要成分[18],因此,苎麻秸秆生物炭具有高效活化过硫酸盐的巨大潜能。
鉴于此,本文选择农田废弃苎麻秸秆制备了苎麻秸秆原始生物炭(BC),然后采用磺化改性掺杂硫原子制备了磺化苎麻秸秆生物炭(SBC),并活化过硫酸盐(PS)降解水中TCH,分析了PS、BC、SBC、BC/PS和SBC/PS体系对水中TCH的去
除能力,探究了初始pH、PS投加量、SBC投加量对SBC/PS体系中TCH降解效果的影响,以及SBC重复利用性能,通过自由基淬灭实验和电子顺磁共振(EPR)证实了SBC活化PS降解TCH的自由基和1O2途径。
1材料与方法
1.1材料与试剂
生物炭原料:苎麻秸秆取自于湖南长沙某地农田。
实验试剂:盐酸四环素(C22H24N2O8·HCl)、氢氧化钠(NaOH)、二硫化碳(CS2)、硝酸(HNO3,65%-68%)、过硫酸钠(Na2S2O8)、甲醇(CH4O)、叔丁醇(C4H10O)、糠醇(C4H6O2)、对苯醌(C6H4O2)、高氯酸(HCIO4)试剂均购于上海麦克林生化科技有限公司,均为分析纯及以上等级。
1.2实验仪器
电子天平(FA2004N,常州市幸运电子设备有限公司)、水质分析仪(HQ40D,美国哈希)、电热鼓风干燥箱(JC-TR-12,青岛聚创环保设备有限公司)、真空干燥箱(DZF-6020,上海精宏实验设备有限公司)、恒温水浴振荡器(SHA-B,金坛区金城海澜仪器制造厂)、紫外可见光分光光度计(UV-752上海佑科仪器仪表有限公司),破碎机(800Y,永康市铂欧五金制品有限公司),管式炉(SGTM-100,洛阳市西格玛仪器制造有限公司)。
1.3苎麻秸秆原始生物炭(BC)制备
先用超纯水清洗干净,再在电热鼓风干燥箱内80℃烘干至恒重,冷却至室温后放入破碎机内破碎,过100目筛,密封保存备用。
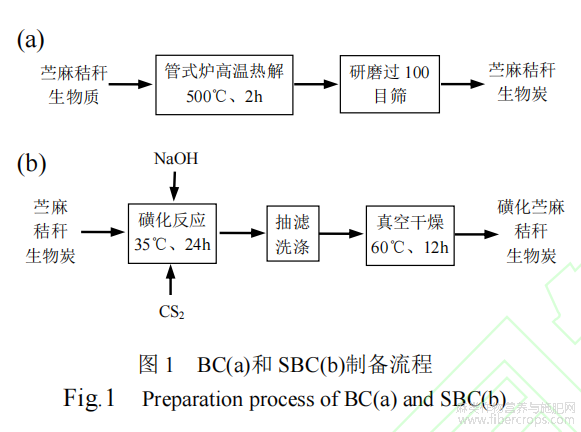
苎麻秸秆原始生物炭(BC)制备(见图1(a)):取适量生物炭原料于坩埚中,将坩埚放置于管式炉的恒温段,在氮气氛围中以10℃/min的升温速率升至500℃后,保持温度烧制2h,冷却至室温后取出,研磨过100目筛,密封保存备用,将制备的苎麻秸秆生物炭命名为BC。
1.4磺化改性苎麻秸秆生物炭(SBC)制备
磺化改性苎麻秸秆生物炭(SBC)制备(见图1(b)):磺化改性参考[19],将0.3gBC分散在100mL0.1mol·L-1的NaOH中,加入3mLCS2,在35℃恒温水浴振荡器中振荡24h,过滤分离,并用去离子水清洗生物炭直至中性,在60℃真空干燥箱中干燥12h,冷却至室温后取出研磨并过100目筛,用密封袋密封保存备用,将制备的磺化改性苎麻秸秆生物炭命名为SBC。
1.5 生物炭材料表征
生物炭的比表面积和孔隙结构采用物理吸附分析仪(美国麦克ASAP 2460)测定,形貌采用超高分辨率场发射扫描电子显微镜(日本日立 SU8020)测定,表面官能团采用傅里叶红外光谱仪(Nicolet IS10)测定,表面元素采用能谱(日本HORIBA HORIBA EX-350)测定。
1.6 TCH降解实验
采用自行配置的20mg/L的TCH溶液,取100mL于锥形瓶中,加入0.05g生物炭,先暗吸附1h,然后加入10mmol/LPS1mL,接触2h,在预定时间取2.5mL样品,加入0.5mL甲醇淬灭反应,经0.22μm滤膜过滤后测定TCH的吸光度并计算其浓度,实验均在35℃、130r/min的水浴振荡器中进行,溶液初始pH采用0.1mol/L的NaOH和HNO3调节。根据预实验结果,在pH为3,PS投加量为10mmol/L,催化剂投加量为0.5g/L的条件下,探究了BC、SBC、BC/PS、SBC/PS和PS体系对水中TCH的降解效果。为了探究不同初始pH值对水体中TCH降解的影响,在PS的投加量10mmol/L,SBC投加量为0.5g/L的条件下,分别设置初始pH为3,5,7,9和11;为了探究不同PS投加量对TCH降解的影响,在pH为3,SBC投加量为0.5g/L的条件下,分别设置了PS的投加量为1,5,10,15和20mmol/L;为了探究催化剂的投加量对水体中TCH降解的影响,在pH为3,PS的投加量为10mmol/L的条件下,分别设置了SBC的投加量为0.1,0.3,0.5,0.8和1.0g/L;为了鉴定反应中产生的活性物种,在pH为3,PS的投加量为10mmol/L,SBC投加量为0.5g/L的条件下,分别加入0.1mol/L的甲醇(MeOH)、叔丁醇(TBA)、糠醇、对苯醌和高氯酸捕获活性物种。
1.7 TCH的测定方法
TCH的浓度采用紫外可见光分光光度计(UV-752上海佑科仪器仪表有限公司)测定,检测波长为356nm。
1.8数据处理
根据TCH的标准曲线计算反应过程中不同时刻TCH的浓度,t时刻TCH的去除率的表达式见式(1),暗吸附1h的去除率为吸附去除率,反应3h的去除率为总去除率,总去除率与吸附去除率的差值即为催化降解率。

式中:R表示t时刻TCH的去除率;C0表示TCH初始浓度;Ct表示t时刻TCH的浓度。
2结果与讨论
2.1生物炭材料的表征
2.1.1 BET分析
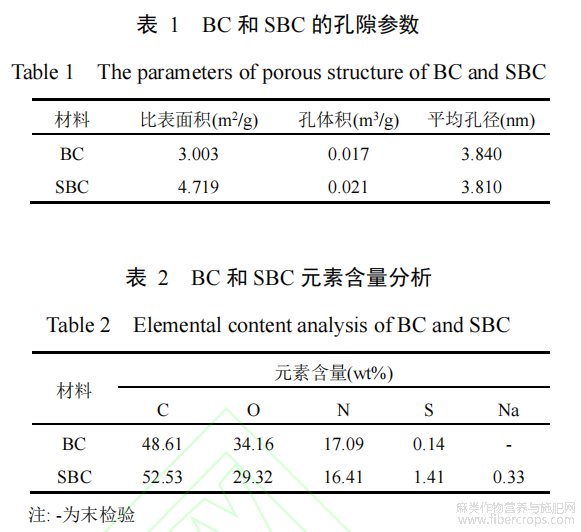
图2(a)为BC和SBC的吸附—脱附等温线。在相对压力达到0.8~1.0时,BC和SBC的吸附量增长速率显著增加,具有明显的H3型滞后回环,属于典型的Ⅳ型吸附。这表明BC和SBC均是片层材料,都存在介孔。图2(b)为BC和SBC的孔径分布曲线,在3.8nm处,BC和SBC都有明显的尖峰,说明BC和SBC孔径在3.8nm比较多,BC和SBC孔径分布集中在2~50nm,说明BC和SBC是介孔材料。表1为BC和SBC的孔隙参数,BC和SBC的比表面积分别为3.003m2/g和4.719m2/g,孔体积分别为0.017m3/g和0.021m3/g,平均孔径分别为3.840nm和3.810nm。
2.1.2 SEM和EDS分析
图3(a)和图3(b)显示了BC和SBC的SEM图像。从SEM图像中可以清楚的看出BC为表面光滑的片状结构,且表面有许多小孔。SBC表面粗糙,表面有许多半球形突起,表面的小孔被覆盖。这是由于磺化反应在生物炭表面形成黄原酸酯涂层,涂层覆盖了小孔并形成突起[20]。表2为BC和SBC的元素含量分析,可以看出磺化反应后,硫元素含量显著增加,大约是磺化前的10倍,这说明硫原子成功掺杂到生物炭表面。
2.1.3 FT-IR分析
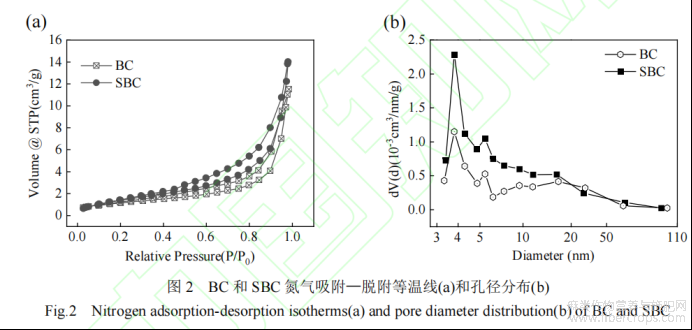
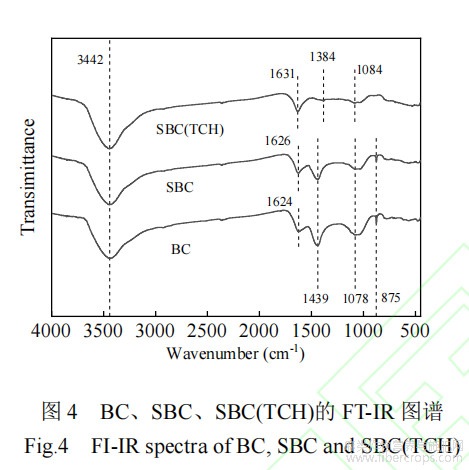
对BC、SBC、降解TCH后的SBC(TCH)进行FT-IR分析,如图4所示,BC在3442cm-1、1624cm-1、1439cm-1、1078cm-1和875cm-1有明显的特征峰,分别与O-H键的伸缩振动、C=O、C-OH、-COOH和-OH变形振动有关,这表明BC中含有丰富的含氧官能团。对于SBC,在1626cm-1和1439cm-1处的振动是C=S伸缩振动,在1439cm-1和1078cm-1的振动分别对应C-OH和-COOH的变形振动,在3442cm-1和1624cm-1处的振动分别对应O-H和C=O的伸缩振动。反应后的SBC,在1631cm-1处对应的是C=S伸缩振动,在1631cm-1处的特征峰是黄原酸基团的特征峰[21]。在1439cm-1和1078cm-1处的特征峰强度减弱,这表明含氧官能团和含硫官能团参与了PS的活化。
2.2不同体系对TCH降解效果比较
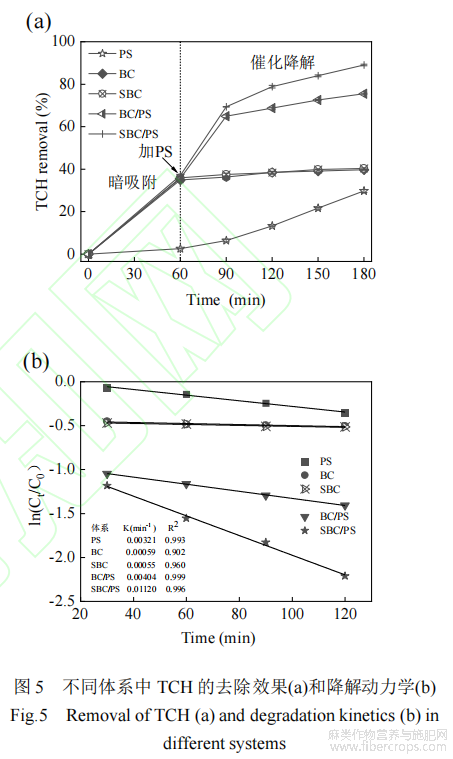
探究了PS、BC、SBC、BC/PS和SBC/PS五种体系对TCH的去除效果。如图5(a)所示,在反应180min后,投加单一PS、BC和SBC的体系中,TCH的去除率分别为29.7%、39.7%和40.1%,BC/PS和SBC/PS体系对TCH的去除率分别为75.5%和89.1%,说明BC/PS和SBC/PS体系通过吸附和催化降解共同作用来实现对TCH的去除,BC/PS体系以吸附作用为主,SBC/PS体系以催化降解作用为主。仅单独使用PS时,TCH有部分降解,这可能是在酸性条件下H+可直接活化PS产生SO-4,促进TCH的降解[22],但酸活化的作用不显著。如图5(b)所示,分析了不同体系下TCH降解动力学,单一PS、BC、SBC体系的一级反应动力学常数分别为0.00321min-1、0.00059min-1和0.00055min-1,BC/PS和SBC/PS体系的一级反应动力学常数分别为0.00404min-1和0.01120min-1。BC/PS和SBC/PS体系的一级反应动力学常数均大于单一体系,说明BC、SBC与PS之间存在协同作用,SBC与PS之间的协同作用更明显。
2.3TCH降解影响因素分析
2.3.1溶液初始pH对TCH降解的影响
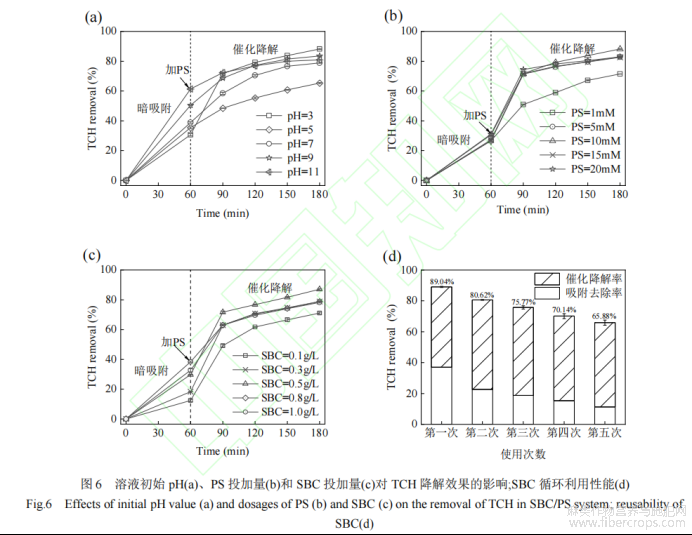
无论是吸附还是催化反应中,溶液的初始pH都起着重要作用,初始pH会影响PS和TCH的形态,还会影响自由基的氧化性能[23-24]。采用SBC/PS体系进行一系列降解实验。如图6(a)所示,在暗吸附阶段,不同pH条件下吸附去除率分别为30.6%、35.3%、38.8%、50.4%和61.3%。TCH的吸附去除率随pH的增大而增大,pH为11时的吸附去除率约是pH为3时的2倍,这是因为TCH有三个酸碱中心区,其pKa值大小分别为pKa1=3.30、pKa2=7.44和pKa3=9.27[25],TCH的等电点位的pH值为5.4,当溶液pH值小于等电点位时,TCH表面带正电,当溶液pH值大于5.4时,TCH表面带负电[26],而SBC表面整体带正电荷,随着pH的升高,静电斥力逐渐减弱,吸附作用逐渐增强,这表明SBC吸附TCH时,静电作用力扮演重要角色,这与之前研究结果一致[27]。反应180min后,不同pH条件下吸附去除率分别88.4%、65.3%、78.8%、83.4%和80.9%。pH为3的体系TCH的去除率和催化降解率均高于其他pH体系。在pH为5时,TCH的去除率最低,这可能是酸性降低,酸活化作用减弱,而酸性降低促进了PS与H2O反应生成非自由基离子HSO-4,体系中产生的自由基最少,对TCH的去除率最低[28]。碱性条件下TCH的去除率大于中性条件,这是因为碱性条件能够活化PS产生更多自由基[29],但是随着碱性的增强,TCH的去除率下降,这是因为碱性越强,SO-4和OH−反应生成的OH越多,而SO-4是降解TCH的主要自由基[30]
2.3.2PS投加量对TCH降解的影响
PS投加量对TCH降解的影响如图6(b)所示,反应180min后,不同PS投加量条件下,TCH的去除率分别为71.4%、82.9%、88.4%、82.6%和82.9%。当PS的投加量从1mmol/L增加到10mmol/L,SBC活化PS产生的SO-4增加,TCH的去除率也随之增加。但是当PS的投加量进一步增加,自由基发生自淬灭[31],导致参与TCH降解的SO-4减少,TCH的去除率降低。
2.3.3SBC投加量对TCH降解的影响
SBC投加量对TCH降解效果的影响如图6(c)所示,在暗吸附阶段,不同SBC投加量条件下,TCH的去除率分别为12.4%、18.4%、29.8%、32.7%和38.4%,TCH的吸附去除率随着SBC投加量的增加而增加。反应180min后,不同SBC投加量条件下,TCH的去除率分别为71.1%、78.9%、87.1%、78.9%和78.2%,TCH的去除率呈现先增加后降低的趋势,这主要是因为SBC投加量从0.1g/L增加到0.5g/L,PS活化的活性位点逐渐增加,产生的自由基也逐渐增加,从而TCH的去除率逐渐增大[32],但是当SBC的投加量从0.5g/L增加到1.0g/L,SBC活化产生的大量自由基,但不能及时与TCH接触而发生自淬灭或失活[33],从而抑制了TCH的降解。
2.4SBC重复重复利用性能
将SBC从反应后的溶液中通过抽滤分离,并用超纯水反复冲洗,然后放入60℃真空干燥箱中烘干,重复使用。如图6(d)所示,SBC使用5次后,SBC/PS体系对TCH的去除率从89.04%下降至65.88%。随着重复使用次数的增加,吸附的位点被占据,导致吸附去除率不断降低[34]。且第二次使用TCH吸附去除率较第一次下降显著,这可能是因为吸附过程中,有机小分子堵塞了孔道,导致吸附量下降[24]。每次重复使用,吸附去除率下降的量大于催化降解率下降的量,说明SBC吸附性能下降是SBC/PS体系中TCH去除率下降的主要原因。
2.5SBC/PS体系去除TCH的机制分析
2.5.1降解途径的探讨
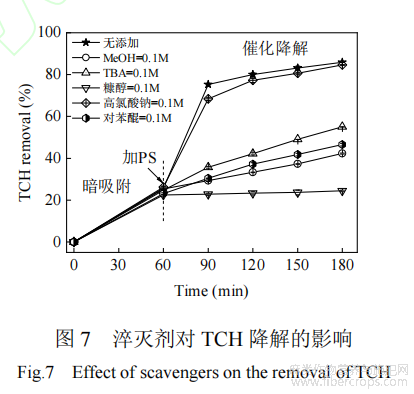
原子掺杂生物炭活化过硫酸盐降解污染物的途径有自由基、非自由基(1O2和电子传递)途径[35]。为探究SBC/PS体系去除TCH的降解途径,采用MeOH作为SO-4和OH的淬灭剂,TBA和对苯醌分别作为OH和O-2的淬灭剂来鉴定自由基对TCH降解的贡献[33]。采用糠醇和高氯酸钠分别鉴定1O2和电子传递对TCH降解的贡献[36-37]。如图7所示,向体系中加入高氯酸钠,基本没有抑制TCH的降解,说明电子转移途径对体系中TCH的降解贡献很小。加入MeOH、TBA、对苯醌和糠醇均抑制了TCH的降解,其中糠醇的抑制效果最明显,这表明SBC/PS体系去除TCH过程中产生了SO-4、OH、O-2和1O2,1O2对TCH的降解起主导作用。
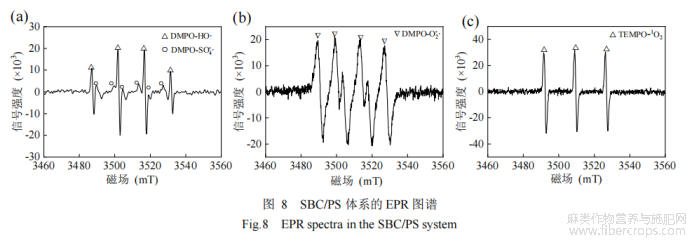
为了进一步验证体系中的自由基和非自由基途径,采用二甲基吡啶氮-氧化物(DMPO)捕获自由基,采用四甲基哌吡啶酮(TEMPO)捕获1O2,在降解反应进行5min时,通过电子顺磁共振仪(EPR)检测DMPO和TEMP分别与自由基和1O2的加合物。如图8(a)所示,1:2:2:1的特征峰是DMPO与OH结合形成的,在四重特征峰之间1:1:1:1:1:1的特征峰是DMPO与SO-4结合形成的,图8(b)中1:1:1:1的特征峰是DMPO与O-2结合形成的,图8(c)中有明显的TEMPO-1O2的三重特征峰[38],说明体系中同时存在SO-4、OH、O-2和1O2。综合淬灭实验和EPR分析,可以确SO-4、OH、O-2和1O2均是参与TCH降解的活性物种,且1O2是一种对于TCH降解非常有效的活性物种。
2.5.2SBC/PS体系去除TCH的机制探究
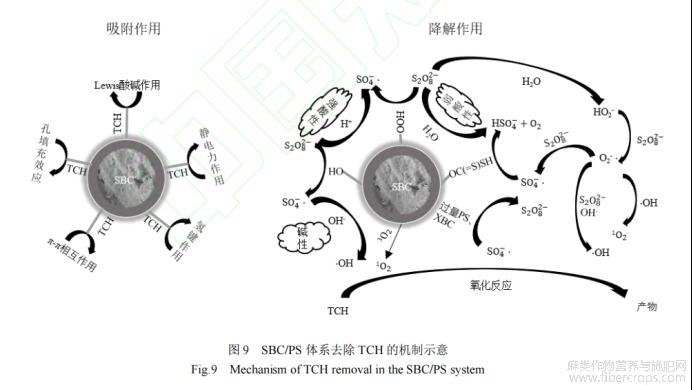
如图9所示,SBC/PS体系通过吸附和催化降解两大机制协同去除TCH。由BET测试可知,经过磺化后,苎麻生物炭材料比表面积和孔体积增加,从而促进其通过孔填充效应吸附TCH[39]。由FT-IR测试可知,SBC材料表面含有丰富的含氧官能团,通过磺化改性后表面增加了含硫官能团,丰富的官能团使得SBC通过π-π作用力、氢键作用力、静电力、Lewis酸碱作用、疏水作用等作用吸附TCH分子[40]。
在催化降解过程中,如式(2)、(3)和(4),表面含氧官能团(羟基和羧基)和含硫官能团(黄原酸酯)促进PS结构中O-O键断裂产生SO-4[19],SO-4进一步和溶液中的OH-反应生成OH(见式(5))。PS在SBC的催化作用下产生O-2(如式(6)-(7)),O-2通过自由基链式反应促进SO-4、OH和1O2的生成(如式(8)-(10))[41]。此外,基态氧分子3O2从SBC上获得能量被激发为单线氧1O2(如式(11)),整个体系在SO-4、OH、O-2和1O2的共同作用下促进TCH的降解。综上,SBC的表面结构有利于其对TCH分子的吸附,表面的羟基、羧基等含氧官能团和黄原酸酯官能团对PS起到活化作用,通过SBC的吸附和催化降解作用,提升了SBC/PS体系对TCH的去除效果。
3结论
3.1
通过磺化改性成功将硫原子掺杂到生物炭表面,表征结果表明,磺化改性苎麻生物炭属于片状介孔材料,材料表面有黄原酸酯涂层,含有丰富的含氧官能团。
3.2
SBC/PS体系降解TCH的效果受到初始pH、催化剂投加量、PS投加量的影响。在初始pH为3,PS投加量为10mmol/L,SBC投加量为0.5g/L,反应温度为35℃的条件下,SBC/PS体系对初始浓度为20mg/L的TCH的去除率达到89.1%,明显优于SBC、BC、PS和BC/PS体系。
3.3
SBC丰富的羟基、羧基等含氧官能团黄原酸酯官能团为PS活化提供了大量活性位点,促进体系中产生SO-4·、·OH、O-2·和1O2,其中1O2是一种对于TCH降解非常有效的活性物种,在TCH的降解中起主导作用。
3.4
SBC/PS体系通过吸附和催化降解两大机制协同去除水中TCH,本实验中,SBC对TCH的吸附去除率最高达到38.4%。SBC表现出良好的重复使用性能,使用5次后,TCH的降解率仍然可达65%以上。但随着SBC重复使用次数的增加,SBC的吸附性能显著下降,催化性能下降幅度较小,SBC吸附性能下降是SBC/PS中TCH去除率下降的主要原因。
3.5
SBC具有良好的活化过硫酸盐降解四环素类抗生素的应用前景,后续可以进一步通过优化SBC制备的条件进一步提高对四环素类抗生素的降解效果,也可尝试用于去除其他有机污染物。
参考文献
[1]Ramachanderan R, Schaefer B. Tetracycline antibiotics[J].Chemtexts, 2021,7(3):1-42.
[2]Caco AI, Varanda F, de Melo MJP, et al. Solubility of Antibioticsin Different Solvents. Part II. Non-Hydrochloride Forms of Tetracycline and Ciprofloxacin[J]. Industrial & Engineering Chemistry Research,2008,47(21):8083-8089.
[3]陈小平,王萌,杨长明,等.四环素类抗生素在我国水环境污染现状及其对水生生物的毒性研究进展[J].应用化工,2021,50(10):2780-2785.ChenX P, Wang M, Yang C M, et al. Review of contaminations in water of tetracyclines in China and toxicity on aquatic organisms[J]. Applied Chemical Industry, 2021,50(10):2780-2785.
[4]Borghi AA, Palma MA. Tetracycline: production, waste treatment and environmental impact assessment[J]. Brazilian Journal of Pharmaceutical Sciences, 2014,50(1):25-40.
[5]Xu LY, Zhang H, Xiong P, et al. Occurrence, fate, and risk assessment of typical tetracycline antibiotics in the aquatic environment: A review[J]. Science of the Total Environment, 2021,753:141975.
[6]Wang DB, Jia FY, Wang H, et al. Simultaneously efficient adsorption and photocatalytic degradation of tetracycline by Febased MOFs[J].Journal of Colloid and Interface Science, 2018,519:273-284.
[7]Ngigi AN, Ok YS, Thiele-Bruhn S. Biochar-mediated sorption of antibiotics in pig manure[J]. Journal of Hazardous Materials, 2019,364:663-670.
[8]Anipsitakis GP, Dionysiou DD. Degradation of organic contaminants in water with sulfate radicals generated by the conjunction of peroxymonosulfate with cobalt[J]. Environmental Science & Technology, 2003,37(20):4790-4797.
[9]Ghauch A, Tuqan A. Oxidation of bisoprolol in heated persulfate/H2O systems: Kinetics and products[J]. Chemical Engineering Journal, 2012,183:162-171.
[10]陈天民,陈颢明,马红玉,等.炭基-Co3O4复合材料活化过一硫酸盐降解阿特拉津[J].中国环境科学,2020,40(11):4786-4794.Chen T M, Chen H M, Ma H Y, et al. Biochar-Co3O4 composite activates peroxymonosulfate to degrade atrazine[J]. China Environmental Science, 2020, 40(11):4786-4794.
[11]苏冰琴,刘一清,林昱廷,等.Fe3O4磁性纳米颗粒激活过硫酸盐体系同步去除水中的诺氟沙星和铅[J/OL].中国环境科学. https://doi.org/10.19674/j.cnki.issn1000-6923.20211009.001.Su B Q, Liu Y Q, Lin Y T, et al. Simultaneous removal of Norfloxacin and Pb(Il) from aqueous solutions through Fe3O4activated persulfate system[J/OL]. China Environmental Science. https://doi.org/10.19674/j.cnki.issn1000-6923.20211009.001.
[12]Nguyen THA, Oh SY. Oxidation of phenol by persulfate activated by zero-valent iron-biochar composites[J/OL]. Chemical Engineering Communications.https://doi.org/10.1080/00986445.2021.1983546.
[13]王华哲,郭婉茜,任南琪.生物炭基非金属过硫酸盐活化剂的开发与应用[J].环境科学学报,2020,40(10):3582-3589.Wang H Z, Guo W Q, Ren N Q. Development and application of biochar-based metal-free persulfate activators[J]. Journal of Environmental Sciences, 2020, 40(10):3582-3589.
[14]Zhong QF, Lin QT, He WJ, et al. Study on the nonradical pathwaysof nitrogen-doped biochar activating persulfate for tetracycline degradation[J]. Separation and Purification Technology, 2021,276(2):119354.
[15]Yang SY, Zhang A, Ren TF, et al. Surface Mechanism of CarbonBased Materials for Catalyzing Peroxide Degradation of Organic Pollutants in Water[J]. Progress in Chemistry, 2017,29(5):539-552.
[16]Guo YP, Zeng ZQ, Zhu YC, et al. Catalytic oxidation of aqueous organic contaminants by persulfate activated with sulfur-doped hierarchically porous carbon derived from thiophene[J]. Applied Catalysis B-Environmental, 2018,220:635-644.
[17]Tan X, Shaaban M, Yang J, et al. Efficient Removal of HexavalentChromium from an Aquatic System Using Nanoscale Zero-Valent Iron Supported by Ramie Biochar[J]. NANOMATERIALS, 2021,11(10):2698.
[18]陈卫刚,武海霞,樊佳炜.活性炭非均相活化不同过硫酸盐降解偶氮染料酸性橙Ⅱ[J].环境工程,2020,38(08):113-118+157.Chen W G, Wu H X, Fan J W. Activated Carbon Heterogeneous Activation of Different Persulfates to Degradation Azo Dye Acid Orange Ⅱ[J]. Environmental Engineering, 2020, 38(08):113-118+157.
[19]Yang Z, Zhao ZW, Yang X, et al. Xanthate modified magnetic activated carbon for efficient removal of cationic dyes and tetracycline hydrochloride from aqueous solutions[J]. Colloids and Surfaces a-Physicochemical and Engineering Aspects, 2021,615.
[20]Lv L, Chen N, Feng CP, et al. Xanthate-modified magnetic chitosan/poly (vinyl alcohol) adsorbent: Preparation, characterization, and performance of Pb(II) removal from aqueous solution[J]. Journal of the Taiwan Institute of Chemical Engineers, 2017,78:485-492.
[21]熊道陵,李金辉,钟洪辉.应用基团电负性理论分析丙三醇黄原酸钠抑制毒砂作用机理[J].中南大学学报(自然科学版), 2010,41(06):2156-2161.Xiong D L, Li J H, Zhong H H. Analysis of suppression mechanism of arsenopyrite by glycerol sodium xanthogenate using group electronegatixity theory[J]. Journal of Central South University(Natural Science Edition), 2010, 41(06):2156-2161.
[22]黄伟英,刘菲,鲁安怀,等.过氧化氢与过硫酸钠去除有机污染物的进展[J].环境科学与技术,2013,36(09):88-95.Huang Wei-ying,Liu Fei,Lu An-huai,et al. Removal of organic pollutants by hydrogen peroxide and sodium persulfate: a review[J]. Environmental Science & Technology,2013,36(9):88-95.
[23]杨珂,唐琪,杨晓丹,等.铁酸铜非均相活化过硫酸盐降解罗丹明B[J].中国环境科学,2019,39(09):3761-3769.Yang K, Tang Q, Yang X D, et al. Degradation of rhodamine B by heterogeneous activation of persulfate with copper ferrate[J]. China Environmental Science, 2019, 39(09):3761-3769.
[24]Zhu K, Shen YQ, Hou JM, et al. One-step synthesis of nitrogen and sulfur co-doped mesoporous graphite-like carbon nanosheets as a bifunctional material for tetracycline removal via adsorption and catalytic degradation processes: Performance and mechanism[J]. Chemical Engineering Journal, 2021,412:128521.
[25]曾令泽,高鸿慈.关于四环素类药物pKa值的讨论[J].中国药学杂志,1987,22(01):56.Zeng L Z, Gao H C. Discussion on pKa value of tetracycline drugs[J]. Chinese Pharmaceutical Journal, 1987, 22(1):56-56.
[26]李宗宸,魏群山,罗专溪,等.水土比、pH和有机质对沉积物吸附四环素的复合影响[J].农业环境科学学报,2017,36(04):761-767.Li Z C, Wei Q S, Luo Z X, et al. Combination effects of pH, solution/soil ratio and inherent organic matter on the adsorption of tetracycline by sediments[J]Journal of Agro-Environment Science, 2017,36(04):761-767.
[27]李国亭,李康丽,张帅阳,等.木质纤维素生物炭对亚甲基蓝和四环素的吸附对比研究[J].江苏农业科学,2021,49(18):234-240.Li G T, Li K L, Zhang S Y, et al. Comparative study on adsorption of methylene blue and tetracycline by lignocellulosic biochar[J]. Jiangsu Agricultural Sciences, 2021, 49(18):234-240.
[28]Rao LJ, Yang YF, Liu XD, et al. Heterogeneous activation of persulfate by supporting ferric oxalate onto activated carbon fibers for organic contaminants removal[J]. Materials Research Bulletin, 2020,130:110919.
[29]周阳,应路瑶,于欣,等.碱热联合活化过硫酸钠氧化降解2,4-二氯苯酚研究[J].水处理技术,2021,47(03):68-72.Zhou Y, Ying L Y, Yu X, et al. Study on Oxidative Degradation of 2,4-Dichlorophenol by Alkaline and Thermal Co-activated Sodium Persulfate[J]. Technology of Water Treatment, 2021,47(03):68-72.
[30]Furman OS, Teel AL, Ahmad M, et al. Effect of Basicity on Persulfate Reactivity[J]. Journal of Environmental EngineeringAsce, 2011,137(4):241-247.
[31]Guan YH, Ma J, Ren YM, et al. Efficient degradation of atrazine by magnetic porous copper ferrite catalyzed peroxymonosulfate oxidation via the formation of hydroxyl and sulfate radicals[J]. Water Research, 2013,47(14):5431-5438.
[32]Li J, Ren Y, Ji FZ, et al. Heterogeneous catalytic oxidation forthe degradation of p-nitrophenol in aqueous solution by persulfate activated with CuFe2O4 magnetic nano-particles[J]. Chemical Engineering Journal, 2017,324:63-73.
[33]Shao FL, Wang YJ, Mao YR, et al. Degradation of tetracycline in water by biochar supported nanosized iron activated persulfate[J]. Chemosphere, 2020,261:127844.
[34]Cui QT, Zhang W, Chai SY, et al. The potential of green biochar generated from biogas residue as a heterogeneous persulfate activatorand its non-radical degradation pathways: Adsorption and degradation of tetracycline[J]. Environmental Research, 2022,204:112335.
[35]Guo YP, Zeng ZQ, Li YL, et al. In-situ sulfur-doped carbon as a metal-free catalyst for persulfate activated oxidation of aqueous organics[J]. Catalysis Today, 2018,307:12-19.
[36]李凯,刘新璐,李辉,等.狐尾藻生物炭活化过硫酸盐降解四环素的研究[J].环境科学与技术,2021,44(06):50-57.Li K, Liu X L, Li H, et al. Research of Tetracycline Degradation by Persulfate Activated with Myriophyllum spicatum Biochar[J].Environmental Science & Technology, 2021,44(06):50-57.
[37]Xia DH, Yin R, Sun JL, et al. Natural magnetic pyrrhotite as a high-Efficient persulfate activator for micropollutants degradation: Radicals identification and toxicity evaluation[J]. Journal of Hazardous Materials, 2017,340:435-444.
[38]Cheng X, Guo HG, Zhang YL, et al. Non-photochemical production of singlet oxygen via activation of persulfate by carbon nanotubes[J].Water Research, 2017,113:80-88.
[39]Tang L, Yu JF, Pang Y, et al. Sustainable efficient adsorbent: Alkali-acid modified magnetic biochar derived from sewage sludge for aqueous organic contaminant removal[J]. Chemical Engineering Journal,2018,336:160-169.
[40]Yujia Xiang, Zhangyi Xu, Yuyi Wei, et al. Carbon-based materials as adsorbent for antibiotics removal: Mechanisms and influencing factors[J]. Journal of Environmental Management, 2019,237:128-138.
[41]Mahamadou Kamagate AAA, Tiangoua Kone, Lacina Coulibaly, Khalil Hanna. Activation of persulfate by irradiated laterite for removal offluoroquinolones in multi-component systems[J]. Journal of Hazardous Materials, 2018,346:159-166.
文章摘自:董康妮,谢更新,晏铭,晏卓逸,熊鑫.磺化苎麻生物炭活化过硫酸盐去除盐酸四环素的效能及影响因素研究[J/OL].中国环境科学:1-10[2022-07-19].DOI:10.19674/j.cnki.issn1000-6923.20220507.014.